首页 > 医疗资讯/ 正文
亮点摘要
-
本研究基于FIGARO-DKD三期临床研究,首次系统揭示了非类固醇矿物皮质激素受体拮抗剂(MRA)Finerenone在血浆蛋白组中的动态调控特征。
-
Finerenone不仅调节经典的RAAS通路相关蛋白,还显著影响纤维化、免疫炎症、能量代谢及神经内分泌等多重生物通路。
-
其中,神经肽Y(NPY)作为一种血管收缩性神经肽,被Finerenone持续下调,揭示了其可能的新型治疗机制和靶点价值。
研究概述
近日,发表在European Heart Journal上的一项后期分析,深度挖掘了FIGARO-DKD试验中Finerenone对血浆蛋白组的影响。该研究涵盖929名慢性肾病(CKD)合并2型糖尿病(T2D)患者,样本来自21个国家115个研究中心。在长达4年的随访期间,通过高通量蛋白组学平台(Olink Explore3072)检测近3000种生物标志物,采用线性混合模型分析Finerenone与安慰剂组间的蛋白质表达差异,厘清了Finerenone多维度的分子作用网络及其潜在的心肾保护机制,为其临床应用提供了更为丰富的生物学依据。

研究背景
Finerenone是一种非类固醇选择性矿物皮质激素受体拮抗剂,已经在多个大规模临床试验中显示出对CKD和T2D患者心血管及肾脏结局的显著改善效果,且在射血分数≥40%的心力衰竭患者中减少心衰事件和心血管死亡风险。现有的动物及临床前研究显示Finerenone可减轻心肾器官的结构损伤,降低蛋白尿和钠潴留,伴随炎症及纤维化相关生物标志物的显著下降。但关于Finerenone在人类体内影响全景蛋白组的详细情况尚缺乏,此项研究旨在填补这一空白,系统描绘Finerenone治疗下的动态蛋白表达变化及相关生物通路,为理解其广泛的临床获益机制提供分子层面证据。
研究方法
本项研究为FIGARO-DKD临床试验的生物标志物亚组分析,共纳入929例患者,分为Finerenone组(474例)和安慰剂组(455例)。所有患者均合并CKD和T2D,基础均使用RAAS抑制剂治疗。研究采用Olink Explore3072蛋白组学平台,纵向检测4个月至48个月内共计4193份血浆样本,涵盖2941种蛋白质标志物。通过线性混合模型(考虑治疗组、时间点、性别及其交互作用),结合严格的多重检验校正(FDR q≤0.01),识别出对Finerenone响应的蛋白标志物。进一步运用R语言包bc3net进行生物路径富集分析,探讨Finerenone调控的关键生物学路径及其演变。
主要研究结果
1. 患者基线特征
指 标
数 值
中位年龄
64岁 (IQR 59-70)
男性比例
75%
中位eGFR
65.3 mL/min/1.73m² (IQR 49.4-81.3)
尿白蛋白/肌酐比 (UACR)
>97%患者≥30 mg/g
既往心血管疾病史
34.6%
心血管住院史
17.3%
所有患者均在试验前接受RAAS抑制剂治疗。
2. Finerenone调节的关键蛋白标志物
-
总计273个蛋白质在Finerenone组与安慰剂组中显示显著差异(FDR q ≤ 0.01),其中156个在两个及以上连续时间点显著改变,28个在所有测量时间点(4月至48个月)稳定存在差异。
-
具体蛋白质中,Neuropeptide Y(NPY)、B型利钠肽(BNP)和线粒体肌酸激酶(CKMT1A/B)呈持续下调趋势。
-
Apolipoprotein-L1(APOL1)、小GTP酶Rab-6A(RAB6A)及免疫激活标志物CD69显著上调。
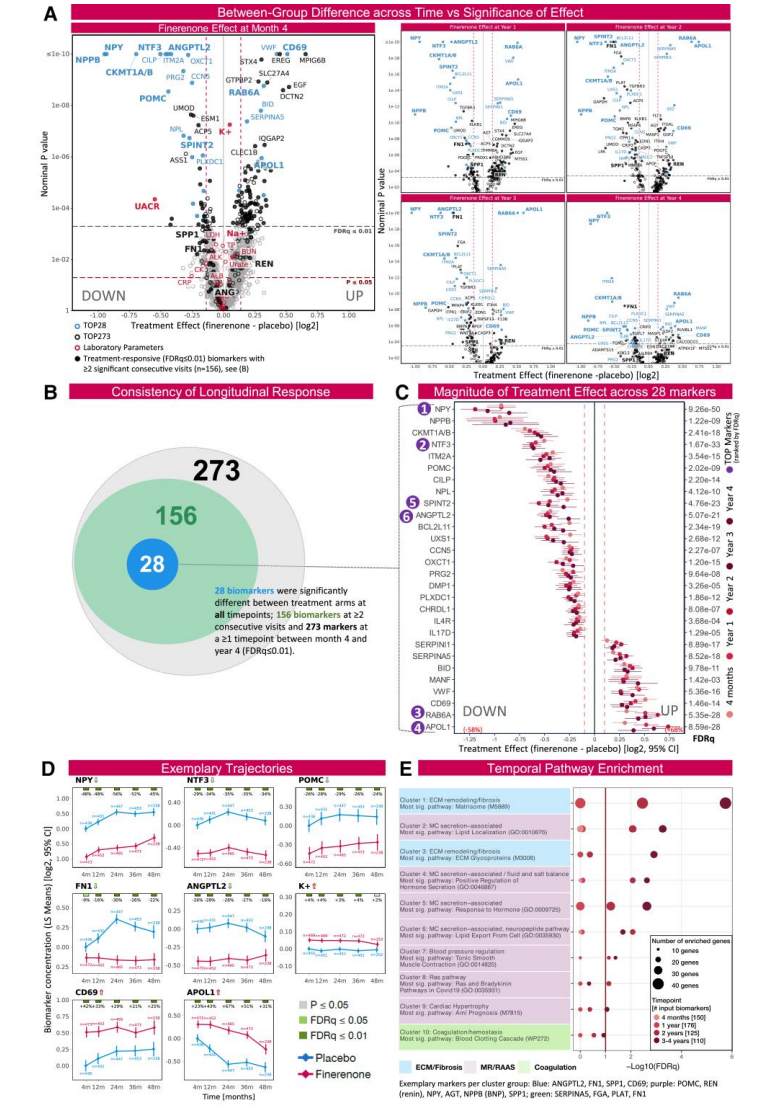
图:Finerenone诱导的血浆蛋白组变化及相关通路
3. 经典RAAS通路及电解质变化
-
Finerenone显著调控肾素、其底物血管紧张素原(AGT)和促肾上腺皮质激素(POMC),表明对RAAS通路的强烈调节作用。
-
血清钾(K+)和钠(Na+)轻微变化,符合MR阻断的反馈调节预期。
4. 生物路径富集分析
-
ECM重塑及纤维化通路:Finerenone治疗2年以上后,纤维连接蛋白(Fibronectin)和骨桥蛋白(Osteopontin)明显下降,提示其抗纤维化效应。
-
矿物皮质激素分泌及血流动力学调节通路:确认了Finerenone对MR/RAAS靶点的有效作用。
-
凝血与止血通路:相关蛋白表达变化反映Finerenone对血液动力学和血液系统的潜在影响。
5. 神经肽Y(NPY)与其他标志物的临床及生物学意义
-
NPY是一种具有多效性的神经激素,具有显著的血管收缩作用,其持续下调可能解释Finerenone改善心血管重构和肾病进展的机制之一。
-
现有文献表明,NPY的异常升高与不良心脏重塑和肾功能恶化密切相关。
-
其他如NTF3(神经营养因子-3)、CD69(T细胞活化标志物)、ANGPTL2(促炎性脂肪因子)、RAB6(细胞内运输蛋白)及APOL1(高密度脂蛋白成分,相关于蛋白尿性肾病)均提示Finerenone广泛调控神经内分泌、免疫调节及能量代谢的复杂网络。
研究价值与意义
本项研究通过高通量蛋白组学手段,拓宽了人们对Finerenone作用机制的认知,不再局限于其对RAAS及矿物皮质激素受体的调控,而是揭示了其对心肾病患者神经内分泌、纤维化、免疫炎症、能量代谢及血液动力学等多重通路的综合调节。NPY的持续下调尤为引人注目,提示这一神经肽有望成为Finerenone心肾保护新靶点。此外,部分免疫和代谢标志物的变化,反映Finerenone可能通过免疫调节和能量代谢平衡参与病理改善,提供未来多靶点治疗设计的新思路。
虽然本项分析为随机对照试验的后期亚组分析,缺乏基线蛋白组数据,但由于母体随机分组的均衡性,该发现具有较高可信度。研究结果需进一步通过机制实验和前瞻性研究验证其临床意义。整体而言,该研究极大深化了Finerenone作为新型非类固醇MRA的分子作用图谱,助力精准治疗策略的制定,为CKD和T2D合并心血管疾病患者提供新的管理思路。
原始出处
Berger M, MacNamara A, Ferreira JP, Kolkhof P, Voss S, Skubala A, Scalise A, et al. Finerenone effects on biomarkers: an analysis from the FIGARO-DKD trial. Eur Heart J. 2025;00:1-5. https://doi.org/10.1093/eurheartj/ehaf316
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)