首页 > 医疗资讯/ 正文
移植血管重构是导致同种异体器官移植终末期失功的主要原因,以心脏移植为例,其10年发生率高达50%。阐明移植血管重构的发生机制对于临床防治器官移植失功具有重要意义。研究表明,移植血管外膜中形成的三级淋巴组织是介导移植物免疫排斥及血管重构的关键环节。同时,三级淋巴组织中富集大量T滤泡辅助(Tfh)细胞,驱动B细胞成熟为记忆B细胞和浆细胞,并控制生发中心的形成。然而,移植血管处Tfh细胞的来源及分化机制尚未完全阐明。
2025年6月24日,中南大学湘雅三医院蔡菁菁教授团队联合浙江大学徐清波教授团队在Circulation上发表题为“Mitochondrial 1-Carbon Metabolism Drives CD34 Lineage Cells to Differentiate into Tfh Cells to Form Tertiary Lymphoid Organ in Transplant Arteriosclerosis”的研究论文。该研究表明,移植血管处Tfh细胞主要源于胸腺CD34谱系细胞,并经淋巴网络转运至移植血管外膜;其中线粒体一碳代谢途径介导了胸腺来源CD34谱系CD4+ T细胞向Tfh细胞的分化。同时,研究证实CD4+ T细胞中一碳代谢关键酶-亚甲基四氢叶酸脱氢酶2 (MTHFD2)可作为潜在分子靶点,用于预防移植血管三级淋巴组织形成及血管重构,为未来移植血管重构的机制研究与药物研发提供了新思路。

该研究首先基于CD34谱系示踪小鼠(Cd34-CreERT2; Rosa26-tdTomato)建立了同种异体移植血管模型,联合免疫荧光、流式细胞术、单细胞测序等技术显示,移植血管术后4周存在大量CD34谱系来源T细胞浸润,且在血管外膜三级淋巴组织处富集(图1)。同时,清除CD34谱系T细胞可显著抑制血管外膜三级淋巴组织形成并改善移植血管重构(图1)。
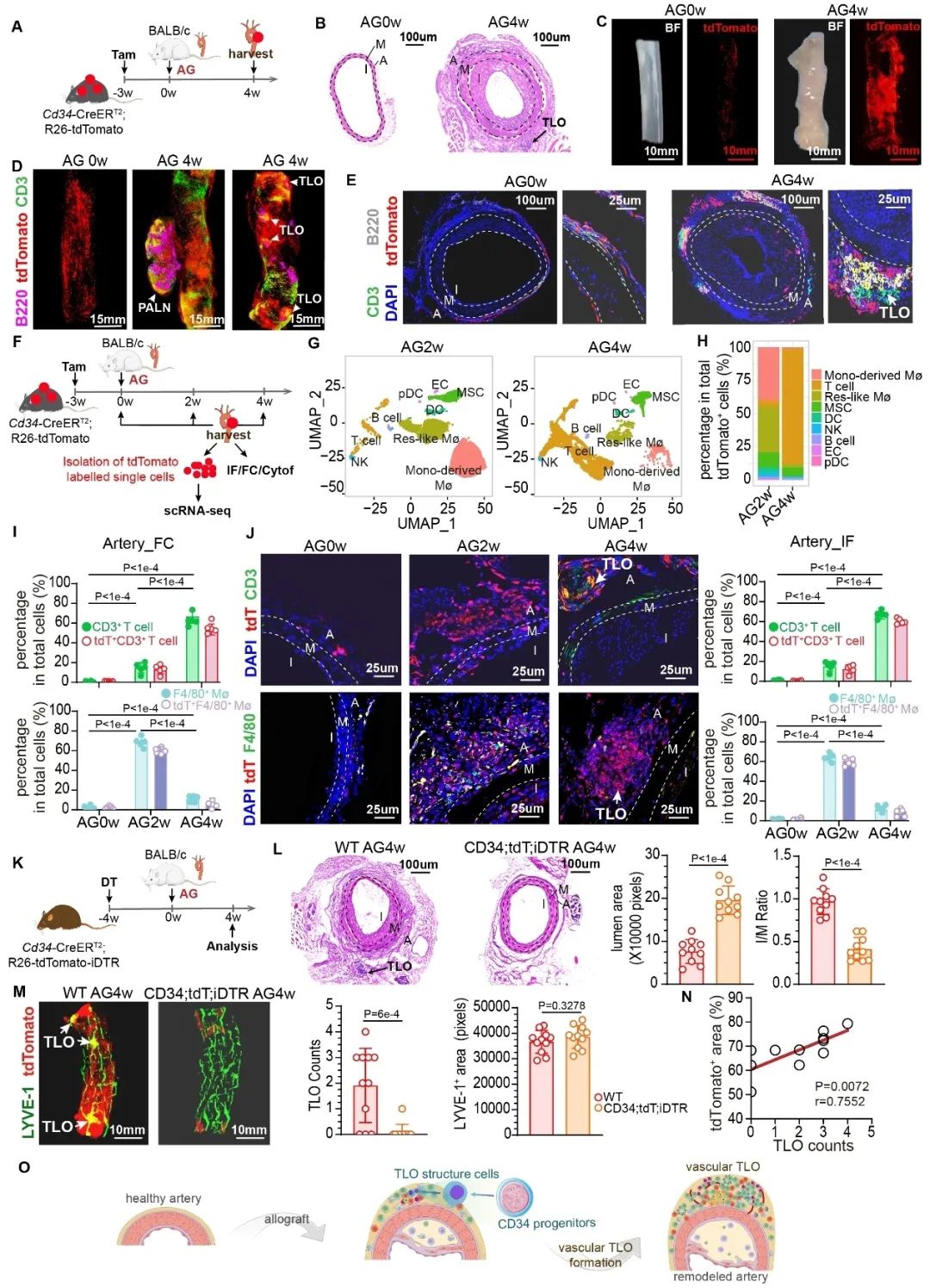
图1. CD34谱系细胞分化为T细胞并促进移植血管三级淋巴组织形成
随后,研究进一步探讨移植血管处CD34谱系T细胞的来源及其转运途径。联合胸腺切除术、淋巴结切除术、骨髓移植术及淋巴管抑制剂干预,研究阐明移植血管处CD34谱系T细胞主要来源于胸腺,并通过淋巴网络转运至移植血管外膜(图2)。靶向“胸腺-淋巴结-淋巴管”这一CD34谱系T细胞生成及转运途径可有效抑制血管外膜三级淋巴组织形成并改善血管重构(图2)。
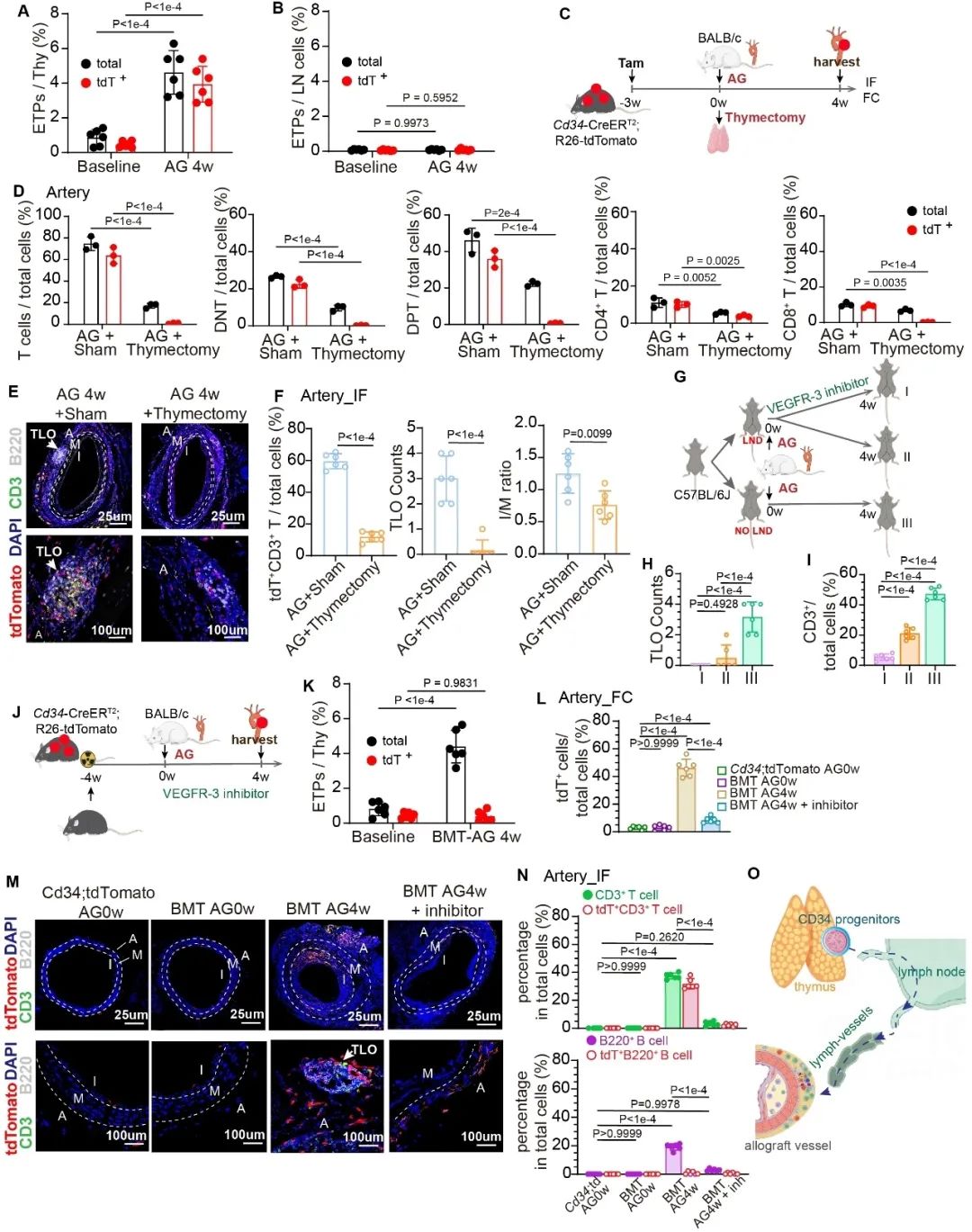
图2. 移植血管处CD34谱系T细胞主要来源于胸腺并通过淋巴网络转运
进一步,研究旨在阐明CD34谱系CD4+ T细胞的分化亚型及其在移植血管中的关键作用。通过单细胞测序、质谱流式细胞术以及流式细胞术等分析发现,CD34谱系CD4+ T细胞主要分化为效应T细胞,特别是Tfh细胞,且CD34谱系细胞并不分化为B细胞(图3)。相互作用分析发现,CD34谱系CD4+ T细胞中Tfh细胞与生发中心相关B细胞亚群相互作用密切。清除CD34谱系T细胞后,生发中心相关B细胞亚群显著减少,提示CD34谱系CD4+ T细胞分化为Tfh细胞并促进移植血管三级淋巴组织形成(图3)。
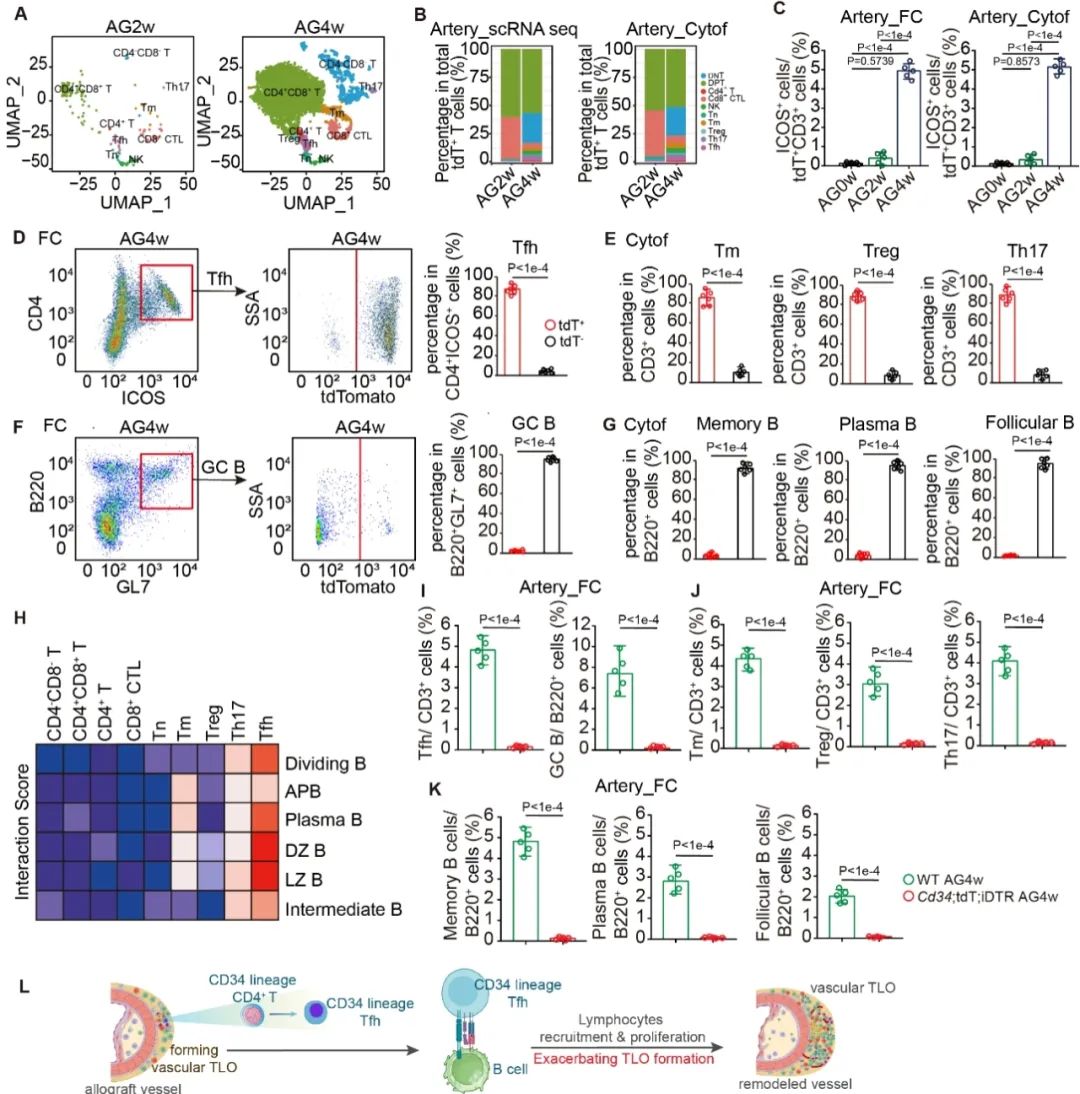
图3. CD34谱系CD4+ T细胞分化为Tfh细胞并促进移植血管重构
为了进一步探讨CD34谱系CD4+ T细胞分化为Tfh细胞的分子机制,研究通过单细胞测序数据的轨迹分析和代谢推断,鉴定到一碳代谢是CD34谱系CD4+ T细胞分化为Tfh细胞的关键代谢通路(图 4)。同时,基于体外CD4+ T细胞向Tfh细胞分化模型与同位素标记质谱分析,发现是线粒体中的一碳代谢途径(而非胞浆)介导了CD34谱系CD4+ T细胞向Tfh细胞的分化(图 5)。基于这些发现,研究进一步证实一碳代谢关键酶—亚甲基四氢叶酸脱氢酶2 (MTHFD2)能有效抑制CD34谱系CD4+ T细胞分化为Tfh细胞,减缓移植血管外膜三级淋巴组织形成,并最终改善血管重构(图 6)。
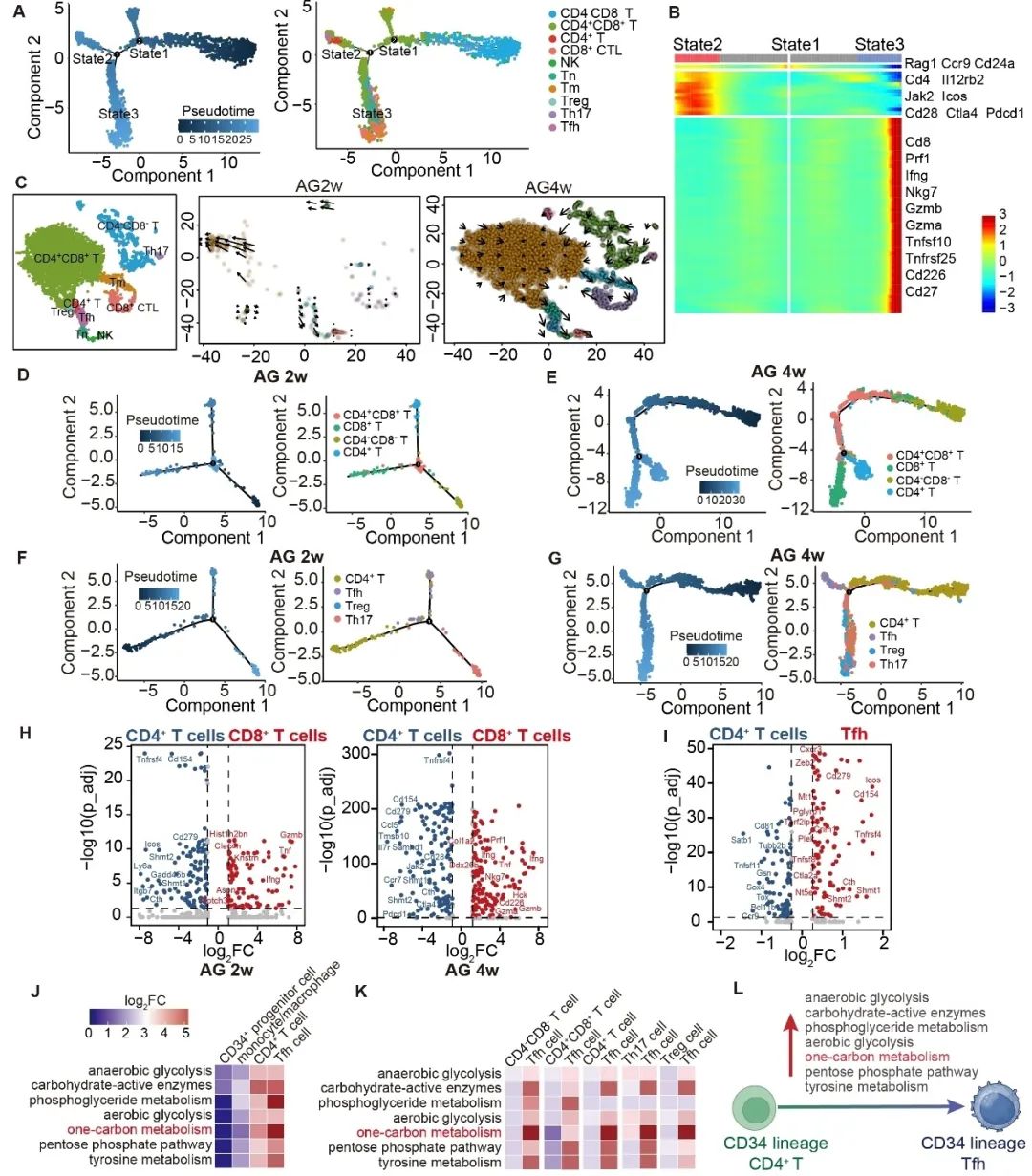
图4. 一碳代谢促进CD34谱系CD4+ T细胞分化为Tfh细胞
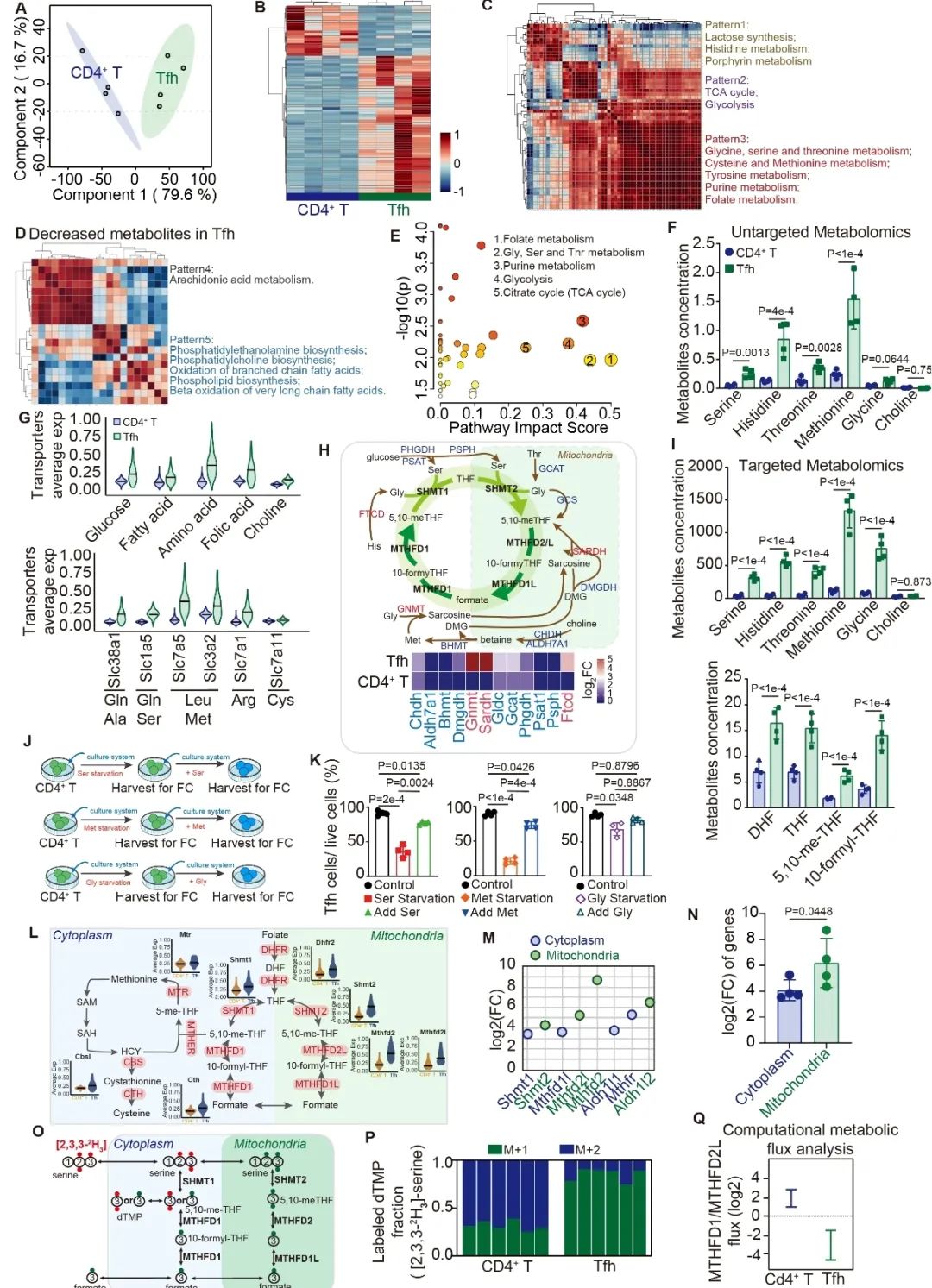
图5. 线粒体一碳代谢促进CD34谱系CD4+ T细胞分化为Tfh细胞
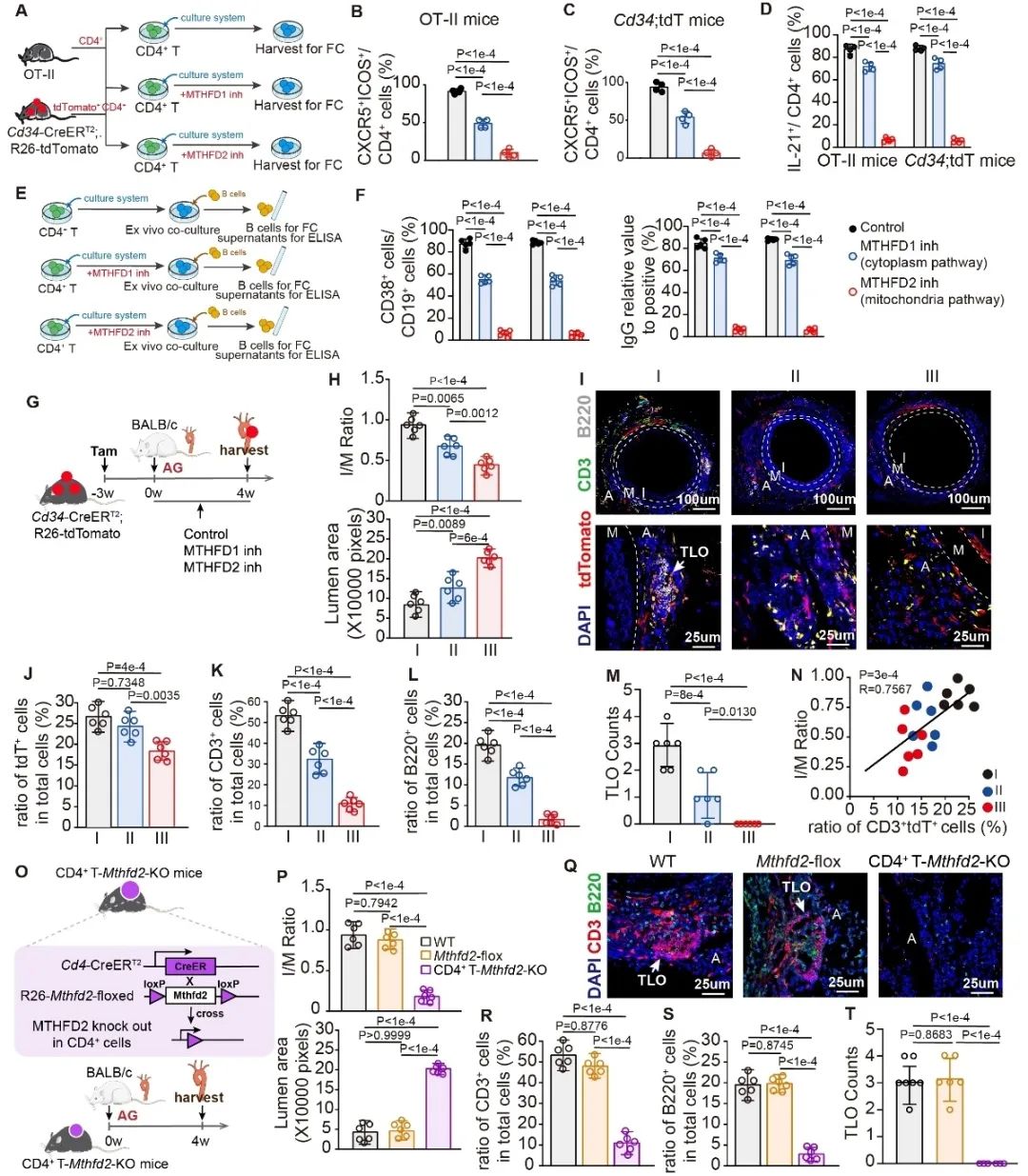
图6. 靶向线粒体一碳代谢酶MTHFD2改善移植血管重构
综上所述,该研究表明,移植血管处的CD34谱系T细胞主要来源于胸腺,这些细胞通过淋巴管网络转运至移植血管外膜。进一步研究发现,线粒体一碳代谢途径介导了CD34谱系CD4+ T细胞向Tfh细胞的分化,并驱动三级淋巴组织的形成。靶向线粒体一碳代谢酶MTHFD2可显著抑制移植血管处三级淋巴组织形成,从而改善血管重构(图7)。
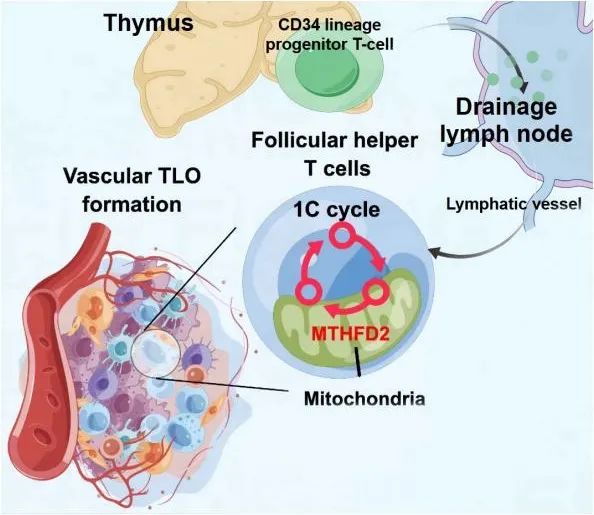
图7. 移植血管中CD34谱系Tfh细胞来源及其分化机制
中南大学湘雅三医院孙雪菁博士、伍俊儒博士后为文章共同第一作者。中南大学湘雅三医院蔡菁菁教授、浙江大学徐清波教授为该文章的通讯作者。同时该研究得到了中南大学湘雅三医院袁洪教授、陆瑶教授的大力支持。
该工作得到了国家卫健委四大慢病重大专项、国家自然科学基金、湖南省自然科学基金、湖南省“三尖”创新人才工程等项目资助。
原文链接:
https://doi.org/10.1161/CIRCULATIONAHA.125.07369
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)