首页 > 医疗资讯/ 正文
引言
白癜风(Vitiligo)作为一种慢性、无法治愈的自身免疫性皮肤疾病,以其独特的黑素细胞受损机制导致的局部或大面积的白斑而广泛关注。全球发病率约为0.5%到2%,我国患者人数已超过3000万,且每年仍在持续增加。这一数字背后,隐藏着巨大的医疗、心理和社会负担。白癜风不仅毁坏外貌,还严重影响患者的生活质量,可能引发自卑、抑郁甚至自杀,成为公共卫生领域亟待解决的难题。
白癜风的发病机制复杂而多元,至今尚未找到完全的根本性治疗方案。传统方案主要依赖于激素类药物、免疫抑制剂等,疗效有限且伴有不少副作用。近年来,随着免疫学和神经科学的快速发展,科学家们逐渐揭示了白癜风中免疫反应之外的神经调控机制,为治疗带来了新思路。
白癜风的现状与挑战
目前,临床治疗白癜风的“金标准”尚未确立。激素类药物虽然短期能改善皮损,但是疗效有限、易复发,且长期使用可能引发皮肤萎缩等副作用。免疫抑制剂如钙调神经磷酸酶抑制剂(如他克莫司)也在部分患者中见效,但由于安全性问题和疗效不稳定,不足以成为主流。
在药物研发方面,靶向治疗治疗碧玺即基于免疫调控的药物逐步问世。免疫学研究显示,白癜风的发病机制主要由黑素特异性CD8+ T细胞攻击黑素细胞引起,但如何有效地阻断这个过程,目前仍缺乏理想药物。JAK抑制剂(如鲁索替尼)已获FDA批准,成为治疗白癜风的突破性药物,但其疗效仍待提升,且存在部分不良反应,限制了其临床应用范围。
神经免疫交叉:白癜风的新“破局钥匙”
近年来,研究揭示,白癜风不仅仅是免疫细胞的“战场”,更是神经系统参与的“舞台”。神经纤维在皮肤中的丰富程度远超预期,尤其是感觉神经纤维分泌的神经肽如CGRP(降钙素基因相关肽)被发现具有免疫调节作用。上海交通大学医学院的王宏林团队从基础到临床,系统探索了一条全新的“感觉神经-免疫”交互通路,为白癜风的治疗带来了曙光。
这项最新研究于2025年6月16日在《Immunity》杂志线上发表,揭示了“感觉神经元-CGRP-真皮类型I树突状细胞-CD8+ T细胞”的致病机制。具体来说,白癜风患者的皮损区,感觉神经密度明显增加,尤其是释放CGRP的神经纤维与活跃的真皮cDC1(类型I树突状细胞)紧密缠绕、空间邻近。此发现提示,神经信号可能通过调控免疫细胞的功能,放大自身免疫反应。

机制解析:神经免疫互作轴的“秘密”
研究团队运用前沿的单细胞联合空间转录组学技术,对正常及白癜风皮肤样本进行深度解析,首次发现白癜风皮损中存在常规Ⅰ型树突状细胞(cDC1)与CD8+ T细胞的关键互作。尤为重要的是,真皮层cDC1细胞特异性高表达降钙素基因相关肽(CGRP)受体CALCRL-RAMP1,暗示其可能受CGRP信号调控。CGRP主要由皮肤中深入表皮层的Nav1.8+/TRPV1+ 感觉神经分泌,是已知的皮肤免疫应答调控者。
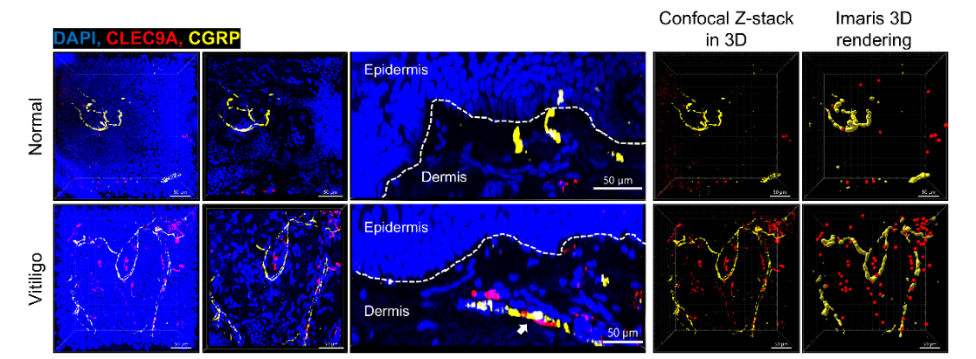
图:白癜风皮损区CGRP+感觉神经密度和真皮cDC1数量均显著增加且二者空间邻近
基于此线索,团队利用先进的皮肤全包埋透明化成像技术进行观察,发现白癜风患者皮损区CGRP+ 感觉神经密度和真皮cDC1数量均显著增加,且两者在空间分布上紧密相邻,强烈提示存在“CGRP+ 感觉神经-真皮cDC1”的相互作用。
深度验证:动物模型揭示致病机制链条
为深入探究,团队构建了高度模拟人类白癜风的小鼠模型,并利用多种基因工程荧光报告小鼠(如Nav1.8-tdTomato、Xcr1-tdTomato)进行追踪:
-
神经的关键作用: 模型小鼠皮肤中同样观察到CGRP+ 神经密度和真皮cDC1增加。特异性消融感觉神经可显著抑制白癜风发展;而在神经消融小鼠中外源性回补CGRP,则能重现疾病表型,确证感觉神经及其分泌的CGRP驱动疾病。
-
cDC1的核心地位: 模型小鼠皮损内真皮cDC1不仅数量增多,其形态由圆形变为树突状,表明活化状态,并紧密缠绕CGRP+ 神经纤维。体内实验证实,消融或扩增真皮cDC1直接影响疾病进程,证明cDC1是激活致病性CD8+ T细胞所必需的。
-
受体验证与机制闭环: 构建cDC1特异性敲除CGRP受体基因(Calcrl)小鼠(cKO)后,发现其发病显著减轻。体外共培养体系进一步证明,感觉神经元或CGRP能显著增强cDC1的抗原提呈能力及促进CD8+ T细胞产生IFN-γ,且此效应依赖CGRP受体CALCRL。
综合人体发现与动物实验,团队创新性提出并证实了白癜风的核心致病机制:感觉神经元-CGRP-cDC1-CD8+ T细胞轴。该轴中,感觉神经分泌的CGRP通过其受体CALCRL作用于真皮cDC1,促使cDC1活化并启动自身反应性CD8+ T细胞攻击黑色素细胞。
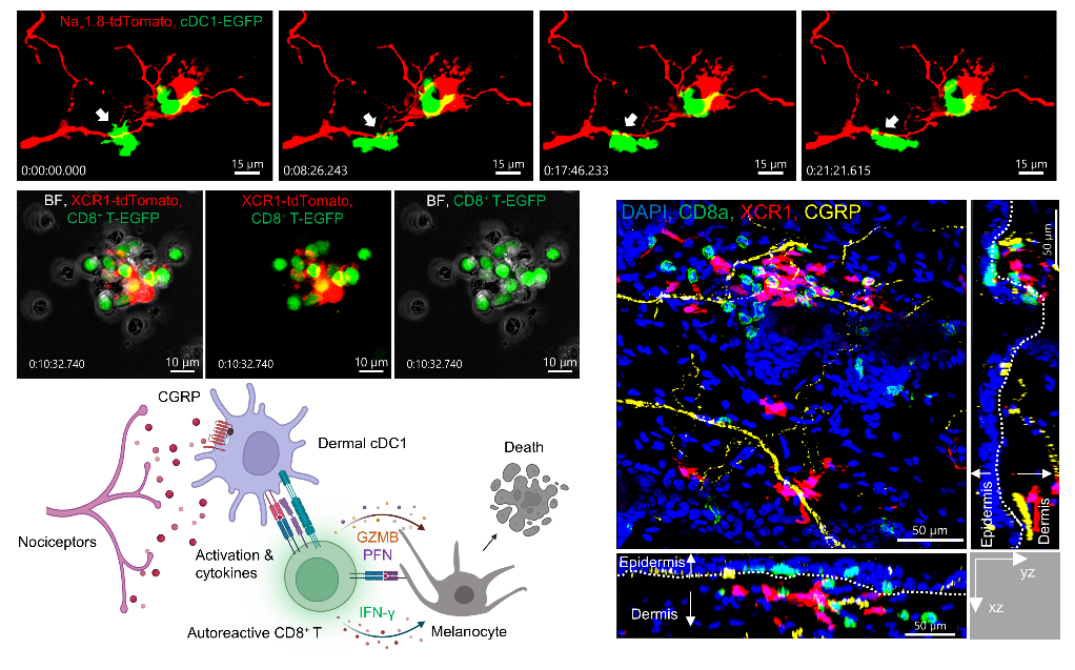
临床验证:从动物到患者的“新药之路”
机制明确后,团队迅速探索靶向阻断该轴的治疗策略。鉴于阻断CGRP信号通路的药物(如CGRP单抗及小分子拮抗剂)已成功用于治疗偏头痛,团队聚焦于适合皮肤外用改造的小分子药物。2024年在中国获批上市的偏头痛口服药瑞美吉泮(Rimegepant)成为首选。
-
动物模型验证: 在白癜风小鼠模型中,瑞美吉泮显示出与现有药物(如鲁索替尼)相当的改善疾病表型的效果,且在抑制关键致病细胞——真皮cDC1扩增方面表现更优。
-
临床疗效确证: 团队成功开发出瑞美吉泮外用软膏剂型(0.1%),并开展了单盲临床试验(57例患者)。患者被分为三组,分别接受:
-
A组:单纯安慰剂或瑞美吉泮软膏。
-
B组:安慰剂或瑞美吉泮软膏 + 每周一次NB-UVB光疗。
-
C组:同一患者邻近两块白斑,分别使用安慰剂或瑞美吉泮软膏 + 光疗。
所有组别的结果一致显示,使用瑞美吉泮软膏能有效促进患者皮肤复色,显著提高白斑复色率,证实其治疗人类白癜风的临床价值。
-
这是第一个通过“老药新用”策略,成功实现神经调控作用在自身免疫性皮肤病中的临床验证。
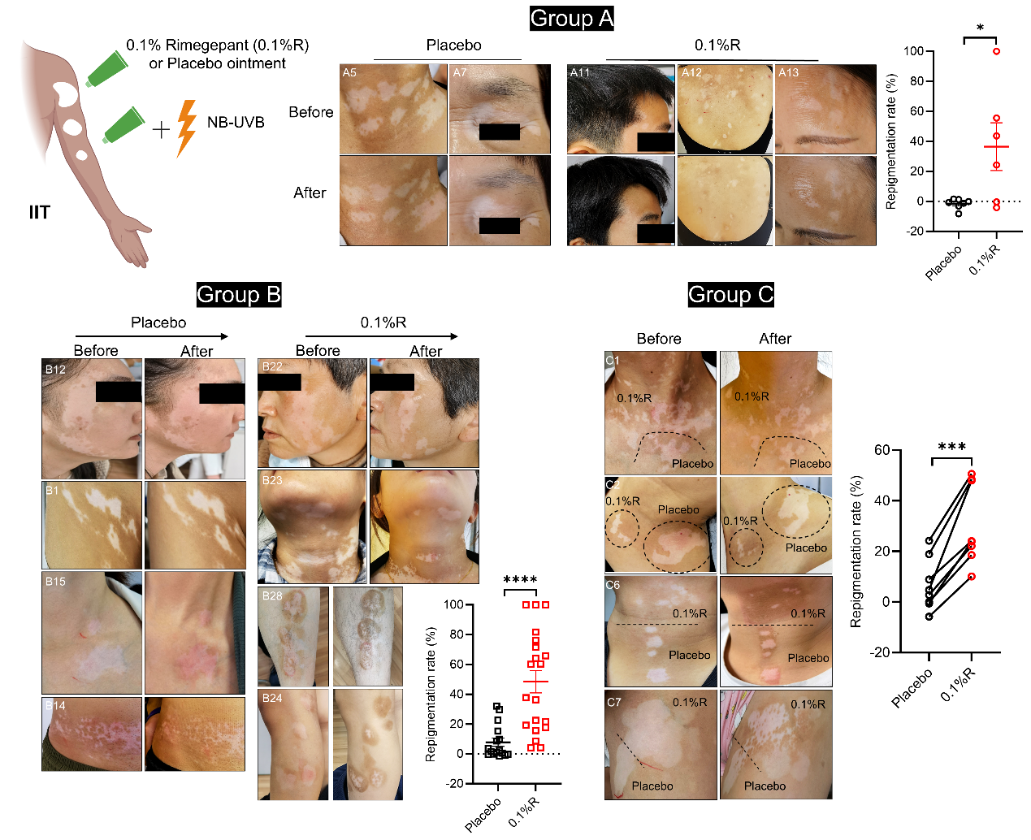
0.1%瑞美吉泮软膏显著改善患者的白癜风表型
白癜风1.1类创新药物CKBA软膏II期临床试验由杭州市第三人民医院皮肤病研究所所长、国内知名白癜风专家许爱娥教授担任主要研究者(Leading PI),是多中心、随机、双盲、平行、溶媒对照、剂量探索试验,旨在评估CKBA软膏在非节段型白癜风患者中的安全性和有效性。2023年7月:获批开展白癜风II期临床试验(通知书编号:2023LP01486);2024年10月:完成全国22个中心200例白癜风患者的入组;2025年5月:所有受试者已全部完成出组,目前正在进行数据清理和数据分析等工作;白癜风II期临床试验数据正式揭盲后拟向国家药审中心申请突破性疗法认定。
未来展望:多层次、多靶点的“白癜风战斗策略”
除瑞美吉泮的“老药新用”外,团队历时二十年潜心研发,从传统中药乳香活性成分中修饰、筛选得到具有完全自主知识产权的全新化合物实体CKBA。该“First-in-Class”1.1类候选新药已完成全球专利布局(覆盖中国、美国、日本、欧盟等),其外用软膏剂型同样旨在治疗白癜风及轻中度寻常型银屑病,标志着我国在皮肤免疫疾病原创药物研发领域取得重大突破。
这也提示我们未来治疗可以多点突破。一方面,充分发挥已有药物的潜力——如炔雌醇、鲁索替尼、瑞美吉泮等——经过配比优化,用于局部或系统治疗;另一方面,新靶点如神经调控信号、免疫细胞亚群甚至表观遗传层面,也等待更多科技助力。
此外,随着个体化医学的发展,将根据患者的免疫表型、神经纤维网密度、基因特征等,为每一位患者制定差异化的治疗方案,真正实现精准医学。在此基础上,研发多功能配合剂,结合光疗、药物和神经调节,或许能大幅提高疗效,降低复发率。
总结
白癜风作为一项典型的免疫-神经交叉调控疾病,传统治疗方式受限;但随着神经科学和免疫学的深度融合,我们第一次在临床层面验证了“感觉神经-免疫”轴的调控作用,为患者提供了全新的治疗思路。利用CGRP受体拮抗剂的持续开发和优化,有望成为白癜风治疗的标志性突破。
这项工作展现了“基础转化”结合的典范路径:从动物模型的分子机制创新,到药物改造、临床验证,再到未来的产业转化,构建了完整的“环路”。在此基础上,可以预见,神经免疫结合的治疗策略将驱动白癜风乃至其他免疫性疾病的未来。
梅斯编辑点评
这项研究不仅在机制上提供了全新视角,也在临床实践中实现了“老药新用”的突破,为白癜风的治疗打开了新的大门。未来,关于神经-免疫轴的调控是否能帮助我们治疗其他自身免疫疾病?不同个体间神经纤维和免疫细胞的空间关系是否会影响治疗效果?这些都值得我们继续探讨。科学的力量,总是在不断创新中推动人类健康的边界,期待更多类似的联结多学科、突破传统的研究,为患者带来实实在在的福祉。
原始出处:
https://www.cell.com/immunity/abstract/S1074-7613(25)00239-0
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)