首页 > 医疗资讯/ 正文
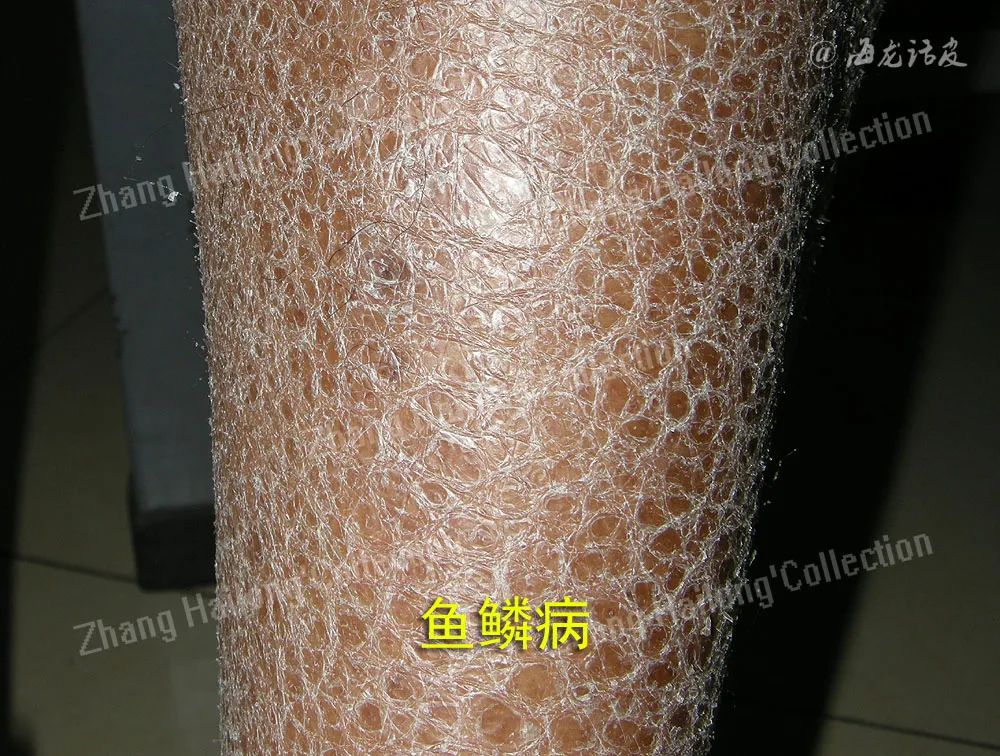
先天性鱼鳞病(congenital ichthyosis,CI)是一种皮肤角化障碍性遗传病,好发于儿童。转谷氨酰胺酶-1(transglutaminase-1,TGM1)等基因负责脂质屏障 的形成和正常功能,角质层(stratum corneum,SC)及其脂质组分是保障皮肤屏障功能的关键,对于维持皮肤健康意义重大,基因突变、脂质组成的改变或由于刺激、损伤和炎性过程而导致鱼鳞病。主要表现为皮肤干燥、脱屑和鱼鳞状的皮损样。增加了患者的心理痛苦和经济负担,严重影响患者生活质量,该病的发病机制复杂,治疗难度较大。近年来,靶向药物、生物制剂、基因治疗的治疗手段的出现为其提供了新希望。

一 维A酸类药物治疗
1、阿达帕林:
阿达帕林是一种第三代局部用类视黄醇,可选择性结合视黄酸受体-β(retinoic acid receptor-β,RAR-β)和视黄酸受体-γ(retinoic acid receptor-γ,RAR-γ),调节细胞角化和抗炎过程,它在外用治疗表皮松解性鱼鳞病(epidermolytic ichthyosis,EI)病例中显示出良好效果。目前阿达帕林具有减少角质形成和细胞黏附性的作用。0.1%的阿达帕林凝胶制剂引起的刺激性低于他扎罗汀和维A酸,可能是由于其与核RAR-β和RAR-γ受体的选择性结合的结果。有研究报道了外用阿达帕林治疗EI,结果显示可抑制角质形成细胞的增殖,减轻面部病变并改善面部皮肤外观。因此,该药对于患有表皮松解性鱼鳞病的患者是一种选择。

2、他扎罗汀:
他扎罗汀是一种具有选择性RAR-β和RAR-γ结合活性的类视黄醇,它对角质形成细胞具有强烈的抗增殖作用并改变其分化和黏附,同时使副作用最小化,他扎罗汀凝胶在外用治疗X-连锁隐性遗传鱼鳞病(recessive X-linked ichthyosis,RX-LI)、板层状鱼鳞病(lamellar ichthyosis,LI)和浅表表皮松解性鱼鳞病(superficial epidermolytic ichthyosis,SEI)中显示出确切疗效。已经证实他扎罗汀可调节表皮细胞分化,缓解角质层过厚。有研究显示他扎罗汀在应用于鱼鳞病患者一个月后,显示出最小的全身吸收。
3、维A酸:
全身性维A酸[0.5~1mg/(kg·d)]通过抑制表皮增殖,促进角质形成细胞分化,从而改善角化过度,它在口服治疗EI(先天性鱼鳞病样红皮病)和LI(火棉胶婴儿)具有显著疗效。目前已证实维A酸可改善毛囊皮质腺导管角化、抗炎。在其中曲法罗汀作为第四代维A酸类药物,对RAR-γ具有选择性作用,已被测试用于治疗先天性鱼鳞病,并证明其安全性和耐受性良好,因此美国食品药监局(Food and Drug Administration,FDA)于2014年将其列为治疗先天性鱼鳞病的药物。
4、TMB-001:
TMB-001是一种新型的局部外用异维A酸软膏制剂,其使用专利的聚乙二醇(polyethy-lene glycol,PEG)技术异维A酸递送系统来治疗CI, 耐受良好且有效,没有全身性异维A酸/维A酸暴露的药代动力学证据,可能是CI患者未来口服类维生素A的有前景的替代品,它正在开发用于RXLI或LI的治疗。
5、阿利维A酸:
阿利维A酸也是欧洲药品管理局(European Medicines Agency,EMA)批准用于治疗CI的唯一一种类视黄醇,其功效和治疗彻底改变了许多患有严重CI的患者的生活,它在口服治疗丑角样鱼鳞病(harlequin ichthyosis,HI)和 LI疗效突出,阿利维A的疗效已在一些初步研究和大量病例报道中得到证实。20mg/d或30mg/d的剂量可有效减少红斑,去除鳞屑和使角化过度变薄,并且在其他方面耐受性良好。还可改善少汗症、毛发再生、改善眼睑外翻和眼睑下垂,但其主要的不良反应是致畸性,因此女性必须谨慎进行妊娠预防。
6、利阿唑:
类维生素A治疗LI具有增加皮肤炎症过程相关的副作用,会导致瘙痒并对上皮产生负面影响,因此使用受限。然而,利阿唑作为一种口服维A酸代谢阻断剂(RAMBA),其通过细胞色素(cyco-pigment,CYP)P450抑制4-羟化酶,从而防止视黄酸分解代谢,并在体内表现出类维生素A节省作用,可以显著改善RXLI、LI和EI患者的角化过度。在存在低剂量视黄酸或全反式视黄醇的情况下,利阿唑可以放大低剂量类维生素A的有效性,其方式与较高剂量的类维生素A相同。
二 靶向治疗
1、IL-4抑制剂:
度普利尤单抗是一种抑制IL-4信号传导的单克隆抗体,IL-4是Th2相关免疫的关键介质,可导致许多炎症性皮肤病,度普利尤单抗皮下注射可改善与特应性皮炎和哮喘相关的LI。有病例显示LI患者最初开始接受10mg阿维A治疗3个月,由于特应性皮炎恶化而停止,随后使用10mg甲氨蝶呤4个月治疗特应性皮炎,结果改善甚微,由于严重的胃肠道不适而停药,随后接受300mg度普利尤单抗,每月两次治疗,3个月后LI、特应性皮炎和哮喘临床显著改善。
2、IL-23抑制剂:
由于鱼鳞病细胞因子谱与银屑病相似,IL-23是一种参与炎症和免疫反应的细胞因 子,靶向IL-23瑞莎珠单抗和古塞奇单抗皮下注射是治疗鱼鳞病的合理选择,通过抑制 IL-23与其受体结合,阻断了IL-23依赖的信号转导和促炎性因子的释放。虽然度普利尤单抗单药治疗可减轻瘙痒,但不足以改善患者的鱼鳞病变,转换为古塞奇尤单抗与度普利尤单抗联合治疗后,鱼鳞病显著改善,耐受性良好。这种显著的改善在联合治疗10周后观察到,并且在80周内趋于稳定,无副作用。因此,使用度普利尤单抗/古塞奇尤单抗联合治疗可快速改善红皮病性鱼鳞病, 这证明了联合用药是一种有效、安全、耐受性良好的选择。
3、IL-17抑制剂:
IL-17A能够诱导角质形成细胞的过度增殖、促进炎症细胞的趋化以及释放更多的炎症介质,从而导致皮肤出现红斑、鳞屑等症状。苏金单抗是靶向IL-17A细胞因子的重组人单克隆抗体, 皮下注射作用于人体,通过精准地结合IL-17A,阻断其生物活性,是一种IL-17A抑制剂,在CI患者中,已证实Th17/IL-17在皮肤和血清中具有IL-17显性特征。其中内瑟顿综合征(netherton syndrome,NS)患者表现出最高的IL-17和IL-22通路基因的诱导。鱼鳞病面积和严重程度指数-红斑评分(IASI-E)显示与IL-17A水平和经表皮水分损失(transepidermal water loss,TEWL)显著相关,并发现皮肤和血液样本中的IL-17和TNF-α水平升高。靶向IL-17A的另一种生物治疗剂是依奇珠单抗,是一种人源化抗IL-17A/F抗体,比苏金单抗对IL-17A亲和力更高。Barbieux等报道三例NS患者,两例患者具有卷曲线状鱼鳞病(NS-ILC)表型,一例患者具有鳞状红皮病(NS-SE)表型,他们都具有增强的IL-17相关细胞因子水平,用依奇珠单抗治疗6个月后IASI-S、皮肤生活质量指数(dermatology life quality index,DLQI)和瘙痒评分显著 降低约50%。表明依奇珠单抗在旋线型鱼鳞病(ichthyosis linearis circumflexa,ILC)患者的诱导期的治疗 耐受性良好,且改善皮肤疗效显著,这也支持了IL-17抑制剂在CI中的应用。
4、IL-18抑制剂:
有研究对血清IL-18水平与鱼鳞病评分系统(ichthyosis scoring system,ISS)进行比较,通过ISS将EI组分为:轻度(ISS 0~2.0)、中度(ISS 2.0~5.0)和重度(ISS 5.0~8.0)三个亚组,并在亚组之间比较IL-18水平,显示重度亚组的IL-18水平显著高于轻度组P<0.05,提示IL-18水平可能与EI具有强相关性。随后对ISS的每个解剖部位处的鳞屑或红斑的组合评分分别计算为ISS量表(ISS-S)或ISS红斑(ISS-E),并且检查IL-18水平与ISS-S或ISS-E之间的相关性,得出两者之间确有显著相关性,但ISS-E的相关性更强,表明IL-18可能与EI中红斑或红皮病的严重程度相关。
5、小分子JAK抑制剂:
JAK-STAT信号通路与炎症和自身免疫性疾病的发病机制有关。有研究显示使用小分子JAK抑制剂靶向治疗特应性皮炎、银屑病、红斑狼疮等炎症性皮肤病。有研究揭示了与HI发病相关的炎症通路,即ABCA12功能缺陷可通过上调IFN-γ的表达,从而过度激活JAK/STAT通路,使下游靶分子NOS2的表达增强,诱发HI表皮炎症,因此小分子JAK抑制剂或许会成为HI的针对性治疗靶点。
三 基因疗法
1、逆转录病毒:
可以有效感染表皮祖细胞,并为皮肤更新的几个周期提供治疗基因在皮肤中的稳定表达,被认为是用于皮肤疾病的基因递送的工具,鱼鳞病患者的角质形成细胞可以使用逆转录病毒成功地修饰。有研究表明,在用编码TGM1基因的逆转录病毒转导后,转谷氨酰胺酶-1(transglutaminase1,TGase-1)的表达和活性在体外LI患者的突变角质形成细胞中恢复。

2、疱疹病毒:
基于单纯疱疹病毒1型(HSV-1)编码TGM1基因的载体已被提出用于由TGM1基因突变引起的鱼鳞病(常染色体隐形先天性鱼鳞病)基因治疗的一种安全有效的方法。HSV-1是用于治疗鱼鳞病的有吸引力的载体,因为它具有亲上皮性并且比其他病毒载体可以更有效地穿透皮肤角质形成细胞。HSV-1载体是安全的,因为其遗传信息不整合到宿主细胞的DNA中,这意味着病毒不引起插入诱变。有研究表明,该载体有效地感染TGM1缺陷的人皮肤细胞,在体外恢复TGase-1酶活性,并且当在体内局部施用到免疫活性BALB/c小鼠中时,还显著增加TGase-1的表达而没有毒性。还描述了载体没有显示出毒性和免疫原性,即使每周注射到动物的表皮中,并且不会从注射部位扩散到其他区域。
四 新型疗法
1、氨基水杨酸疗法:
5-氨基水杨酸(5-aminosalicylic acid,5-ASA)是一种口服抗炎药物,该药可对抗神经酰胺诱导的炎症,神经酰胺是表皮脂质屏障的主要成分,并且是HI表皮中描述的最失调的脂质种类之一,因此5-ASA治疗HI具有确切疗效。有研究发现在胚胎HI表皮的器官培养物中,5-ASA显著改善角质形成细胞分化。并在建立的诱导型HI小鼠模型中测试了5-ASA、阿维A和相关化合物4-氨基水杨酸(4-aminosallic acid,4-ASA)和阿司匹林的疗效。结果表明,与5-ASA相比,4-ASA表现出皮肤表型的改善更明显,并且没有在应用阿维A或阿司匹林后的副作用,同时还纠正了许多基因的错误表达,被认为有助于屏障功能的恢复,并与其他类型的鱼鳞病有关。因此将4-ASA确定为适合用于治疗HI的候选药物,具体应用有待后续研究和临床更多的病例支持。
2、酶替代疗法:
酶替代疗法(enzyme replacement therapy,ERT)即替换缺陷的结构蛋白或酶,CI的病理表现是表皮正常角质化所必需的蛋白质的部分或完全缺失,因此ERT是治疗各种类型的CI的有效方法。在动物模型中,LI的局部ERT可恢复TGase-1活性并纠正TGase-1缺陷皮肤移植物的结构。有研究在LI动物模型中证明了使用脂质体递送重组蛋白以恢复TGase-1活性并再生皮肤的有效技术。负载有TGase-1的脂质体有效地恢复了表皮上分层中的TGase-1活性,增加了表皮的完整性,并改善了其屏障功能。有学者研究了从TGM1突变的CI患者的成纤维细胞和角质形成细胞获得的全层皮肤等效物,用TGase-1酶处理所得皮肤等同物,使用热敏纳米凝胶(tNG)进行蛋白质递送。在用负载有TGase-1的tNG处理后,观察到皮肤等同物的渗透性显著降低50 倍,表明屏障功能有所改善。
3、纳米递送疗法:
糖皮质激素由于吸收的皮肤表面积较大,通过SC的渗透有限,导致给药频率高,这可能导致局部不良反应和患者依从性降低。此外,由于不良反应,如免疫抑制、皮肤刺激或妊娠纹,糖皮质激素不应长期或高剂量应用于皮肤敏感区域。但含有纳米载体的局部制剂可以有效改善皮肤渗透和减少,同时降低糖皮质激素的相关副作用,提高局部治疗的安全性和有效性。因此将糖皮质激素包封到纳米递送系统中被预测为一种有潜力的治疗CI的策略,其提供的生物相容性和生物利用度,允许局部施用,改善糖皮质激素的风险—效益比,并最终提供更有效的治疗。此外,含神经酰胺(ceramides,CER)的纳米载体可以为这些关键脂质提供更有效和持续的释放作用,以维持和/或恢复皮肤屏障稳态。另外可以通过调节纳米载体的物理化学性质,针对皮肤病患者进行个体性差异治疗。
五 小结
CI作为一种难治性疾病,对患者的生活质量影响较大,目前尚无标准的治疗方案,除了应用传统的保湿剂、润肤剂、维生素D以外,维A酸类药物(阿达帕林、他扎罗汀、曲法罗汀、TMB-001、维A酸、阿利维A酸、利阿唑),以及靶向药物(IL-4、IL-17、IL-18、IL-23的单克隆抗体,小分子JAK抑制剂),新型的逆转录病毒和疱疹病毒的基因治疗,氨基水杨酸、酶代替疗法和糖皮质激素纳米递送疗法的研究也为CI的治疗开拓了新前景,但是由于实验研究和临床应用的病例相对有限,因此其用法用量、疗效性和安全性仍需进一步的研究去证实。
参考文献:
1.张潇亚,许琳琳,李廷保.先天性鱼鳞病的治疗进展[J].中国麻风皮肤病杂志,2025,5(41):384-388.
2. 张民阔,宋智敏,孙青.维A酸类药物在皮肤科中的应用[J].中国麻风皮肤病杂志,2022,38(9):653-658.
3.其他文献略。
猜你喜欢
- 让老年人更有获得感专家详解医养结合领域指导意见
- 美学设计师陈方芳:美的艺术从内而外
- 一文带你认识胰岛素抵抗及诊断方法
- 乌豆根的功效与作用及禁忌
- Adv Sci:刘佳利/陈娟/丁德强合作阐明PARN维持RNA稳定性以调节胰腺β细胞中的胰岛素成熟和GSIS
- 化疗药物溶媒选择一表总结:这 5 种常用药 90% 医生都配错了!
- 北航樊瑜波、刘海峰团队/军科院郭希民团队ACS Nano:工程化牙髓间充质干细胞源细胞外囊泡复合多功能水凝胶促进骨再生
- 2022年04月03日每日养生小知识健康简报,星期日!健康是一种生活态度!
- 基于亚组分化作为帕金森病辅助治疗的中草药治疗
- 湖北襄阳开展“药店乱象” 整治 29家医保定点药店被处罚
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)