首页 > 医疗资讯/ 正文
甲状腺功能减退可导致多器官功能障碍,其中心脏受累是甲状腺功能减退导致多器官受累的重要环节。然而,甲状腺功能减退导致心力衰竭的病理机制尚未完全阐明。因此,亟需详细阐明甲状腺功能减退导致心力衰竭的分子机制,并研发能够靶向改善甲状腺功能减退患者心功能的药物。
北京大学第三医院唐熠达教授团队在甲状腺功能减退导致心力衰竭的分子机制上取得重要进展,2025年5月13日,美国心脏协会(AHA)主办的国际权威期刊Circulation杂志发表了题为“Dusp14-Mediated Dephosphorylation of MLKL Protects Against Cardiomyocyte Necroptosis in Hypothyroidism-Induced Heart Failure”的研究论文。该研究发现,坏死性凋亡在甲状腺功能减退引起的心力衰竭中起着关键作用,Dusp14的缺失会引发坏死性凋亡并加重甲状腺功能减退引起的心力衰竭。小分子化合物P077-0472增强Dusp14的去磷酸化活性,以抑制坏死性凋亡。该研究提示,Dusp14可能成为治疗甲状腺功能减退引起心力衰竭的新靶点。对于甲状腺功能减退导致的心力衰竭患者,靶向抑制心肌坏死性凋亡可能是新型的治疗策略。

首先,团队为阐明甲减导致心衰的可能机制,采用Malacards人类疾病基因数据库分析与丙硫氧嘧啶诱导的小鼠甲减心衰模型结合。通过生物信息学分析提示甲减患者坏死性凋亡可能激活,并进一步采用动物实验证实这一发现。甲减小鼠出现相应心衰表现,包括射血分数下降、BNP升高等,收集小鼠心脏进行转录组分析,并进行KEGG富集同样提示坏死性凋亡通路明显激活。结合相应动物实验进一步成功验证坏死性凋亡在甲减小鼠中的重要作用。
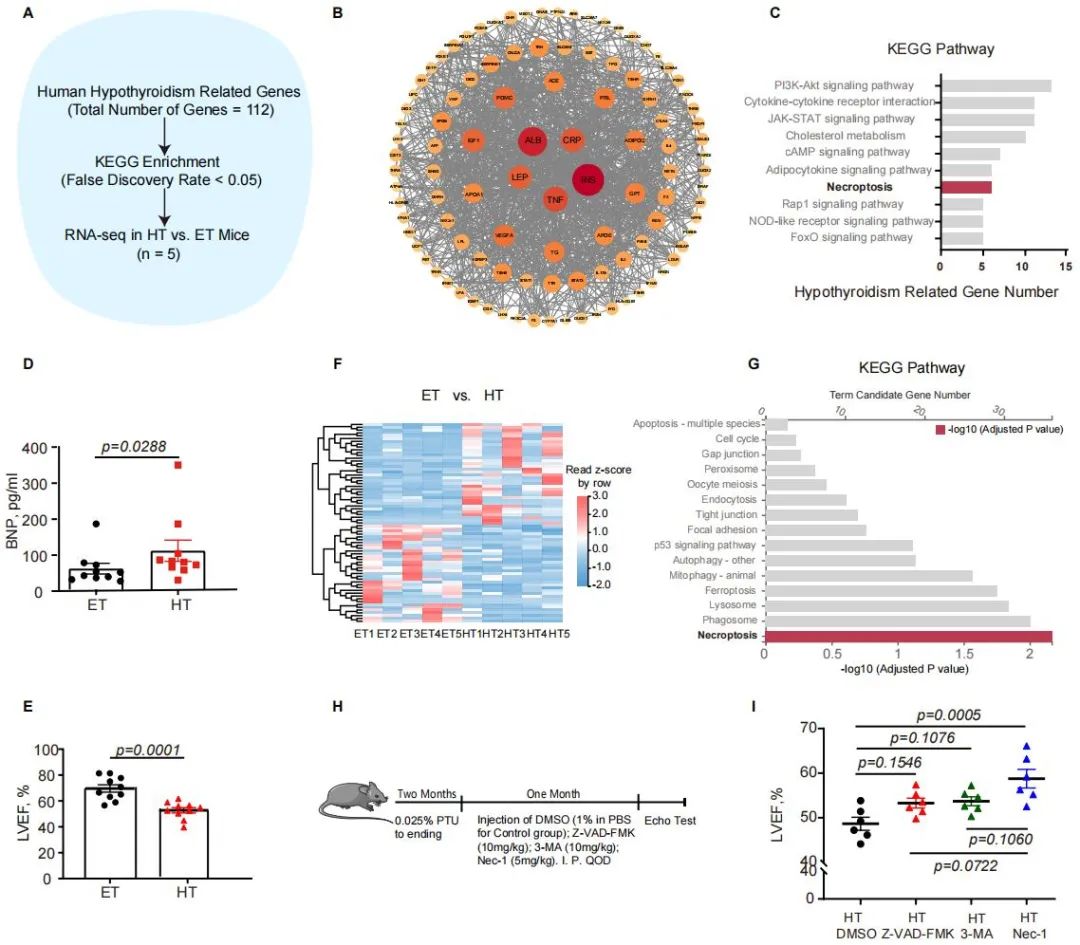
图1. 甲状腺功能减退患者和小鼠心肌坏死性凋亡上调
随后,该研究通过甲减/正常组小鼠心脏RNA测序鉴定出差异表达基因Dusp14 (双特异性磷酸酶14)。QPCR和WB检测提示,甲减小鼠心肌Dusp14 mRNA和蛋白水平表达均明显下调。而正常小鼠的心肌单细胞转录组证实Dusp14主要定位于心肌细胞,免疫荧光显示甲减组小鼠心肌细胞Dusp14荧光强度下降。同时相应临床样本的分析发现,甲减人群的Dusp14表达同样明显降低,且同患者的NYHA心功能分级呈密切相关性。这些证据提示Dusp14可能通过调控坏死性凋亡通路影响甲减性心衰进程,但其具体分子机制及治疗潜力仍需深入解析。
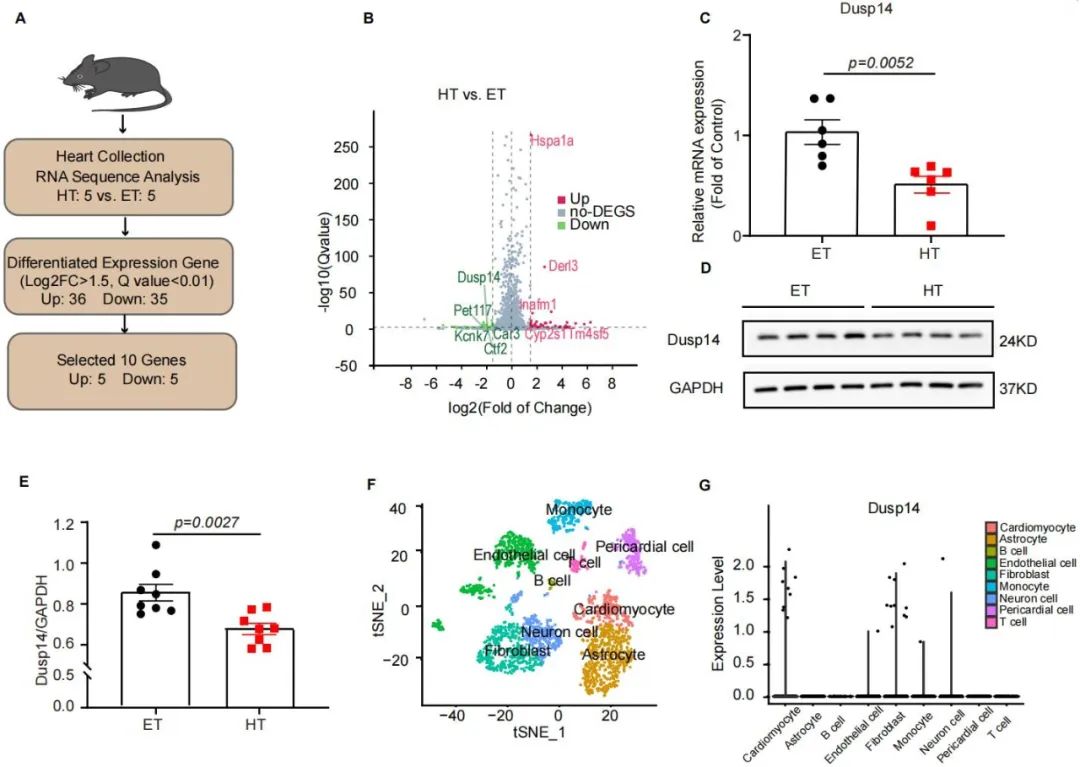
图2. Dusp14在甲减小鼠中表达下降
研究者进一步通过体内和体外实验验证Dusp14调控心肌细胞坏死性凋亡,发现Dusp14可通过直接调控MLKL的磷酸化发挥作用,通过在乳小鼠心肌细胞(NMCM)敲低和过表达Dusp14发现,Dusp14可抑制H2O2诱导的NMCM坏死性凋亡。同时,基于DUSP14KO小鼠以及AAV9-cTnT-Dusp14介导的DUSP14心肌特异性过表达小鼠构建甲减心衰模型,发现Dusp14可显著改善小鼠心力衰竭。
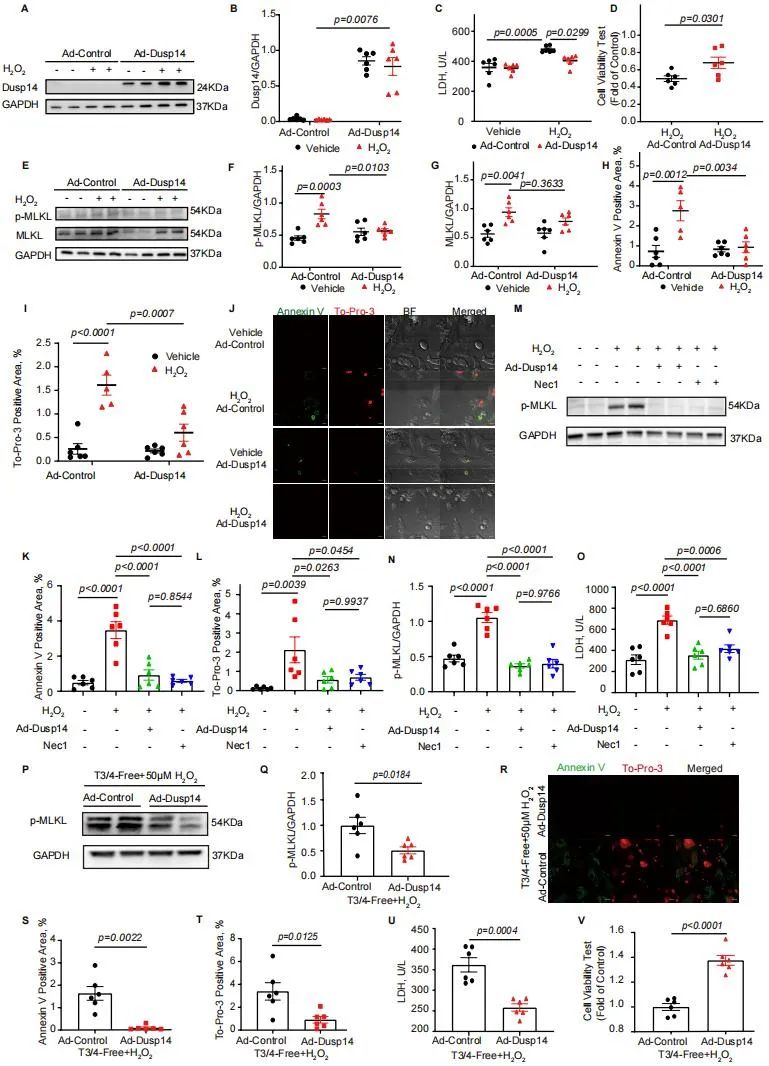
图3. Dusp14抑制乳小鼠心肌细胞坏死性凋亡
最后,研究者进一步通过分子对接及虚拟筛选技术,筛选出可调控Dusp14去磷酸化活性的小分子化合物P077-0472,并在体外证实其可抑制小鼠心肌细胞的坏死性凋亡,改善心肌细胞活性。
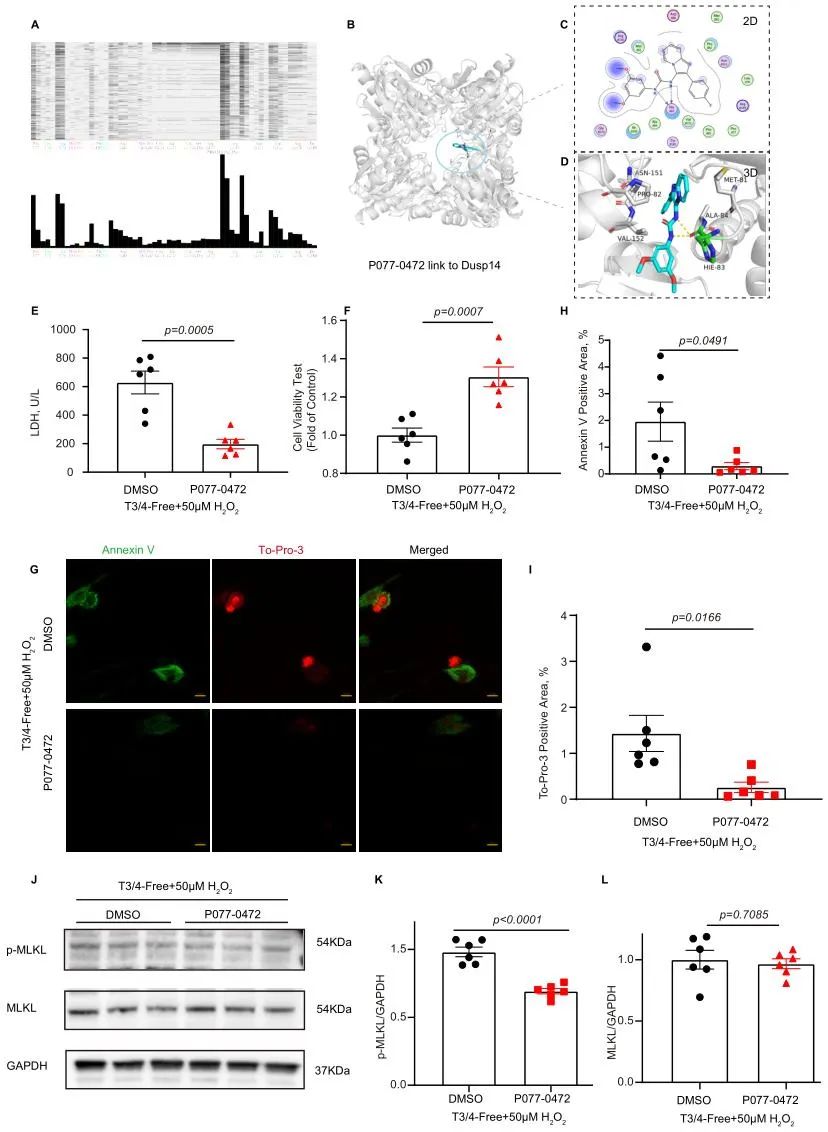
图4. P077-0472激活Dusp14去磷酸化功能抑制心肌细胞坏死性凋亡
综上,该研究揭示Dusp14通过直接去磷酸化MLKL(不依赖RIP1/RIP3通路)抑制心肌细胞坏死性凋亡,在甲减导致的心力衰竭中发挥关键保护作用。甲减状态下心脏Dusp14表达下调是心衰发生的重要分子基础。Dusp14不仅可作为甲减导致心衰的新型生物标志物与治疗靶点,其小分子激活剂P077-0472的发现更为临床干预提供了新的方向。该发现首次阐明Dusp14-MLKL轴在坏死性凋亡中的独立调控机制,为靶向细胞死亡通路治疗甲减性心脏病提供了新方向。
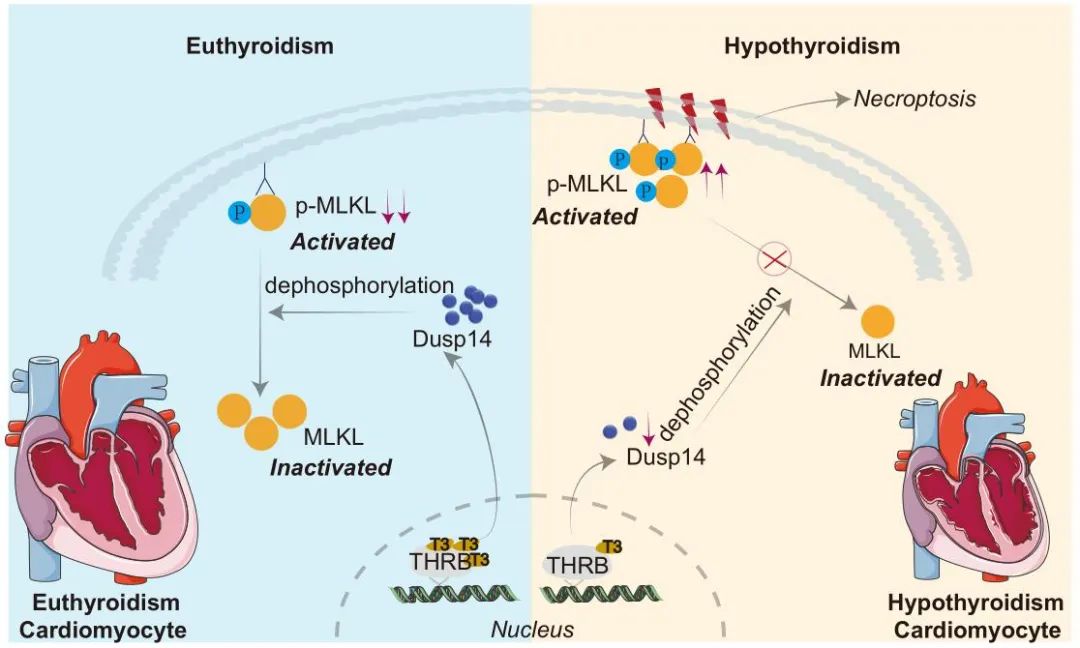
图5. Dusp14介导的MLKL去磷酸化抑制心肌坏死性凋亡改善甲减导致心力衰竭
北京大学第三医院唐熠达教授为该文章的通讯作者,北京大学第三医院郑一天博士为文章的第一作者。此外,该研究得到了北京大学第三医院张幼怡教授、肖晗教授以及北京大学张岩教授等专家的大力支持。
论文链接:
https://doi.org/10.1161/CIRCULATIONAHA.125.074353
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)