首页 > 医疗资讯/ 正文
PTCL
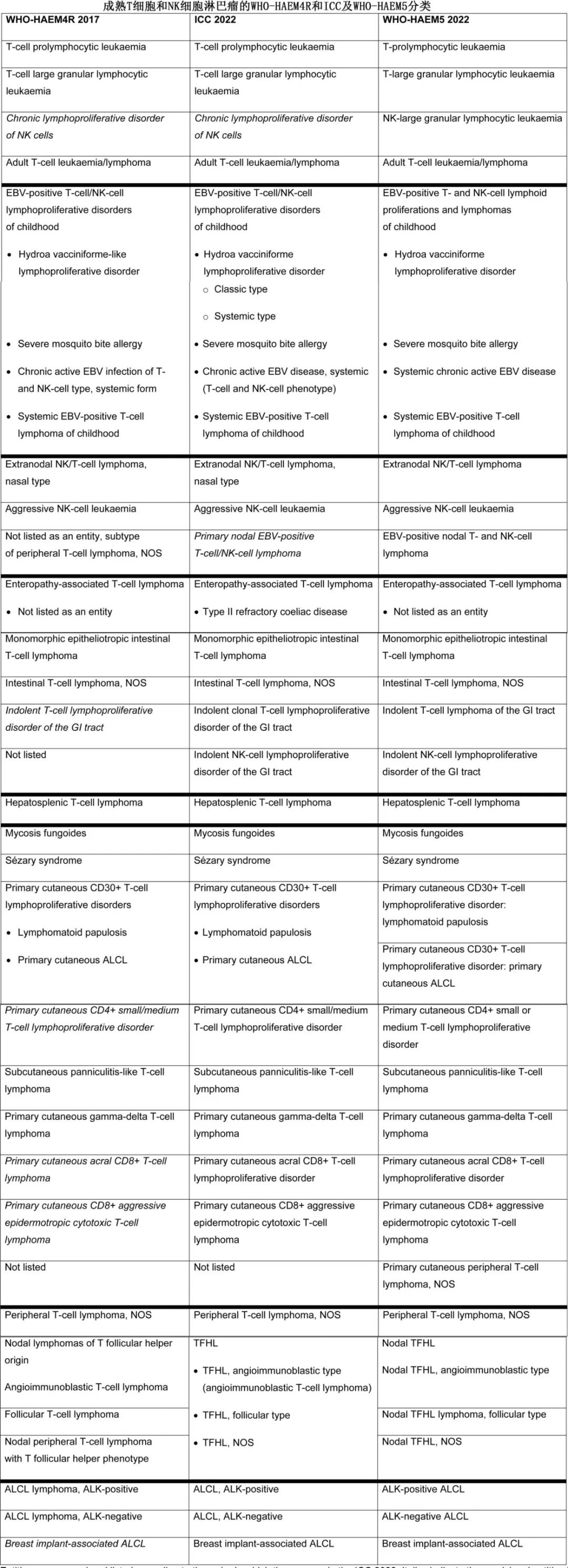
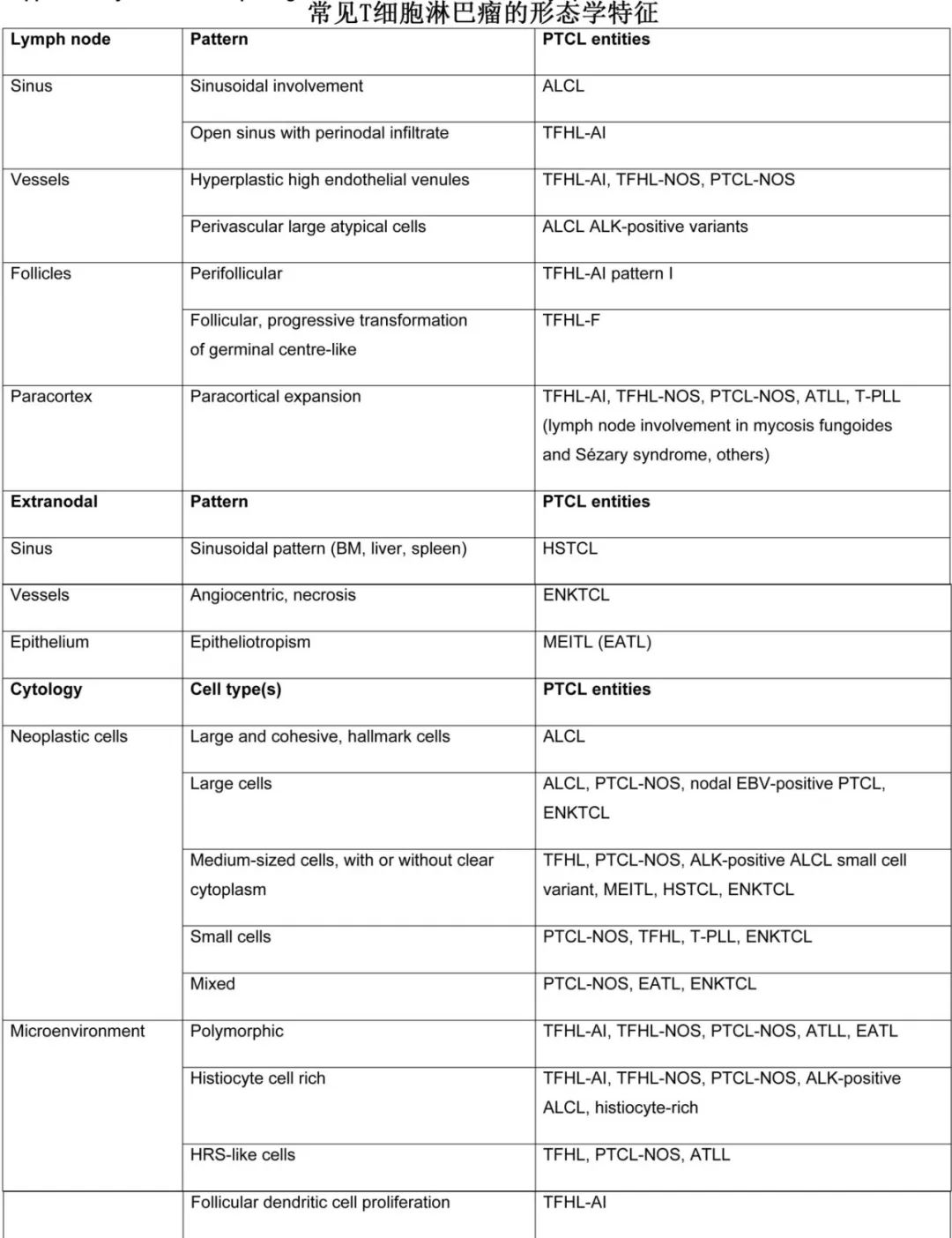
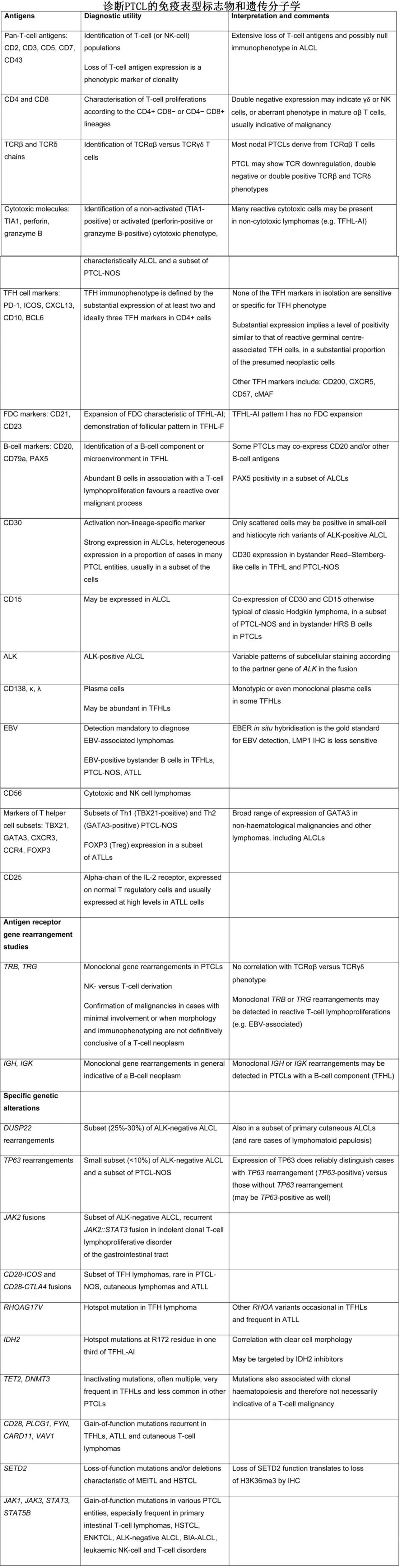
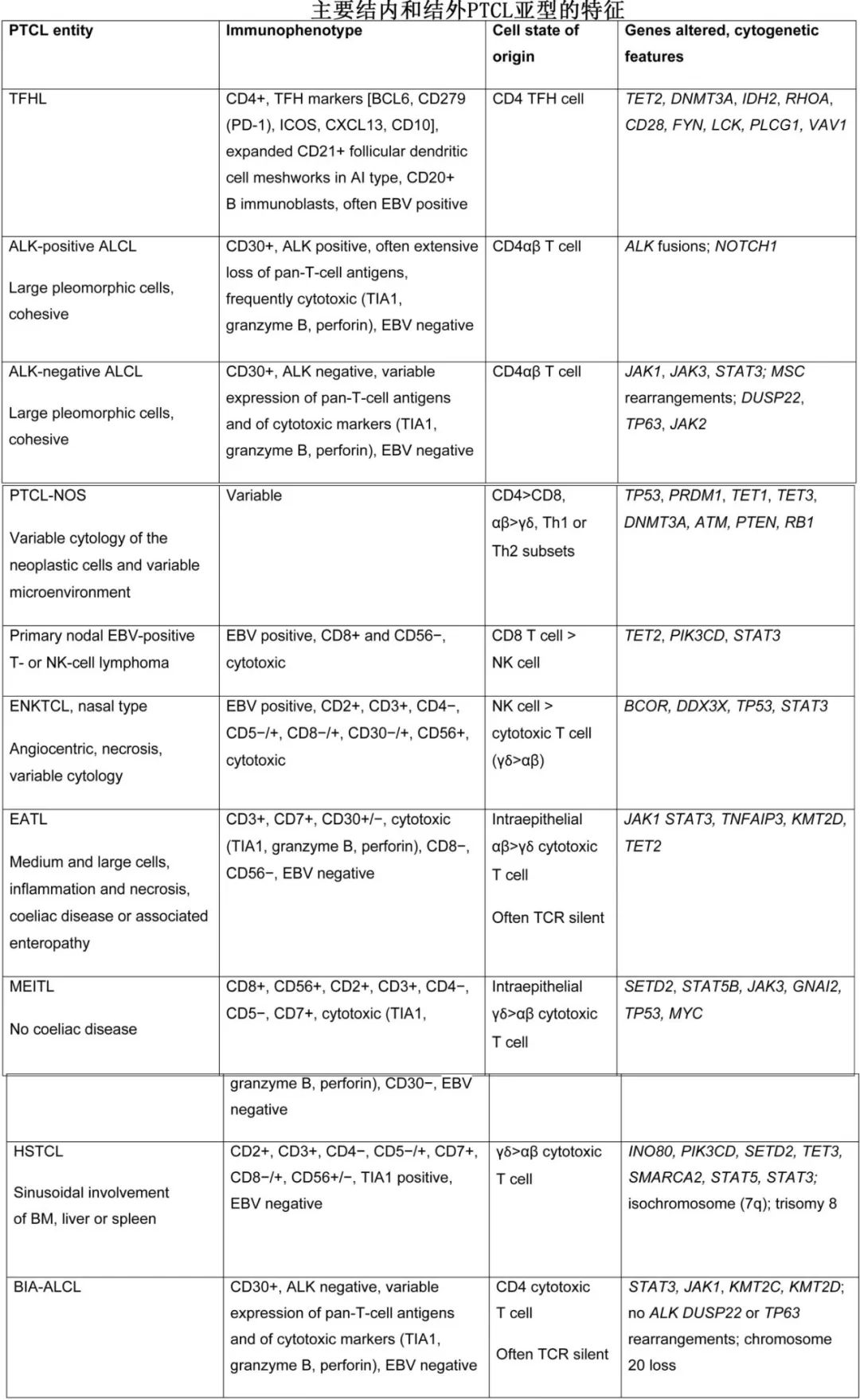
T 细胞淋巴瘤是一个通用术语,含T 细胞和NK细胞系免疫细胞的恶性肿瘤,包括不成熟 T 细胞的肿瘤(即 T 淋巴母细胞淋巴瘤/白血病)及成熟 T 和 NK 细胞的恶性肿瘤,后者通常称为“外周”或“成熟”T细胞淋巴瘤 (PTCL)。2022年ICC和WHO分类(第5版)整合了血液学、免疫学、病理学和遗传学最新信息,分为超过30种T/NK 细胞源性肿瘤(文末多个表格汇总了ICC和WHO的具体分型、常见T细胞淋巴瘤的形态学特征、免疫表型和分子学、结内和结外PTCL的特征)。
《Annals of Oncology》近日发表了PTCL的ESMO-EHA重磅指南,主要推荐整理如下。

诊断、病理学与分子生物学
临床病理学相关性应作为诊断的主要手段,并结合影像学结果、症状和实验室信息 [III,A]。
PTCL 的诊断应尽可能依赖于手术切除或切口活检 [II,A]。
应根据形态学、异常 T 细胞表型和是否存在致病性突变、病毒感染(EBV或HTLV-1)或 TCR 克隆性进行诊断 [II,A]。
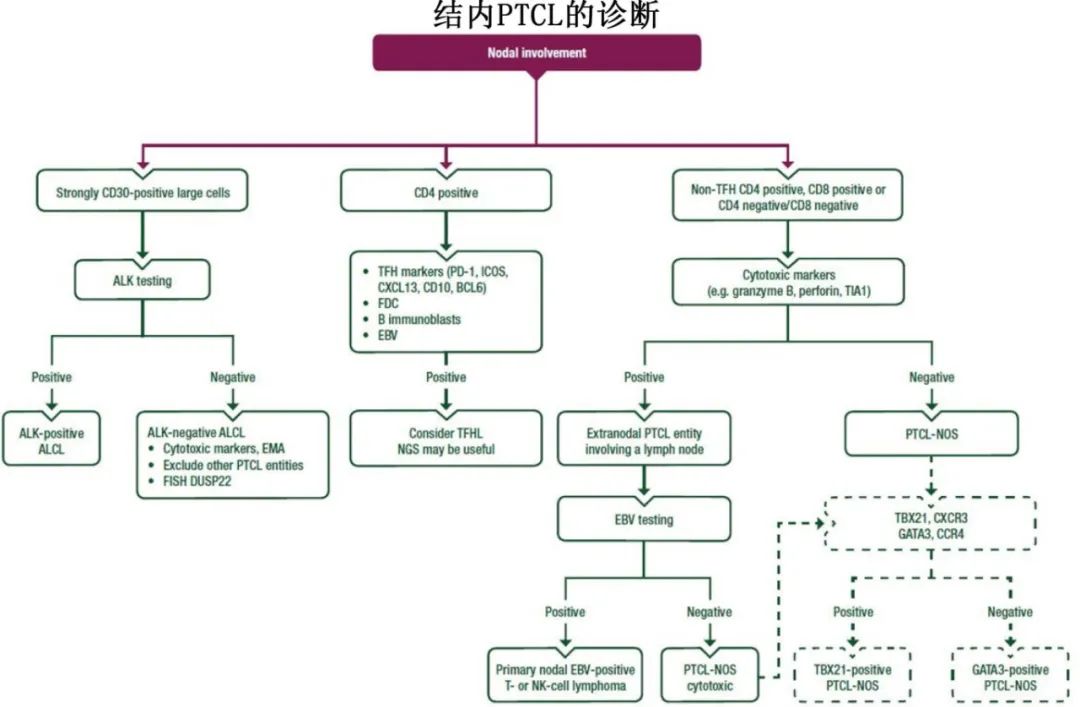
分期与风险评估
所有患者的管理应由 MDT 讨论,包括血液病理学家(包括病理学、细胞学和分子生物学专家)、诊断影像学专家、血液肿瘤学家和具有 PTCL 特定经验的放疗师 [I,A]。
如果可用,诊断、中期(可选)和治疗结束(EOT)时的 PET-CT 可视为所有结内和结外(非白血病)PTCL的首选影像学模式 [I,B]。如果 PET-CT 不可用,可使用诊断性CT [III,C],但在某些情况下 CT 检测结外疾病可能不充分。
在所有情况下,建议进行 BM 活检以进行准确分期,包括病毒表达的检查 [I,A]。
应在部分亚型中进行额外的检测,例如评估外周血细胞的免疫表型(例如原发性白血病实体的流式细胞术)和测量病毒载量(例如 ENKTCL 中的EBV DNA)[II,A]。
建议在复发或进展时进行再活检 [I,A]。
一线治疗
患者应尽可能入组临床试验 [II,A]。
PTCL-非特指型(PTCL-NOS)和滤泡性辅助T细胞淋巴瘤(TFHL)
CHOP或CHOP样化疗(例如CHOEP)可作为一线治疗推荐 [II, B]。
对于局限期、非大包括且治疗前风险特征良好的患者,可考虑缩短化疗疗程(例如3到4个周期的CHOP或CHOEP)[IV, B]。
对于局限期且在CHOP或CHOP样化疗后缓解的患者,可以考虑进行巩固性ISRT(例如15到20次分割的30-40Gy) [IV, B]。
对于高危局限期或进展期且缓解的患者,可以考虑进行巩固性自体造血干细胞移植 (auto-HSCT)[III, B]。
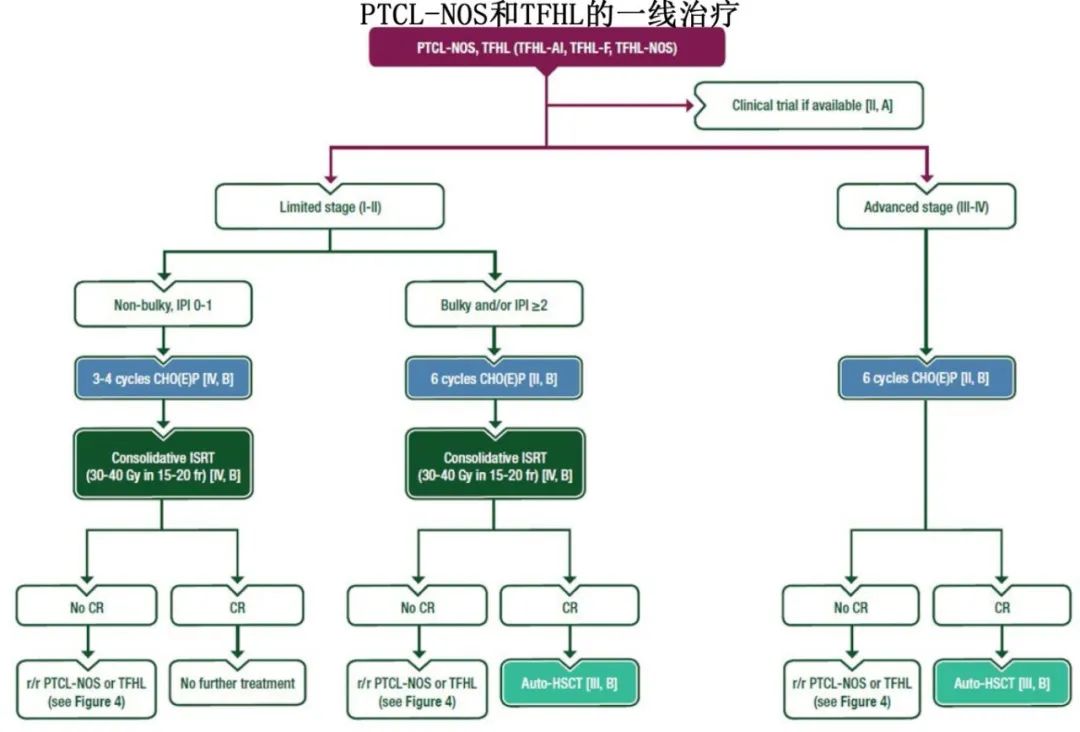
系统性间变性大细胞淋巴瘤(ALCL)
对于局限期、非大包块ALK阳性或ALK阴性疾病且治疗前风险特征良好(IPI 0-1)的患者,可以考虑缩短化疗疗程(例如3到4个周期的BV-CHP或CHOEP) [III, B]。
对于所有其他适合化疗患者(即ALK阴性和ALK阳性患者),推荐6个周期的BV-CHP [I, A]。也可以考虑6个周期的CHO(E)P [III, B]。
对于局限期ALCL,可以考虑进行巩固性受累部位放疗(ISRT)(例如15到20次分割的30-40Gy) [IV, B]。
对于首次完全缓解(CR)且对化疗敏感的ALK阴性ALCL患者,如果适合造血干细胞移植(HSCT),可以考虑进行巩固性auto-HSCT [II, B]。
一般来说,对于首次CR的ALK阳性ALCL患者,不推荐auto-HSCT [III, D]。但对于有高危特征(IPI≥2,大包块)且在3个周期化疗后未达到CR的患者,可以考虑 [III, B]。
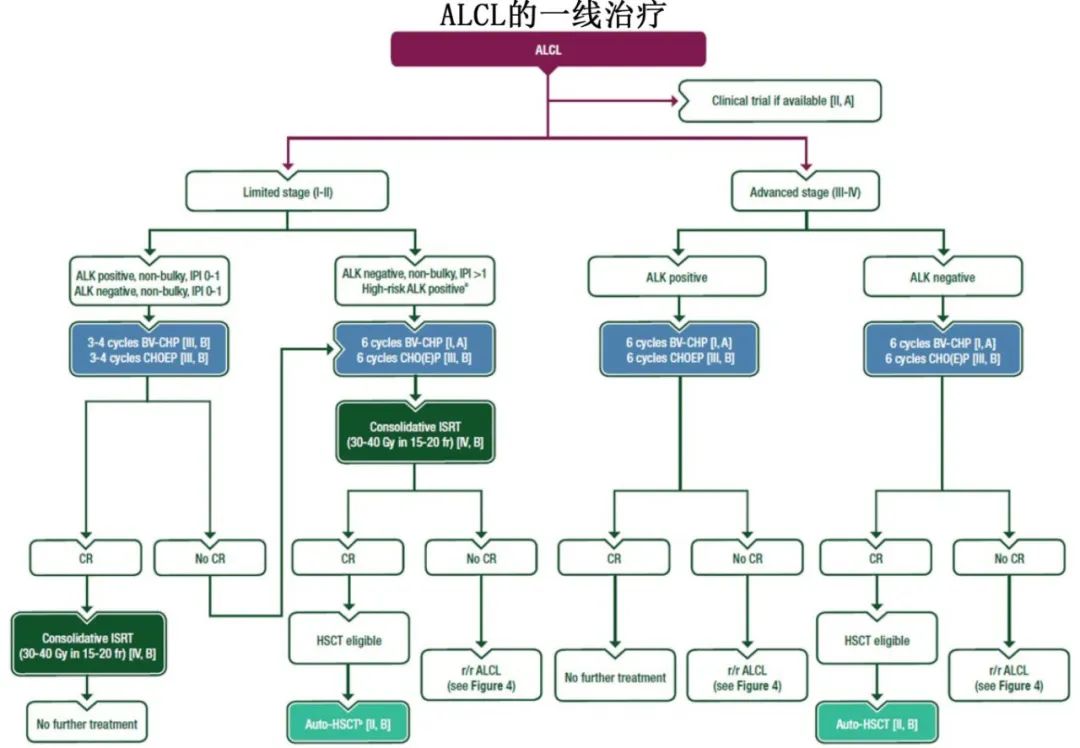
乳腺假体相关间变大细胞淋巴瘤(BIA-ALCL)
推荐采用多学科方法进行诊断评估、分期和治疗计划 [III, A]。
对于没有进一步疾病扩散迹象的患者,建议进行全包膜切除,移除乳房植入物并切除任何相关肿块 [III, A]。
如果发现可疑的区域淋巴结,应进行典型活检(representative biopsy)(优先选择切除活检) [III, A]。
建议移除对侧植入物,特别是如果有纹理 [III, A]。
不推荐进行乳房切除术 [IV, D]。
对于适应性TNM分期为IIA-IIB的疾病,以及在IA-IC期疾病如果存在残留疾病的证据,建议在手术后进行IRST(例如15次分割的30Gy)[III, A]。
对于在IRST后有残留疾病以及患有晚期疾病(III-IV期)患者,建议进行6个周期的BV-CHP、CHOP或CHOEP [III, A]。
对于化疗缓解患者,可以考虑Auto-HSCT [III, B]。
对于化疗缓解且晚期的患者,可以考虑进行双侧包膜切除 [III, B]。
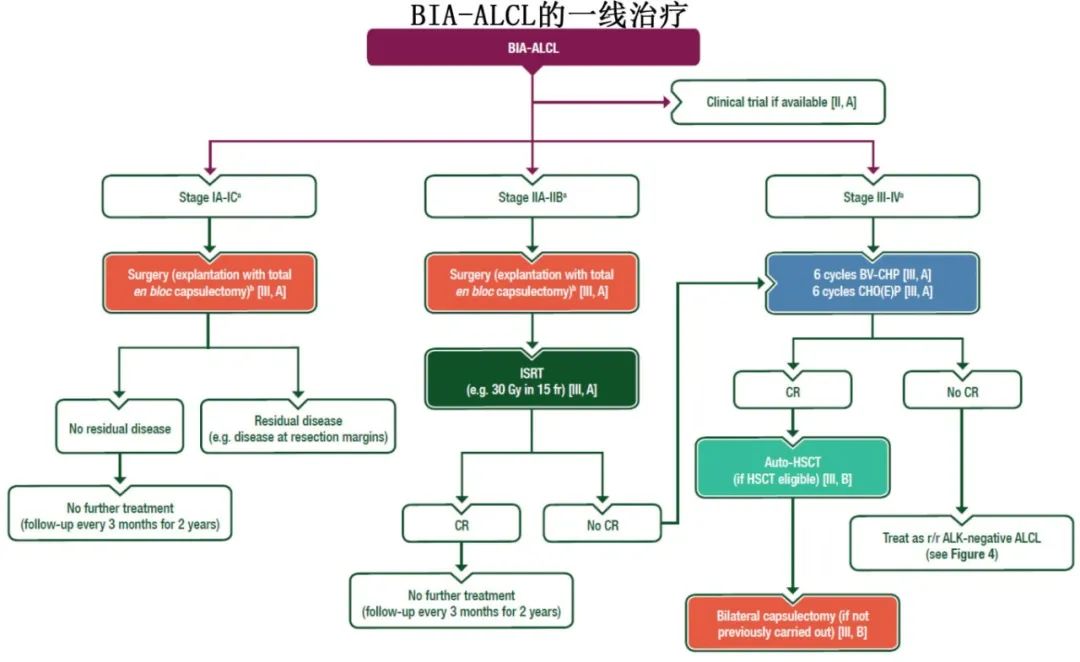
肝脾T细胞淋巴瘤(HSTCL)
在缺乏临床试验的情况下,对于fit且适合HSCT的患者,建议采用比CHOP更具侵袭性的化疗 [III, A]。
建议ICE作为一线治疗的首选方案 [IV, B]。其他选择包括IVAC、地塞米松-大剂量阿糖胞苷-顺铂(DHAP)、地塞米松-阿糖胞苷-奥沙利铂(DHAX)和CHOEP [IV, C]。
对于frail和/或不适合HSCT的患者,化疗选择包括减少剂量的ICE和吉西他滨-奥沙利铂(GEMOX)[IV, C]。
由于HSTCL经常累及骨髓,通过PET-CT进行的反应评估应通过骨髓活检来证实,并且尽量进行肝脏活检,因为弥漫性肝内肿瘤细胞浸润在PET-CT上可能难以识别 [III, A]。
如果可能的话,应通过流式细胞术分析骨髓和外周血样本,以评估肿瘤细胞表面的抗原,这些抗原无法通过常规免疫组化实现可靠识别(例如CD52) [III, B]。
对于缓解(CR或PR)的合格患者,应进行巩固性HSCT,最好是异体造血干细胞移植(allo-HSCT) [III, A]。对于不适合allo-HSCT的患者,推荐Auto-HSCT [III, A]。

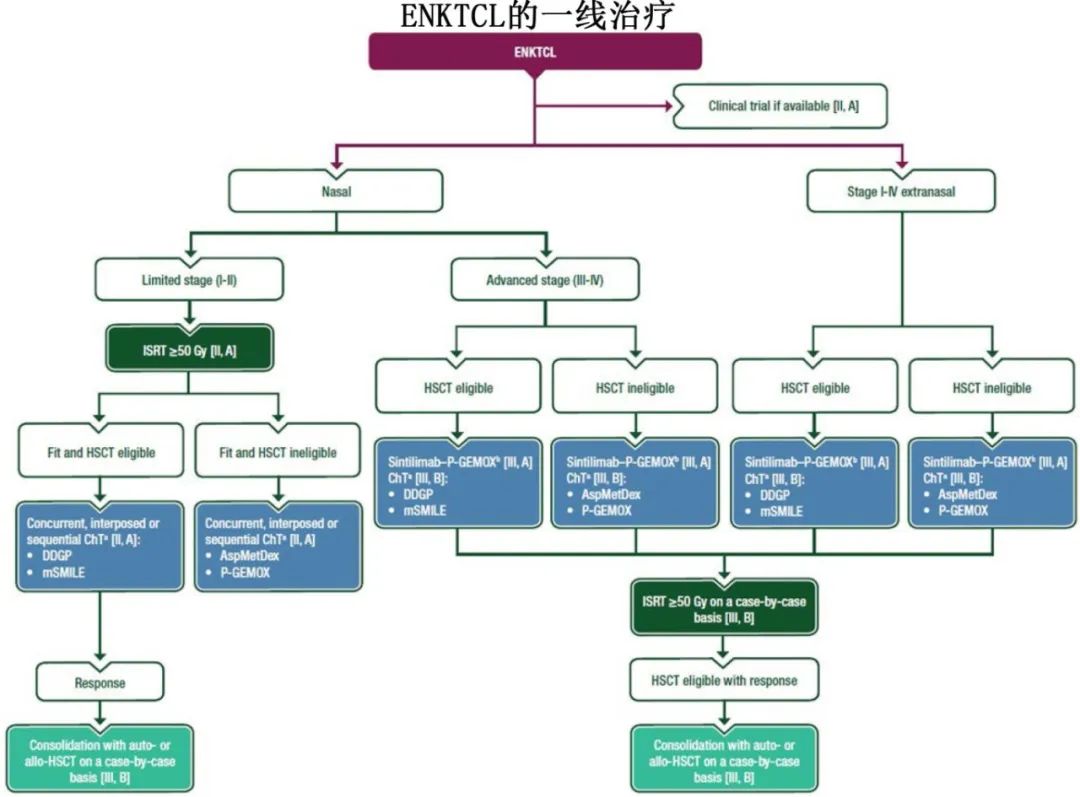
结外NK或T细胞淋巴瘤(ENKTCL)
在基于影像的反应评估的基础上,应通过定量PCR在基线和治疗期间监测外周血中的EB病毒DNA,作为反应的生物标志物 [II, A]。
Fit的局限期患者应接受IRST(≥50Gy),伴随同步、嵌入或顺序进行不含蒽环类药物、含有L-天冬酰胺酶的化疗 [例如DDGP或改良SMILE(mSMILE)用于适合HSCT的患者,AspMetDex或P-GEMOX用于不适合HSCT的患者] [II, A]。
对于III期和IV期鼻部疾病或I-IV期鼻外疾病的患者,可以推荐使用含有多药、不含蒽环类药物、含有L-天冬酰胺酶的方案(例如DDGP或mSMILE用于适合HSCT的患者,AspMetDex或P-GEMOX用于不适合HSCT的患者) [III, B]。是否添加放疗可以根据具体情况决定 [III, B]。
对于III期和IV期鼻部疾病或I-IV期鼻外疾病的患者,也应考虑使用抗PD-1抗体(如信迪利单抗)联合含L-天冬酰胺酶的方案(例如P-GEMOX)进行一线治疗 [III, A]。
如果可用,对于对大肠杆菌来源的L-天冬酰胺酶产生过敏反应或灭活抗体的患者,建议使用由欧文氏菌(Erwinia chrysanthemi)提取的L-天冬酰胺酶(crisantaspase) [III, A;在ENKTCL中未获得EMA或FDA批准]。
对于缓解的高危且适合HSCT的患者,可以考虑进行巩固性auto或allo-HSCT [III, B]。是否进行HSCT应根据具体情况决定,考虑因素包括治疗前风险特征、对一线治疗的反应、体能状态(PS)和供者的可用性 [III, B]。
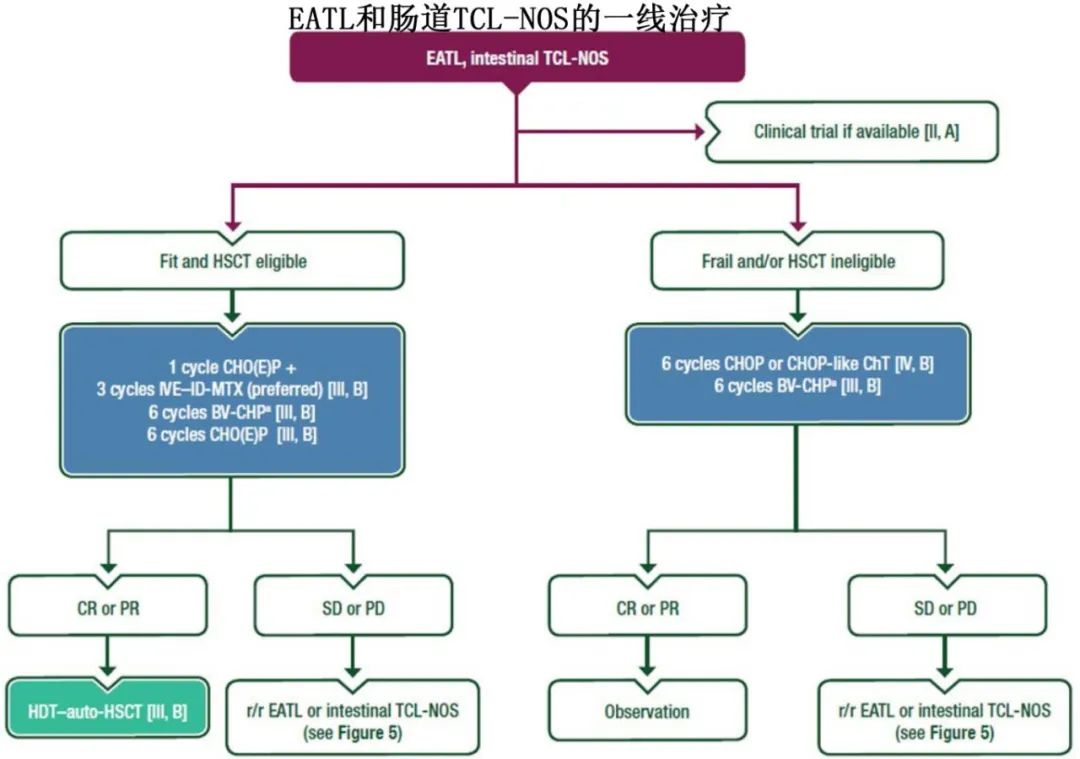
肠病相关T细胞淋巴瘤(EATL)和肠道T细胞淋巴瘤-非特指型(TCL-NOS)
对于fit且适合HSCT的患者,建议进行一个周期的CHOP或CHOEP,然后进行三个周期的IVE交替使用中等剂量的MTX [III, B]。其他选择方案包括六个周期的BV-CHP(FDA批准,EMA未批准)、CHOP或CHOEP [III, B]。
对于缓解且适合HSCT的患者,可以考虑进行巩固性大剂量化疗-auto-HSCT [III, B]。
对于frail或不适合HSCT的患者,建议进行六个周期的CHOP或CHOP样化疗 [IV, B],或者六个周期的BV-CHP [III, B;FDA批准,EMA未批准]。
T细胞幼淋巴细胞白血病(T-PLL)
对于无症状的T-PLL患者,建议采取观察等待 [III, B]。
对于新诊断的有症状T-PLL患者,建议使用Alemtuzumab(通过静脉注射,第一周剂量递增为3、10和30mg,随后每周三次,每次30mg,共10-12周) [III, A;未获得EMA或FDA批准,但可通过患者指定使用]。
建议在治疗前后以及治疗期间通过流式细胞术评估CD52状态 [III, B]。
在Alemtuzumab治疗期间,建议进行抗水痘-带状疱疹病毒和肺孢子菌的预防,以及定量监测巨细胞病毒DNA [III, A]。
对于达到CR且有供者的合格患者,建议进行巩固性非清髓性allo-HSCT [III, B];否则的话,可以考虑根据具体情况进行auto-HSCT [IV, C]。

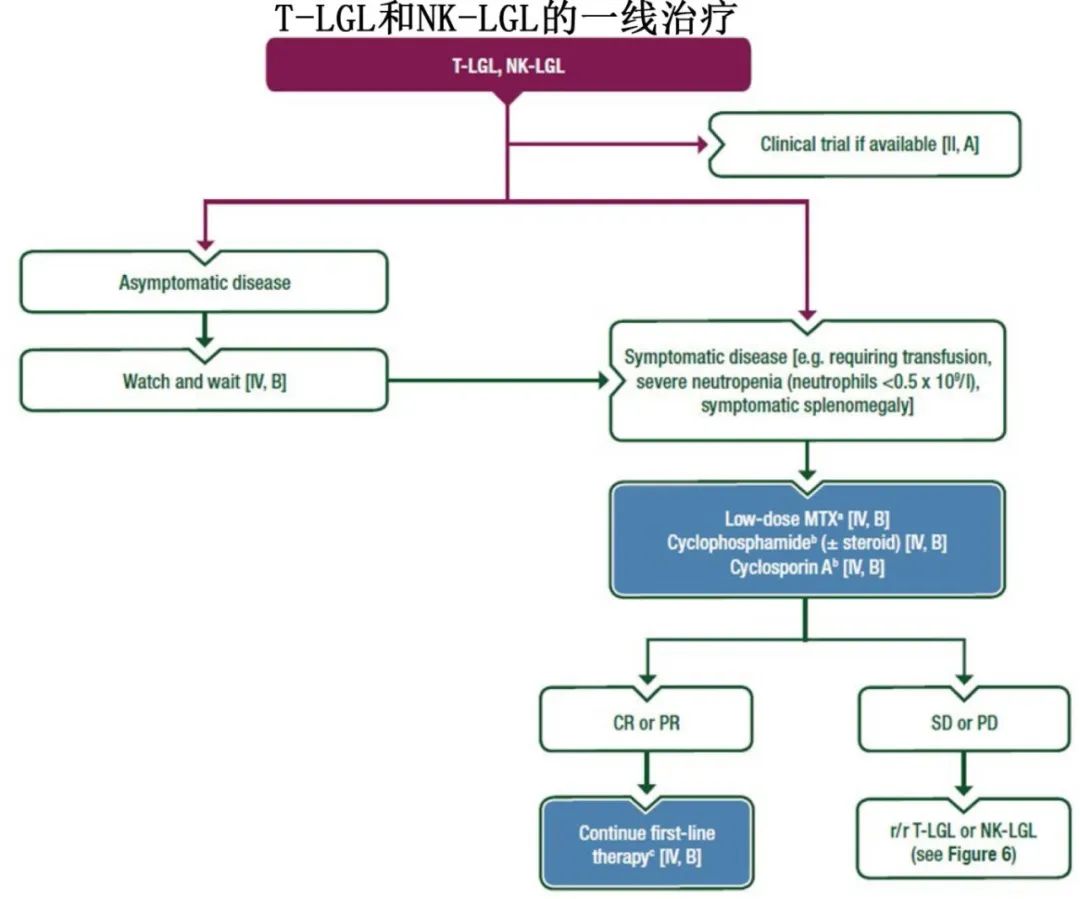
T细胞大颗粒淋巴细胞白血病(T-LGL)和NK细胞大颗粒淋巴细胞白血病(NK-LGL)
对于无症状且没有严重血细胞减少症或显著脾肿大的患者,最初可以通过观察进行管理 [IV, B]。
对于有症状的患者(例如需要输血的贫血和/或血小板减少症、严重中性粒细胞减少症[中性粒细胞<0.5×10⁹/l]和/或有症状的脾肿大),可以开始使用免疫抑制剂进行一线治疗,包括每周低剂量甲氨蝶呤(MTX)(首选用于有相关自身免疫疾病的患者是)、环磷酰胺(联合或不联合类固醇)或环孢素A(后两种首选用于重度血细胞减少症的患者是)[IV, B]。
可以在3-4个月后评估一线治疗的疗效,如果缓解(CR或PR)和可行性令人满意,则可以继续相同的治疗 [IV, B]。
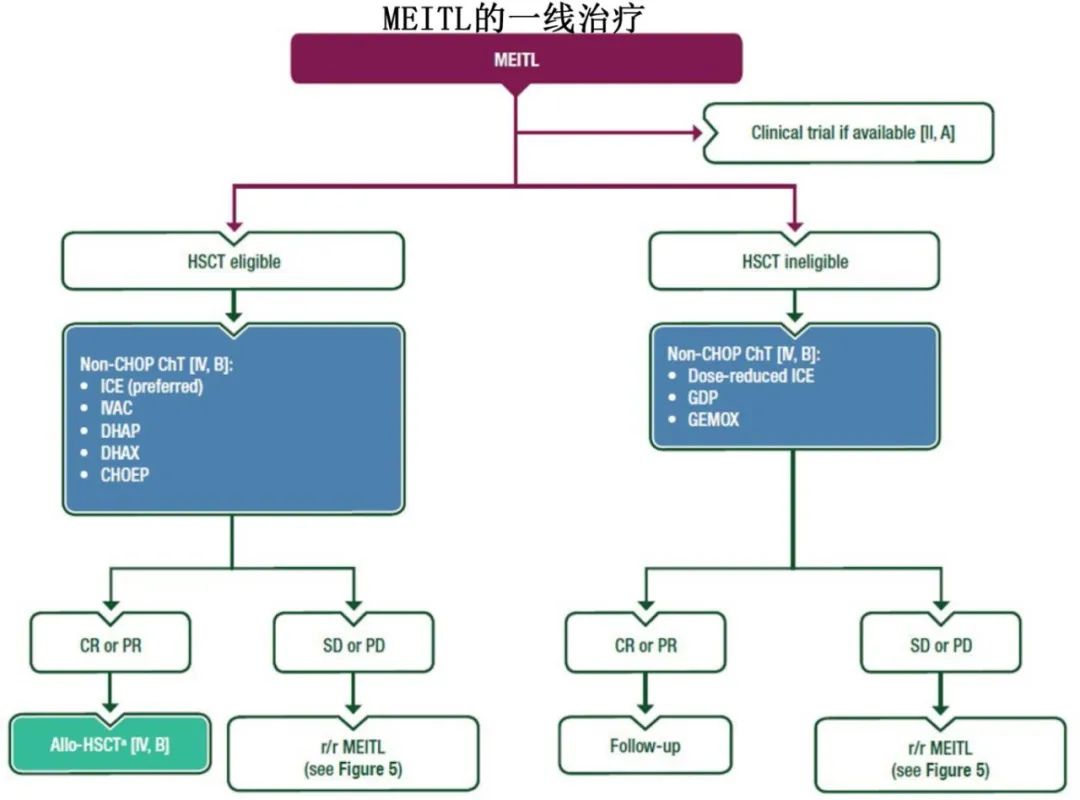
单形性亲上皮性肠道T细胞淋巴瘤(MEITL)
建议使用非CHOP多药化疗(优先推荐) [IV, B]。
-
对于适合HSCT的患者,选择包括ICE(优先推荐)、IVAC、DHAP、DHAX和CHOEP [IV, B]。
-
对于不适合HSCT的患者,选择包括剂量减少的ICE、吉西他滨-地塞米松-顺铂(GDP)和GEMOX [IV, B]。
对于有合适供者且对化疗敏感(CR或PR)的适合HSCT患者,可以考虑进行Allo-HSCT巩固治疗 [IV, B]。
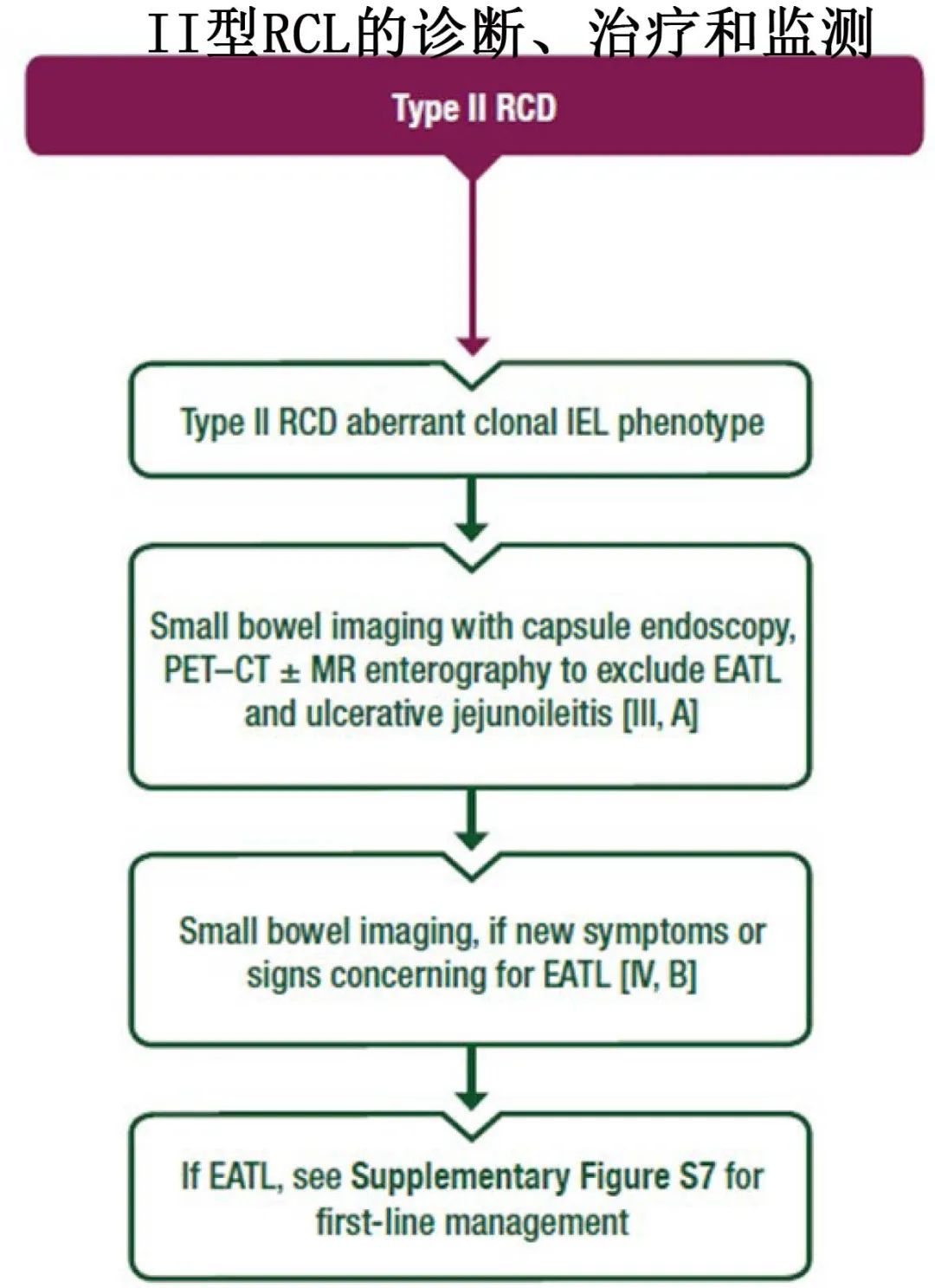
II型难治性乳糜泻(RCD)
如果发现异常的克隆性上皮内淋巴细胞,应进行小肠成像检查,包括胶囊内镜和PET-CT扫描(可补充磁共振肠造影)以排除EATL和溃疡性空回肠炎 [III, A]。
组织活检应由经验丰富的血液病理学家检查,以识别提示EATL的病变(包括CD30表达) [III, A]。
如果诊断EATL,应开始针对该病种的特定治疗。如果没有,可以考虑每6-12个月进行一次EATL检查,包括在出现新的症状或体征提示EATL时进行小肠成像 [IV, B]。
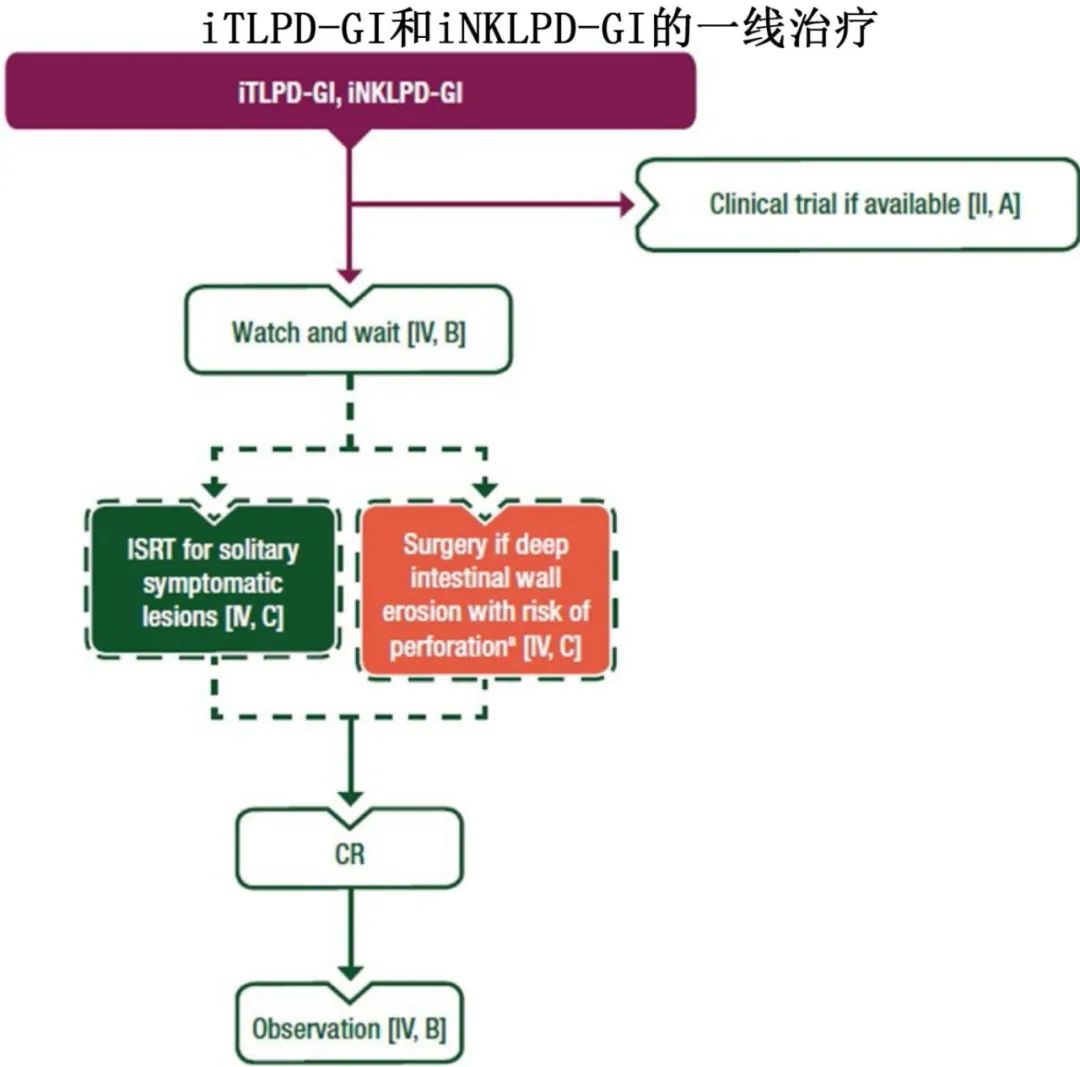
胃肠道惰性T淋巴组织增生性疾病(iTLPD-GI)和胃肠道惰性NK淋巴组织增生性疾病(iNKLPD-GI)
只有在证实有疾病扩散和/或组织学转化的情况下,才应使用基于传统联合化疗的侵袭性方法 [IV, B]。
可以推荐采取观察方法,主要集中在排除疾病进展和扩散 [IV, B]。可以对个别病变进行内镜检查,以评估肠道壁穿孔的风险(例如是否存在深部溃疡) [IV, C]。
对于孤立性有症状病变,可以考虑IRST [IV, C]。
如果存在深部肠道壁溃疡(例如由于随后的局部感染或炎症导致的浅表黏膜溃疡加深),且穿孔风险高,可以考虑进行局部手术切除 [IV, C]。
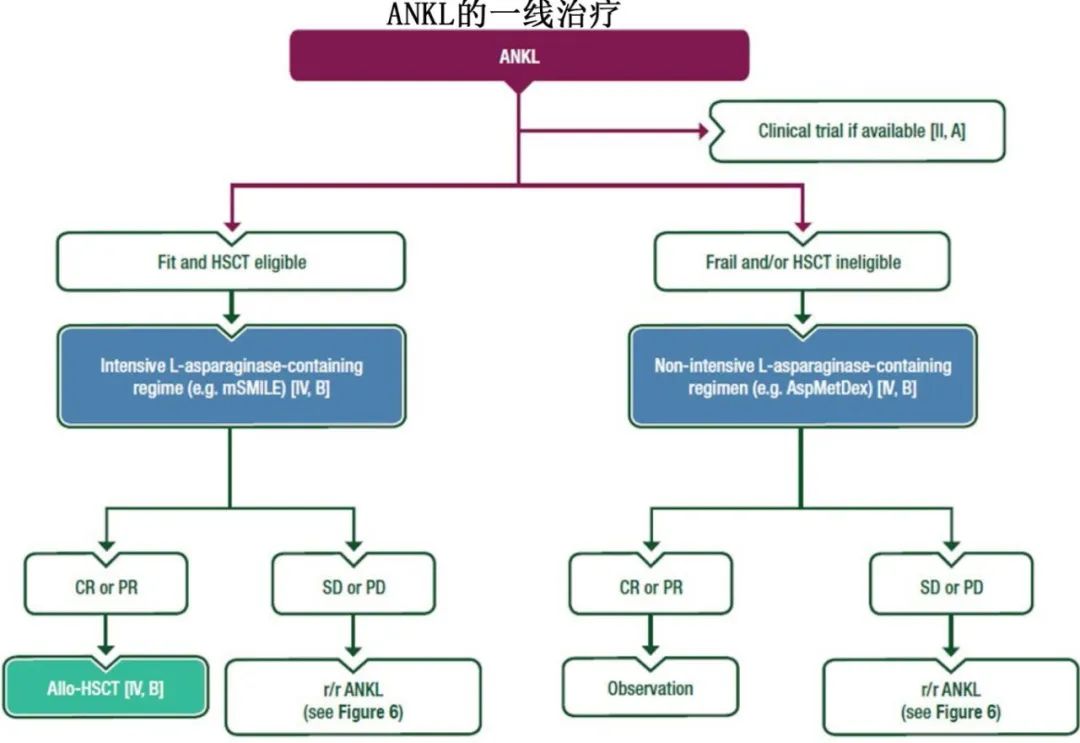
侵袭性NK细胞白血病(ANKL)
对于fit且适合HSCT患者,可以推荐使用含L-天冬酰胺酶的强化疗一线方案(例如改良SMILE方案) [IV, B],目的是通过allo-HSCT巩固初步反应 [IV, B]。
对于frail和/或不适合HSCT的患者,可以考虑使用非强化的含L-天冬酰胺酶的化疗方案(例如AspMetDex) [IV, B]。
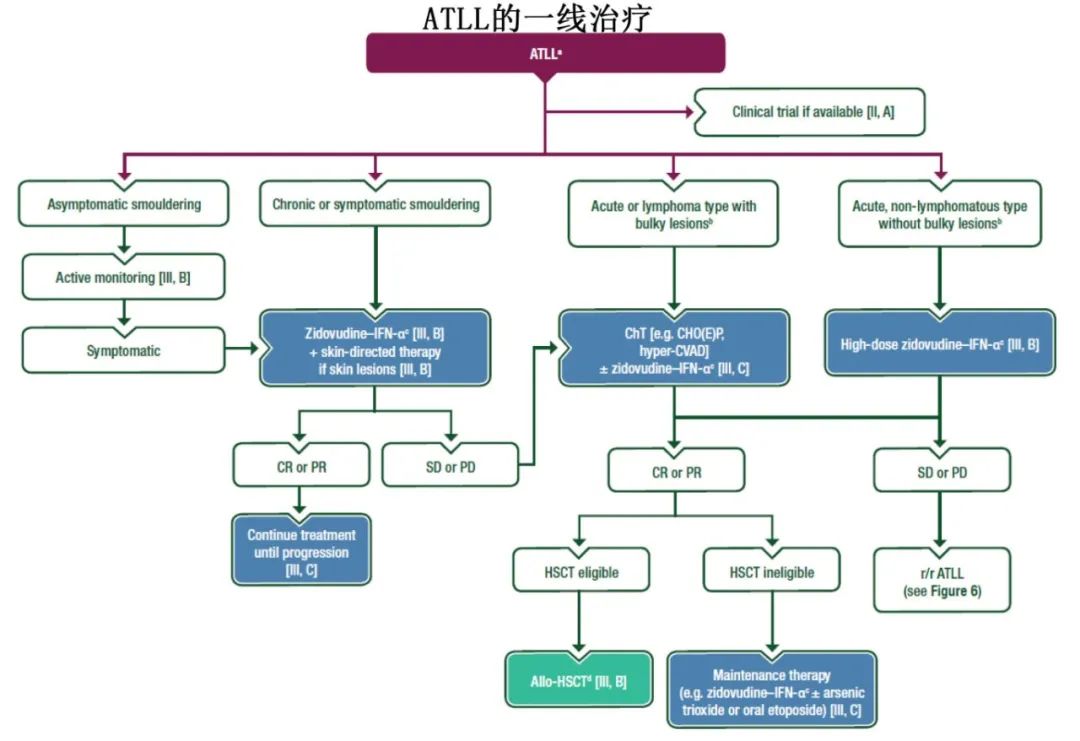
成人T细胞白血病或淋巴瘤(ATLL)
建议对ATLL患者的直系亲属和伴侣进行HTLV-1检测 [II, B]。
建议所有患者使用抗微生物药物预防机会性感染 [II, B]。如果粪类圆线虫(Strongyloides stercoralis)血清学检测结果呈阳性,即使患者无症状,也可以开始治疗 [III, B]。
无症状的慢性ATLL可以通过积极监测进行管理,无需立即进行治疗干预 [III, B]。
对于有症状的慢性ATLL(皮肤或肺部病变、机会性感染)、原发性皮肤型伴有肿瘤性病变或慢性ATLL患者,建议使用齐多夫定联合干扰素α(IFN-α) [III, B;未获得EMA或FDA批准],如果存在皮肤病变,还可以进行针对皮肤的治疗 [III, B]。
建议对所有急性型或淋巴瘤型ATLL患者进行CNS预防 [III, B]。
对于急性、非大包块、非淋巴瘤型ATLL患者,如果可行,特别是对于不适合强化疗或allo-HSCT的患者,建议使用大剂量齐多夫定联合干扰素α作为一线治疗 [III, B;未获得EMA或FDA批准]。
对于有大包块的急性或淋巴瘤型ATLL患者,可以给予强化联合化疗 [例如CHOP、CHOEP或超分割环磷酰胺-长春新碱-柔红霉素-地塞米松-甲氨蝶呤-阿糖胞苷(超分割CVAD)],根据患者耐受性,可同步或序贯使用齐多夫定联合干扰素α [III, C;未获得EMA或FDA批准]。
对化疗敏感的患者可以进行allo-HSCT [III, B]。可以在预处理方案中添加抗逆转录病毒药物,以防止供者细胞被HTLV-1新感染 [III, B]。
对于不适合allo-HSCT的缓解患者,可以使用齐多夫定联合干扰素α进行维持治疗,可联合或不联合砷剂 [III, C;未获得EMA或FDA批准]。如果齐多夫定联合干扰素α耐受性差或不再有反应,可以考虑使用口服低剂量依托泊苷作为单药治疗或作为方案的一部分 [III, C]。
一线治疗的总结如下

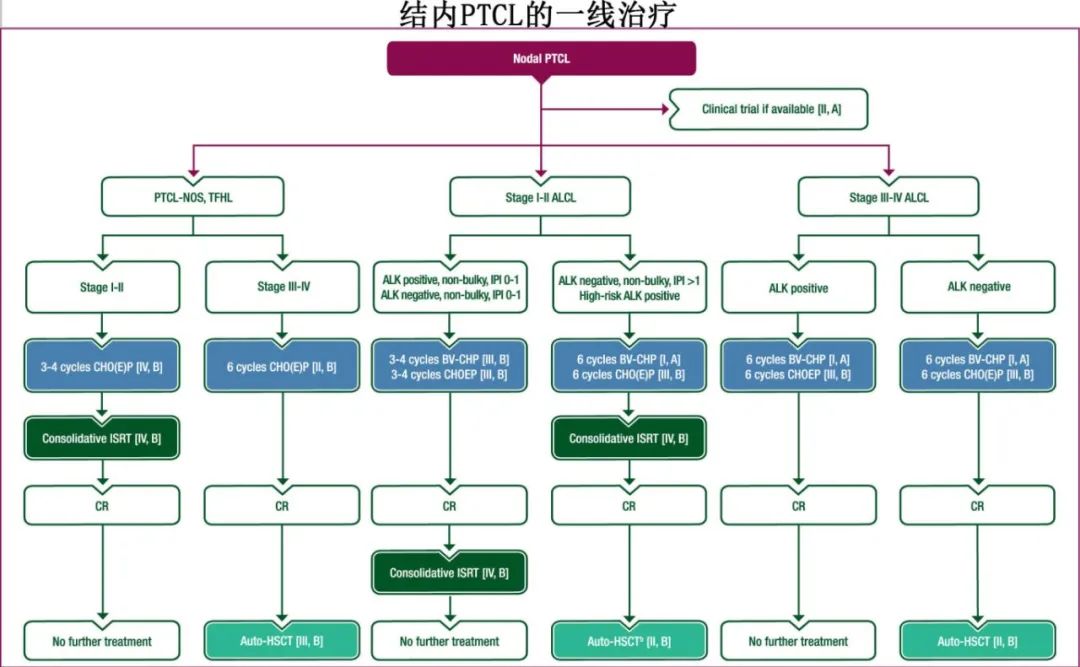
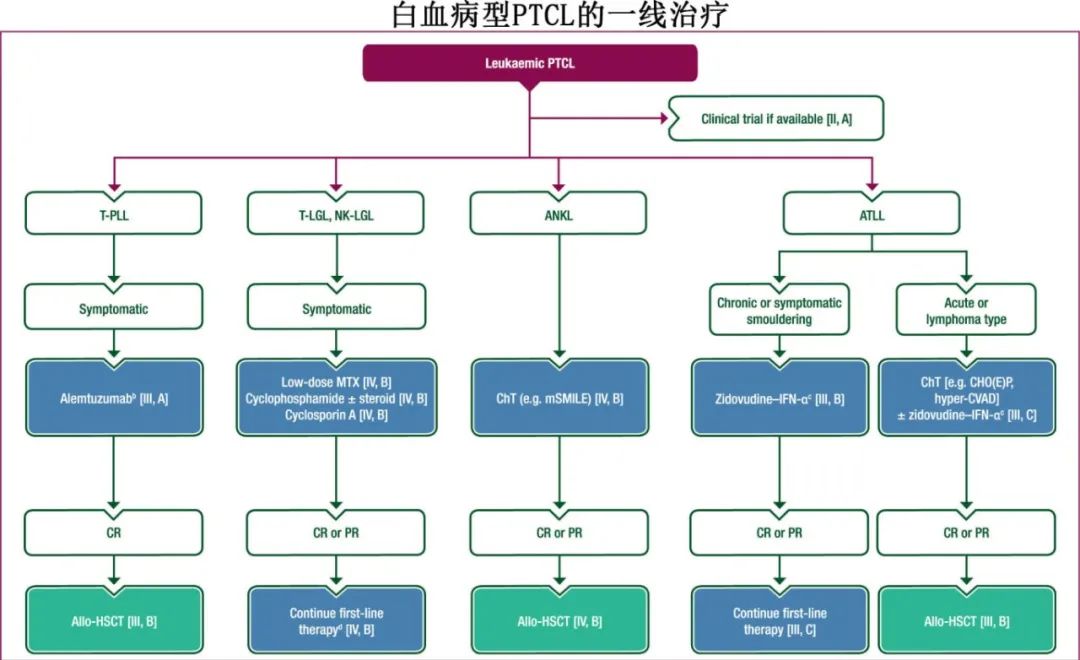
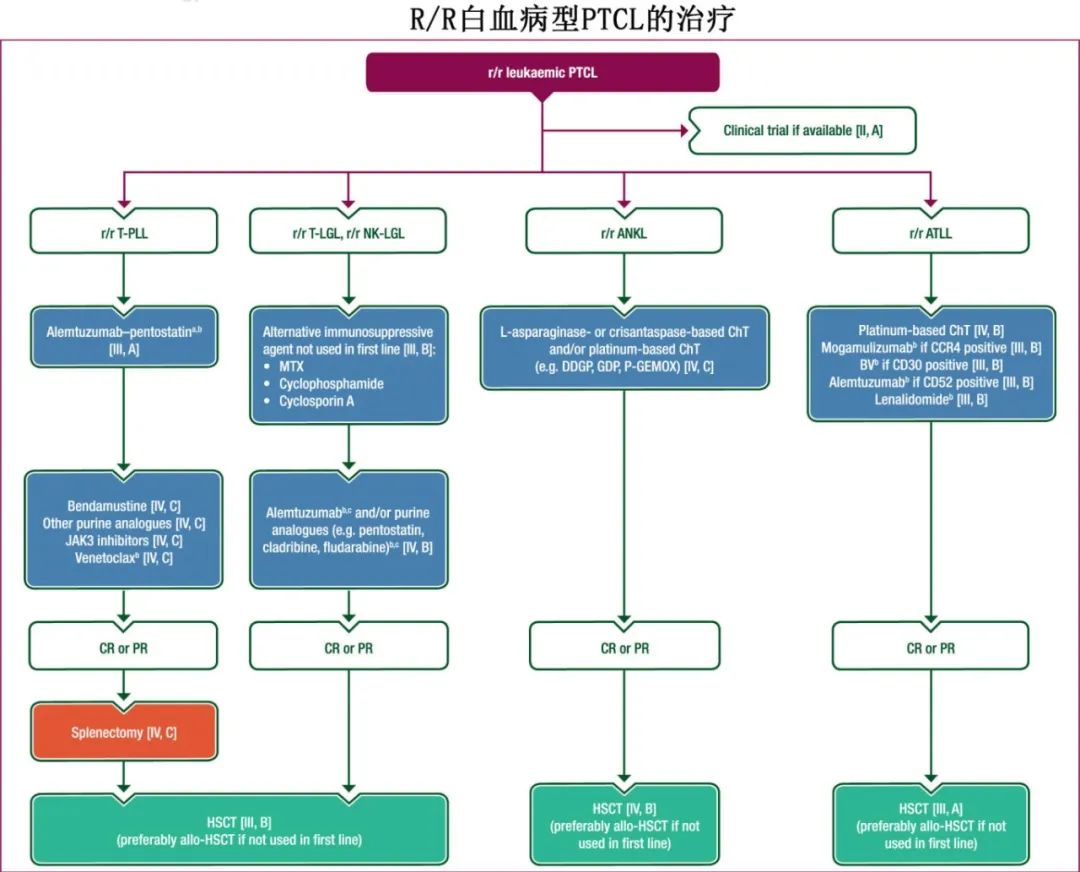
复发难治性(R/R)疾病的治疗
R/R PTCL 预后不良,尽可能入选临床试验[II,A]。
R/R结内和结外PTCL,除外ALK阳性ALCL、ENKTCL、iTLPD-GI和iNKLPD-GI
如果没有临床试验可用,可以考虑使用与一线蒽环类药物化疗无交叉耐药的铂类药物方案 [III, B]。
-
对于 R/R PTCL-NOS和TFHL,选择包括ICE、DHAP、GDP、IVAC+MTX和5-aza(仅限TFHL) [III, B]。对于不适合强化疗的患者,选择包括来那度胺(未获得EMA或FDA批准)、苯达莫司汀和环孢素A [III, B]。
-
对于R/R ALK阴性ALCL和BIA-ALCL,选择包括ICE、DHAP、GDP和IVAC+MTX [III, B]。BV单药治疗也可作为选择 [III, B]。
-
对于R/R HSTCL和MEITL,选择包括ICE和DHAP [III, B]。如果通过流式细胞术(例如骨髓或外周血样本)证实肿瘤细胞为CD52阳性,也可以选择嘌呤类似物,联合或不联合alemtuzumab [IV, C;未获得EMA或FDA批准]。
-
对于R/R EATL和肠道TCL-NOS,选择包括ICE、DHAP和IVAC+MTX [III, B]。
对于对挽救治疗有反应且适合HSCT的患者,可以考虑进行HSCT(优选allo-HSCT,如果在一线治疗中未使用) [II, B]。
R/R ALK阳性ALCL
对于未接受一线BV治疗或在初次缓解后晚期复发的患者,建议使用BV [III, A]。
对于BV耐药的患者,应考虑使用ALK抑制剂,如克唑替尼(在儿童和青少年中获得EMA和FDA批准)、阿来替尼(未获得EMA或FDA批准)、brigatinib(未获得EMA或FDA批准)或塞瑞替尼(未获得EMA或FDA批准) [III, A]。化疗(例如ICE、DHAP或IVAC+MTX)也可作为选择 [III, B]。
应根据挽救治疗的反应、当前缓解质量、合并症和预测的耐受性考虑巩固性allo-HSCT [III,A]。
R/R ENKTCL
如果可用,抗 PD-1 抗体如帕博利珠单抗(未经 EMA 或 FDA 批准)或纳武利尤单抗(未经 EMA 或 FDA 批准)可作为单药治疗或联合吉西他滨和/或左旋门冬酰胺酶或 crisantaspase [III,B]。
作为替代方案,也可考虑使用含铂治疗方案(例如GDP)[III,B]。
对于对挽救治疗有反应的适合 HSCT 患者,可考虑HSCT(首选allo-HSCT,如果一线治疗未使用)[III,C]。
R/R T-PLL
对于仍有 CD52 阳性肿瘤细胞的患者,建议在6个月无治疗期后使用Alemtuzumab联合喷司他丁 [III,A;未经 EMA 或 FDA 批准]。苯达莫司汀、其他嘌呤类似物、JAK3抑制剂和维奈克拉(未经 EMA 或 FDA 批准)是Alemtuzumab-喷司他丁后的选择 [IV,C]。
缓解患者可考虑脾切除术 [IV,C]。
对于适合HSCT 的缓解患者,可推荐巩固HSCT(首选allo-HSCT,如果一线治疗未使用)[III,B]。
R/R T-LGL 和 NK-LGL
可考虑一线治疗建议列表中的替代免疫抑制剂(MTX、环磷酰胺、环孢素A)[III,B]。
对MTX、环磷酰胺或环孢菌素 A 无反应的患者可考虑使用Alemtuzumab(未经 EMA 或 FDA 批准)和/或嘌呤类似物(未经 EMA 或 FDA 批准;例如喷司他丁、克拉屈滨、氟达拉滨)[IV,B]。
对于适合HSCT的缓解患者,可推荐巩固HSCT(首选allo-HSCT,如果一线治疗未使用)[III,B]。
R/R iTLPD-GI 和 iNKLPD-GI
可推荐观察等待 [IV,B],对于伴有溃疡的局部疾病考虑ISRT [IV,C],对于伴有溃疡或穿孔风险的局部疾病可选择手术 [IV,C]。
R/R ANKL
如果没有临床试验可用且患者体能状态(PS)允许,可以考虑使用替代的含L-天冬酰胺酶或crisantaspase以及/或铂类药物的方案(例如DDGP、GDP、P-GEMOX) [IV, C]。
对于对挽救治疗有反应且适合HSCT条件的患者,如果在一线治疗中未使用,可以考虑进行Allo-HSCT [IV, B]。
R/R ATLL
可考虑使用含铂二线治疗方案 [IV,B]。
可以考虑mogamulizumab(如果 CCR4 阳性;非 EMA 或 FDA 批准)、BV(如果 CD30 阳性;非 EMA 或 FDA 批准)、alemtuzumab(如果 CD52 阳性;非 EMA 或 FDA 批准)或来那度胺(非 EMA 或 FDA 批准)单药治疗 [III,B]。
适合HSCT的缓解患者应考虑Allo-HSCT(如果未用于一线治疗)[III,A]。
如果计划进行allo-HSCT,不应在 allo-HSCT 前50天内给予mogamulizumab [III,A]。
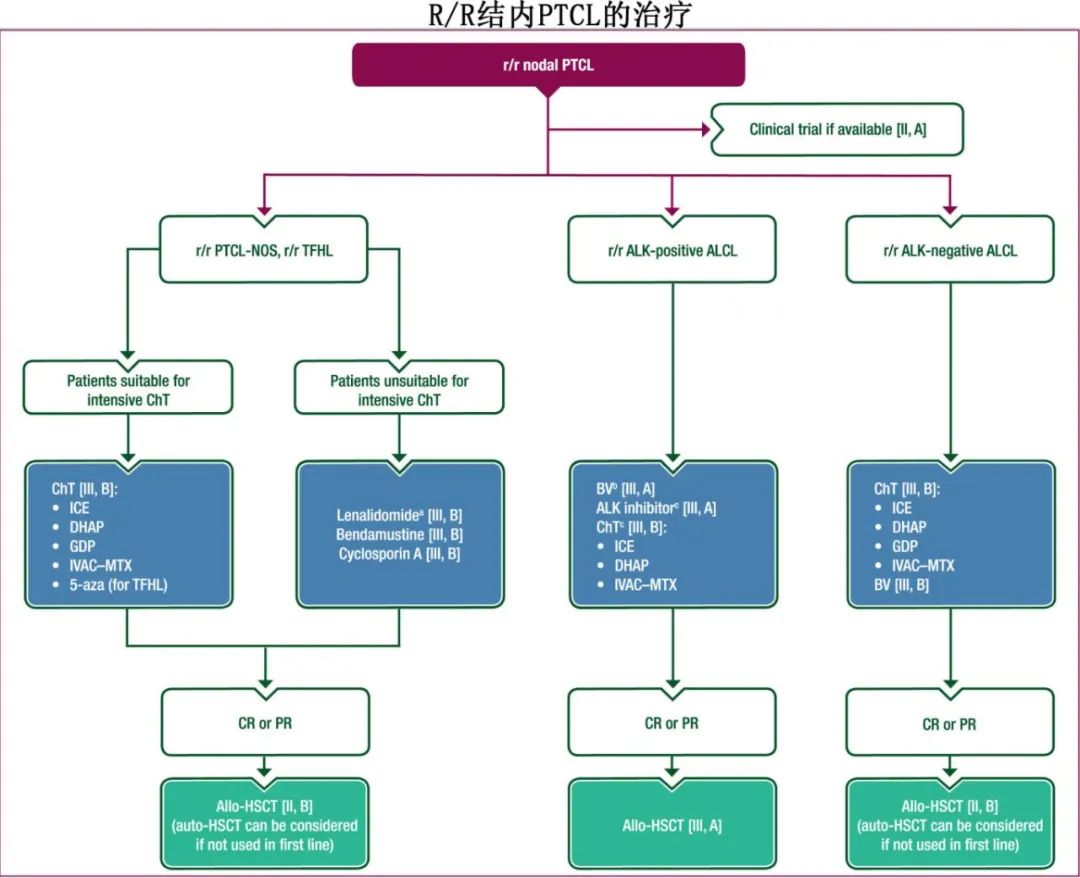
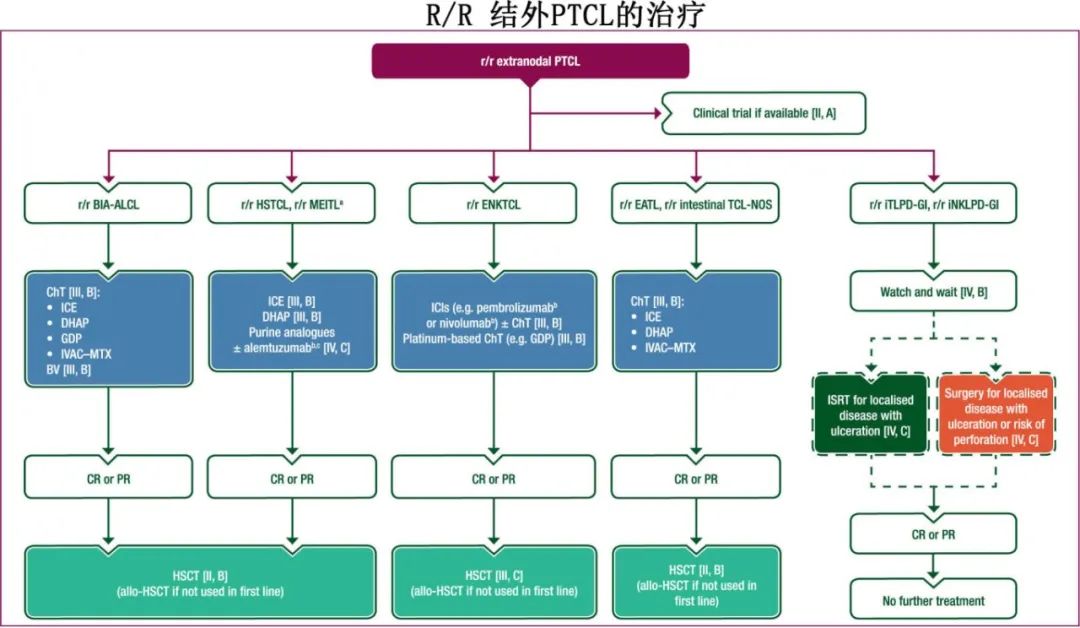
疗效评估和随访
可以进行中期评估以评估化疗敏感性 [II, B]。
如果最初有骨髓受累,治疗结束时(EOT)可以重复进行诊断影像学检查(优先选择PET-CT)以及骨髓活检 [II, B]。
在结内PTCL中中期PET反应具有预后价值,但不适用于ALK阳性ALCL [II, B]。
随访可能包括每3个月进行一次病史和体格检查,持续1年,然后每6个月进行一次,对于非auto-HSCT巩固治疗的患者再持续2年,对于auto-HSCT巩固治疗的患者持续再4年 [IV, C]。
对于达到CR的患者,不推荐常规使用PET-CT或诊断性CT进行监测 [III, D]。
对于ENKTCL患者,建议进行EB病毒DNA监测 [II, A];对于在诊断时有循环EB病毒DNA的结内PTCL患者,可选EB病毒DNA监测[IV, C]。
如果患者处于持续CR状态:对于非移植的无症状患者,随访可以在3年后停止 [III, B];对于接受auto-HSCT的无症状患者,随访可以在5年后停止 [III, B]。对于接受allo-HSCT的患者,应遵循allo-HSCT的一般指南 [III, A]
参考文献
F d'Amore, M Federico, L de Leval,et al.Peripheral T- and natural killer-cell lymphomas: ESMO-EHA Clinical Practice Guideline for diagnosis, treatment and follow-up.Ann Oncol . 2025 Mar 14:S0923-7534(25)00059-6. doi: 10.1016/j.annonc.2025.01.023
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)