首页 > 医疗资讯/ 正文
4月10日,东北大学理学院徐章润教授团队在国际权威学术期刊《自然—通讯》(Nature Communications)杂志在线发表了题为“FRET imaging of glycoRNA on small extracellular vesicles enabling sensitive cancer diagnostics”的研究论文。徐章润教授团队提出一种双识别Förster共振能量转移技术(drFRET),首次实现生物体液中新型癌症标志物——小细胞外囊泡上糖基化RNA(glycoRNA)的灵敏检测,为癌症早筛与精准分型提供了新工具!东北大学为该论文的第一作者单位,东北大学理学院化学系博士研究生任廷举为该论文的第一作者,徐章润教授为该文的唯一通讯作者。

2021年,斯坦福大学Carolyn R. Bertozzi教授(2022年诺贝尔化学奖得主)团队在《Cell》发表突破性成果,揭示了细胞表面存在一类新型生物分子——糖基化RNA(glycoRNA),首次证实RNA不仅能被糖基化修饰,还可锚定于细胞膜表面参与生物识别。GlycoRNAs是一类兼具 RNA 序列信息与聚糖修饰的新型膜锚定分子,由含有唾液酸的聚糖修饰的小RNA组成,具有潜在的重要生理功能。这类由 RNA 与 N-糖链共价连接形成的生物分子,通过聚糖末端的 N-乙酰神经氨酸(Neu5Ac)等结构,参与细胞黏附、信号传递等关键生理过程。然而,由于缺乏高效且特异性的成像技术,人们对glycoRNA的认知仍十分有限。
为了解决这一问题,徐章润教授研究团队开发了一种基于双识别Förster共振能量转移的glycoRNA原位成像方法。这种方法首次直接原位观测小细胞外囊泡(sEVs)上的glycoRNA,并具有极高的灵敏度和特异性。研究团队首先通过代谢标记与点击化学等技术,证实了 sEVs 表面存在 Neu5Ac 修饰的 glycoRNAs,并验证了不同糖基化修饰的 glycoRNAs 在 sEVs 中的存在。drFRET 技术的核心在于构建“聚糖-核酸”双识别探针系统,通过分子间近场能量转移实现 glycoRNAs 的原位可视化。drFRET技术通过两种功能化DNA探针协同作用:糖链识别探针,设计偶联Cy3供体荧光染料的DNA 适配体,利用其空间折叠特性精准识别 glycoRNAs 末端的Neu5Ac;RNA 原位杂交探针,针对目标 glycoRNA 序列设计互补寡核苷酸链,标记受体荧光染料 Cy5,通过碱基配对实现 RNA 组分的特异性锚定。当两类探针在 sEVs 表面形成空间近场(1–10 nm)时,激发态的 Cy3 通过偶极-偶极耦合向 Cy5 传递能量,产生非辐射能量转移信号。通过敏化发射校正技术消除光谱串扰,确保信号仅来源于聚糖与 RNA 的共价结合位点,有效规避了传统单探针检测的非特异性干扰。
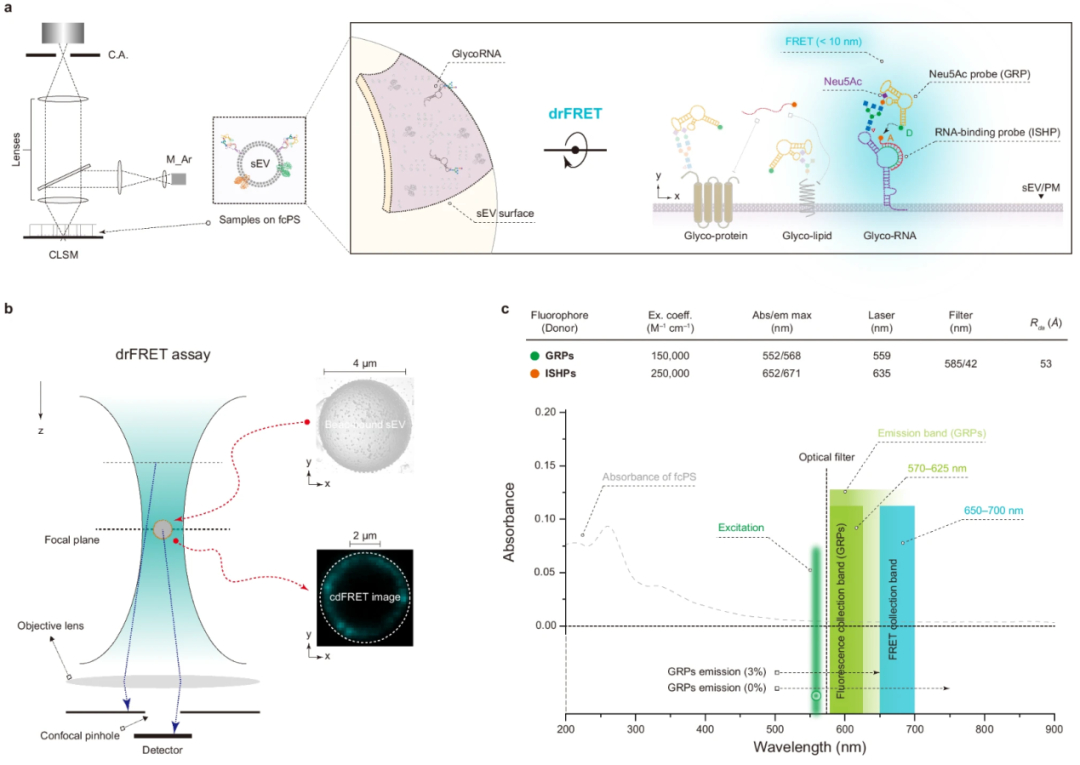
图 drFRET方法原位成像小细胞外囊泡表面的glycoRNAs
研究团队利用drFRET技术分析了来自7种癌症细胞系及100例临床样本的sEVs glycoRNAs。通过对血清来源的 sEVs 表面 5 种glycoRNAs的信号进行无监督层次聚类分析,癌症与非癌症样本形成完全分离的聚类簇,其诊断灵敏度与特异性均达 100%(95% CI)。进一步通过主坐标分析构建癌症精准分型模型,6 种癌症类型的总体分类准确率达 89%(95% CI)。研究表明,肿瘤sEVs表面glycoRNA的异常表达与癌症进展高度相关,这为癌症液体活检提供了全新分子靶标。研究还揭示了 glycoRNAs 可能通过糖-蛋白相互作用介导 sEVs 与靶细胞的黏附及内吞过程,并最终可能在肿瘤细胞向远端器官递送信息、构建转移前微环境中发挥关键作用。
本研究工作得到了国家自然科学基金资助。参与该工作的还有中国医科大学第一附属医院/国家医学检验临床医学研究中心张潆之博士、东北大学理学院化学系王月副教授和杨春光副教授等。王建华教授、于永亮教授等对该工作提供了大力支持与帮助。
原文链接:
https://www.nature.com/articles/s41467-025-58490-2- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)