首页 > 医疗资讯/ 正文
医学理念的转变是一个有趣的过程。记得早年在临床药物实习时,对螺内酯的初印象仅仅是"保钾利尿剂",常与呋塞米"搭档"使用。然而,随着对心衰治疗深入研究,醛固酮受体拮抗剂(MRA)已从配角华丽转身为心衰治疗的核心药物之一。今天我们就来深入探讨MRA在慢性心力衰竭中的应用,特别是其机制、临床证据与实际应用。
一、MRA的作用机制与分类
1.1 醛固酮的病理生理作用
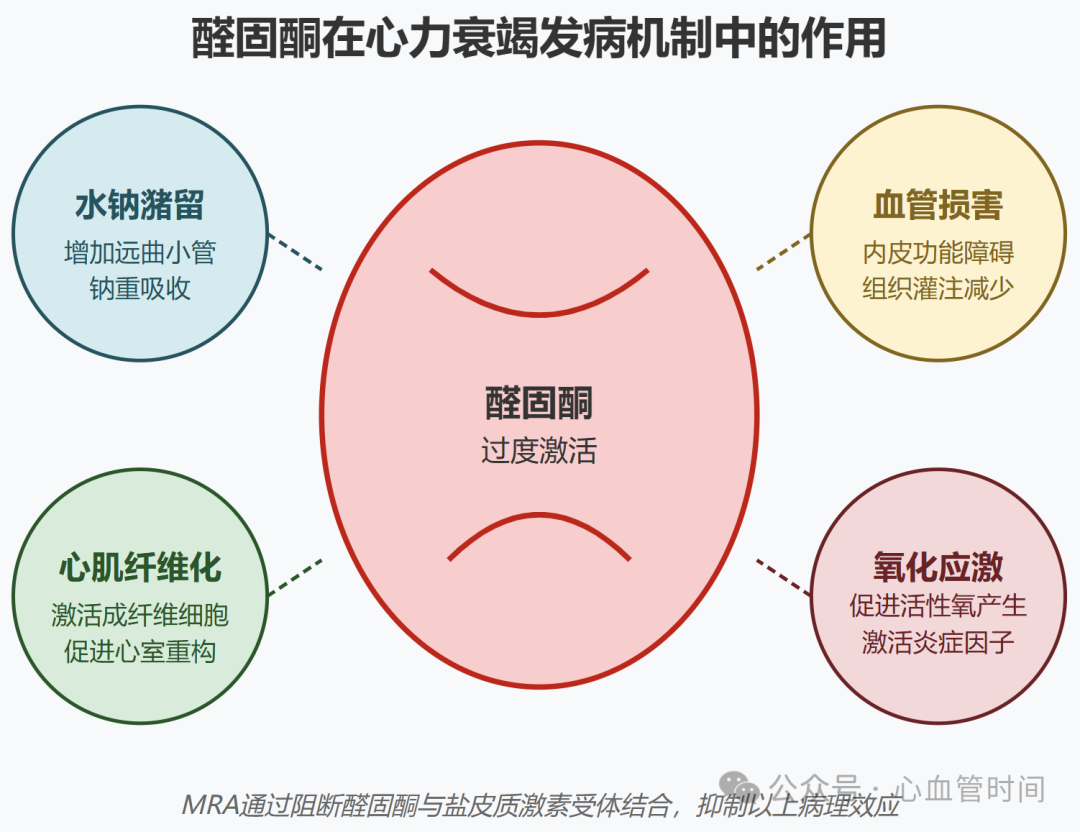
醛固酮是肾上腺皮质球状带分泌的盐皮质激素,在正常生理条件下通过与矿物质皮质激素受体(MR)结合,调节电解质平衡和血压。然而在心衰状态下,醛固酮水平显著升高,导致一系列病理效应:
-
水钠潴留:增加肾远曲小管和集合管对钠的重吸收,促进水分潴留
-
心肌纤维化:激活成纤维细胞,增加胶原合成,促进心室重构
-
血管损害:内皮功能障碍,血管收缩增强,组织灌注减少
-
氧化应激和炎症:促进活性氧产生,激活炎症因子
-
电解质紊乱:引起低钾低镁血症,增加心律失常风险
值得注意的是,醛固酮有两个重要来源:经典的RAAS系统途径和局部组织合成。局部组织合成的醛固酮不受传统ACEI/ARB完全抑制,这也是为什么需要MRA的理论基础之一。
1.2 MRA的分类与药理特点
MRA药物大致可分为三代:
-
第一代:螺内酯
-
非选择性甾体类MRA
-
与MR结合不够稳定,对雄激素、孕激素受体也有亲和力
-
导致性激素相关不良反应(如男性乳房发育)
-
第二代:依普利酮
-
选择性增强的甾体类MRA
-
对MR的选择性高于螺内酯,减少了内分泌不良反应
-
但对MR亲和力仅为螺内酯的1/40
-
第三代:非奈利酮(Finerenone)
-
高选择性非甾体类MRA
-
对MR高选择性结合,无内分泌不良反应
-
心肾分布更均衡
-
目前主要应用于CKD合并T2DM患者

笔者心得:与常见认识不同,MRA并非单纯的保钾利尿剂,其抗纤维化、抗炎和抗重构作用是改善心衰预后的关键机制。因此使用时不应仅考虑其利尿作用,更应关注其对长期预后的改善。
二、循证医学证据:MRA在心衰中的临床研究
2.1 HFrEF的里程碑研究
**RALES研究(1999年)**:作为评价MRA治疗心衰的里程碑研究,RALES纳入1663名NYHA III-IV级、LVEF≤35%的HFrEF患者,在标准治疗(当时主要是ACEI和利尿剂)基础上加用螺内酯(平均剂量26mg/d)或安慰剂。结果显示:
-
全因死亡率相对降低30%(P<0.001)
-
心衰住院率相对降低35%
-
NNT(治疗9例患者可避免1例死亡)
**EMPHASIS-HF研究(2011年)**:评估依普利酮在轻中度HFrEF患者中的疗效,纳入2737名NYHA II级、LVEF≤35%患者,结果显示:
-
心血管死亡或心衰住院复合终点降低37%
-
全因死亡降低24%
-
心衰住院降低42%
2.2 HFpEF和HFmrEF的证据
**TOPCAT研究(2014年)**:纳入3445名LVEF≥45%的HFpEF患者,在北美地区参与者中:
-
螺内酯未能显著降低主要复合终点(心血管死亡、心脏骤停和心衰住院)
-
但显著降低心衰住院风险(17%)
随后的亚组分析显示,对于LVEF在45-55%的患者及伴有升高BNP或近期因心衰住院者,获益更为明显。
荟萃分析证据:对于HFmrEF(LVEF 41%-49%)患者,荟萃分析提示MRA可能带来与HFrEF类似的获益,但仍需更多针对性研究验证。
2.3 醛固酮"逃逸"现象
值得一提的是,临床研究发现即使在ACEI/ARB治疗的心衰患者中,约30%-40%的患者会出现"醛固酮逃逸"现象——即初期醛固酮水平下降后再次升高。这种现象部分解释了为什么在ACEI/ARB基础上加用MRA能带来额外获益。
三、MRA在心衰治疗中的临床应用
3.1 适应证与推荐
根据《中国心力衰竭诊断和治疗指南2024》:
-
HFrEF:对有症状的HFrEF患者,推荐使用MRA降低心衰死亡率和住院率,除非有禁忌证或不能耐受(I类推荐,A级证据)
-
HFmrEF:可考虑应用MRA降低心衰住院风险和心血管死亡(IIb类推荐,B级证据)
-
HFpEF:可考虑在特定HFpEF患者中(LVEF<55%-60%,BNP升高或1年内因心衰住院)使用MRA以降低住院风险(IIb类推荐,B级证据)
3.2 禁忌证与注意事项
禁忌证:
-
肌酐>221 μmol/L(2.5 mg/dl)或eGFR<30 ml·min⁻¹·1.73 m⁻²
-
血钾>5.0 mmol/L
-
妊娠妇女
用法用量:
-
螺内酯:初始剂量10-20 mg,1次/d,至少观察2周后再加量,目标剂量20-40 mg,1次/d
-
依普利酮:初始剂量25 mg,1次/d,目标剂量50 mg,1次/d
笔者心得:MRA与襻利尿剂合用便不需要再同时补钾,除非有低钾血症。临床中常见的是同时使用螺内酯与口服钾剂,对于肾功能正常的患者,应谨慎评估是否有此必要,以避免高钾血症风险。
3.3 不良反应监测与处理
定期监测:
-
使用MRA治疗后3天和1周应监测血钾和肾功能
-
前3个月每月监测1次,以后每3个月1次
不良反应处理:
-
肾功能恶化和高钾血症:
-
血钾>5.5 mmol/L或eGFR<30 ml·min⁻¹·1.73 m⁻²应减量并密切观察
-
血钾>6.0 mmol/L或eGFR<20 ml·min⁻¹·1.73 m⁻²应停用
-
内分泌不良反应:
-
螺内酯导致的男性乳房发育(发生率约10%),大多可逆
-
必要时可减量、停药或改用依普利酮
-
停药后不能自愈者可考虑他莫昔芬等药物治疗
四、MRA在心衰综合管理中的地位
4.1 与四联疗法中的其他药物关系
现代心衰治疗已从传统的"金三角"(ACEI/ARB、β受体阻滞剂、MRA)发展为"五朵金花"(ARNI/ACEI/ARB、β受体阻滞剂、MRA、SGLT2i、sGC刺激剂)。研究表明,使用四联药物治疗可使HFrEF患者全因死亡率降低73%。
在这一治疗框架下,MRA的应用注意要点:
-
与ARNI/ACEI/ARB合用时需密切监测高钾风险
-
与SGLT2i合用时注意同时使用可能带来的血容量变化
-
在优化利尿剂治疗的基础上应用,避免脱水和低血压
4.2 启动时机与顺序
对于慢性HFrEF患者:
-
在收缩压≥100 mmHg时,可小剂量同时启动新四联药物
-
对于不能耐受同时启动的患者,可先启动1-2类,逐步添加
-
对已接受ARNI/ACEI/ARB、SGLT2i、BB治疗的患者,如血钾<5.0 mmol/L,eGFR≥30 ml·min⁻¹·1.73 m⁻²,可加用MRA
对于急性心衰患者:
-
血流动力学稳定后尽早启动或在出院前应启动MRA

4.3 中国特色:MRA使用现状与问题
中国心衰中心注册研究指出,我国心衰患者MRA使用率较高,可能与临床医生把MRA作为保钾利尿剂使用有关。这种现象提示我们需要更加规范MRA的使用:
-
明确其在改善预后而非单纯利尿中的价值
-
关注目标剂量而非最小有效剂量
-
避免不必要停药,TRED-HF研究显示停用心衰标准治疗药物后约40%患者在6个月内出现心衰复发
笔者心得:对于合并多种疾病的老年心衰患者,药物种类多且复杂时,容易忽略MRA的目标剂量滴定。建议在临床随访中特别关注MRA的剂量优化,并与其他心衰药物一样进行长期随访与管理。
总结
MRA已经从单纯的"保钾利尿剂"成长为心衰治疗的核心药物之一,通过阻断醛固酮及盐皮质激素受体的过度激活,发挥保护心血管、改善预后的重要作用。
根据现有循证医学证据,对于HFrEF患者,MRA应作为基础治疗方案的组成部分;对于特定HFmrEF和HFpEF患者,MRA也可能带来临床获益。在实际应用中,需注意MRA的适应证、禁忌证、用法用量以及不良反应监测与处理,以最大化其临床价值。
未来,随着第三代MRA在更多临床场景的应用和研究,MRA药物家族有望为心衰患者带来更多获益,而更加精准的个体化用药策略也将不断完善。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)