首页 > 医疗资讯/ 正文
肺动脉高压(PAH)是一种以肺动脉压力异常升高为特征的严重疾病,其发病率虽较低,但预后较差,且与肺血管重塑密切相关。流行病学数据显示,虽然特发性肺动脉高压的年发病率较低,但在COPD患者中肺动脉高压的并发率约为20%-50%,左心衰竭患者中肺动脉高压的并发率高达60%-80%。PAH好发于年轻女性,且病情进展迅速,若不及时治疗,患者的中位生存期仅为2.8年。研究证实,PAH患者的心力衰竭、心律失常及猝死风险较普通人群显著升高,是导致患者死亡的主要原因。肺血管重塑是PAH的核心病理机制,表现为血管壁增厚、管腔狭窄及原位血栓形成,进一步加剧肺动脉压力升高和右心功能衰竭。探索肺血管重塑的分子机制(如内皮细胞功能障碍、平滑肌细胞异常增殖及炎症因子激活),对于开发靶向治疗策略具有重要意义。
2025年2月25日,陆军军医大学第二附属医院呼吸科范晔团队在Circulation Research杂志(中科院1区,5年影响因子16.5)发表了题为“ASH2L Deficiency in Smooth Muscle Drives Pulmonary Vascular Remodeling”的论文。该研究系统阐明了ASH2L调控肺动脉高压肺血管重塑的分子机制,为肺动脉高压的靶向治疗提供了新策略。

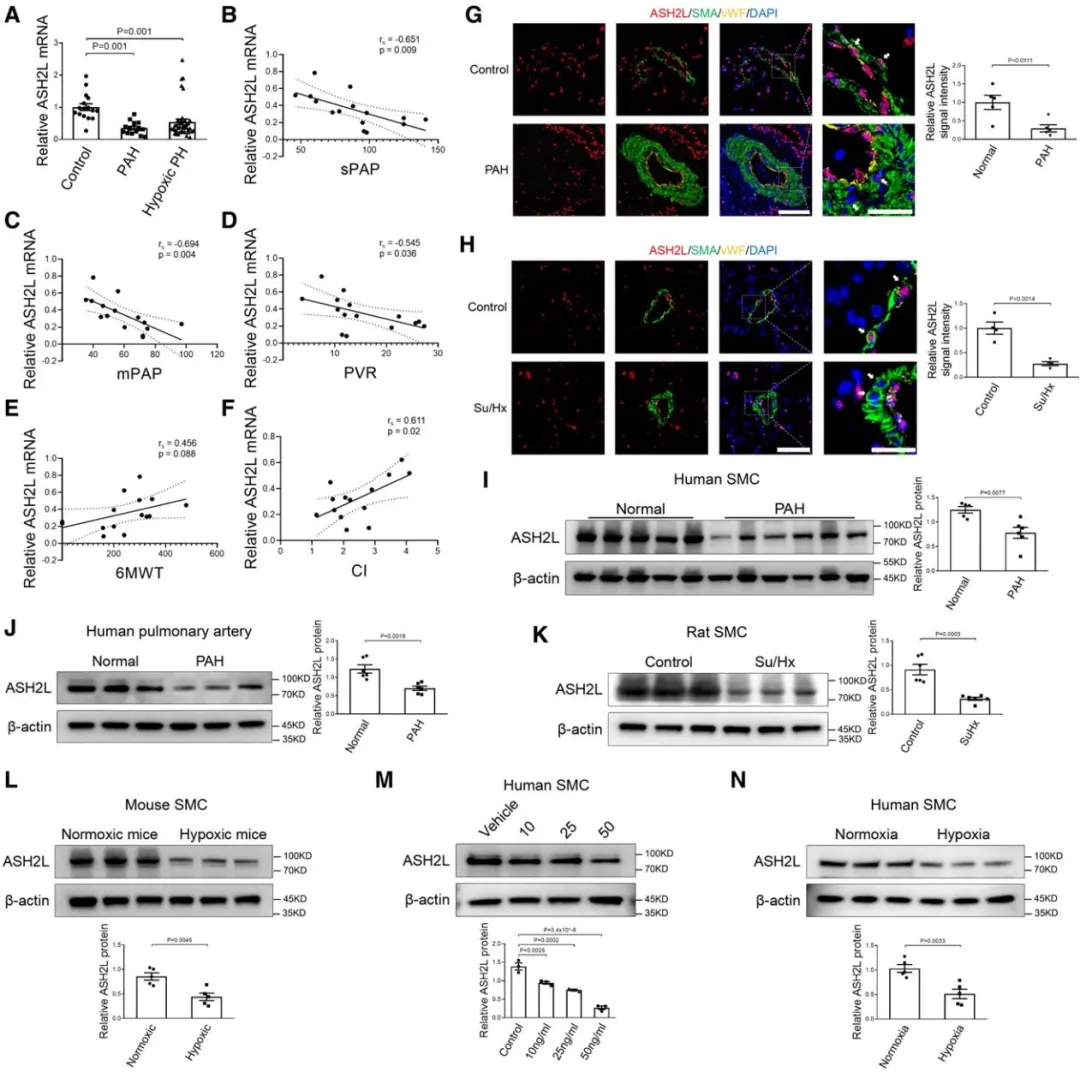
首先,课题组通过分析肺动脉高压病人肺血管与对照组转录组数据发现,PAH患者中ASH2L的表达量的高低与sPAP、mPAP、PVR、6MWT等存在相关性,且进一步在疾病动物模型的肺血管组织及细胞中进一步验证ASH2L在平滑肌细胞表达显著下降,提示ASH2L可能通过调控平滑肌细胞的表型参与肺动脉高压肺血管重塑的病理进程。该现象进一步在细胞水平得到验证。
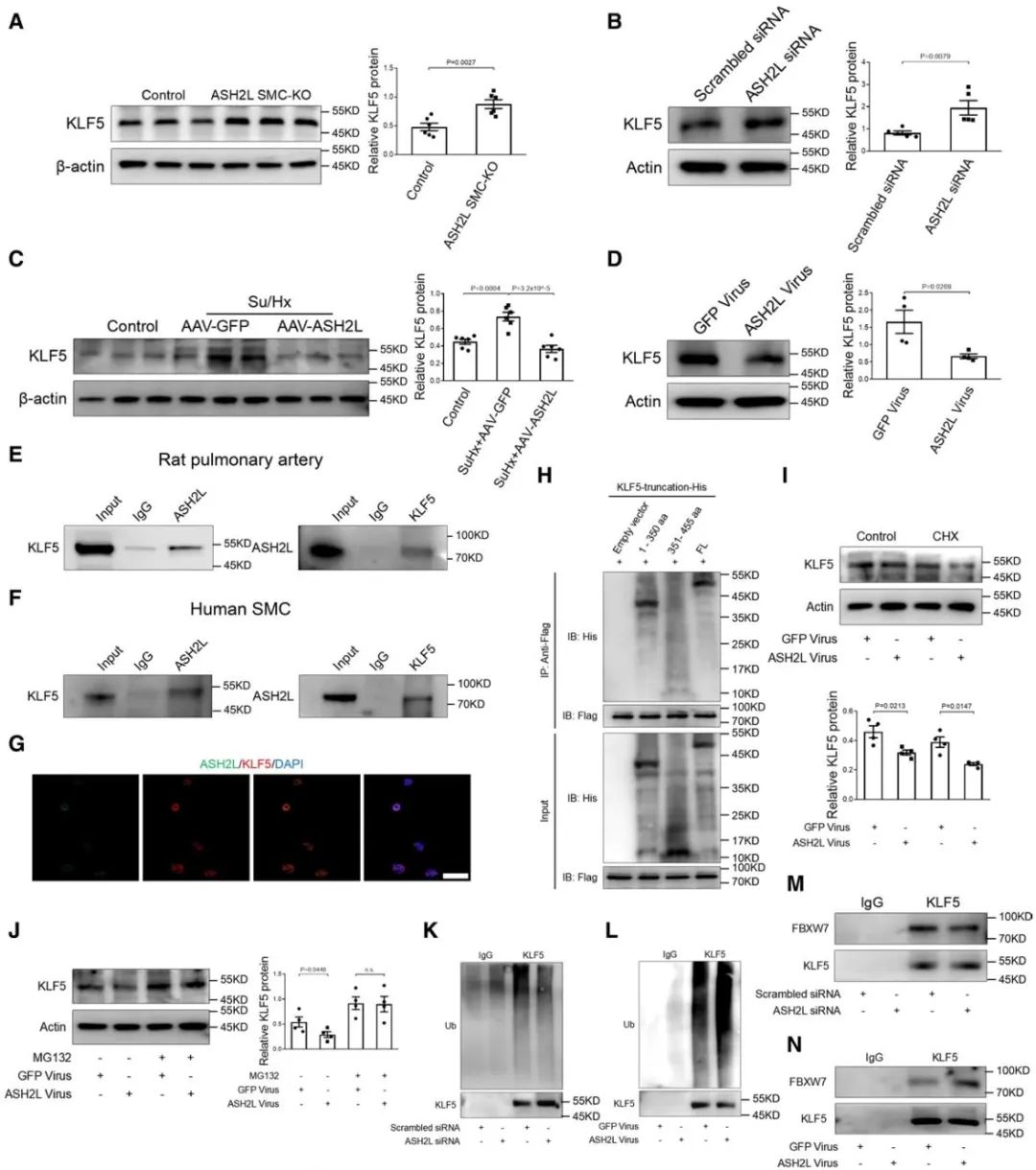
机制研究揭示,生物信息学预测结合实验验证发现ASH2L可以与平滑肌细胞中表型变化密切相关的转录因子KLF5相互结合,并通过促进KLF5的泛素化加速KLF5蛋白的降解。进一步对该机制做深入探索发现,作为KLF5的E3泛素连接酶-FBXW7,ASH2L可以影响KLF5的E3泛素连接酶-FBXW7与KLF5的结合以调控KLF5在血管平滑肌细胞中的表达。本研究利用western blot、免疫荧光及免疫共沉淀(Co-IP)、染色质免疫沉淀(ChIP)等技术证实,ASH2L通过结合KLF5的1-350aa区域,促进KLF5蛋白的泛素化进程进而影响KLF5与notch3启动子区的结合。
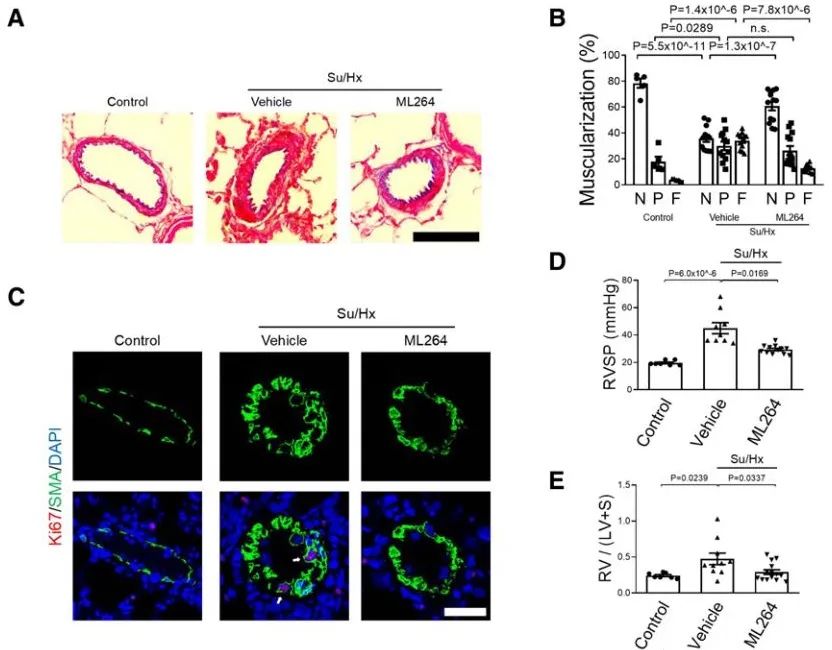
最后,在体研究表明,通过对大鼠肺血管平滑肌组织特异性过表达ASH2L,以及在小鼠模型中使用KLF5的抑制剂均表现出对肺血管重塑表型的显著缓解。

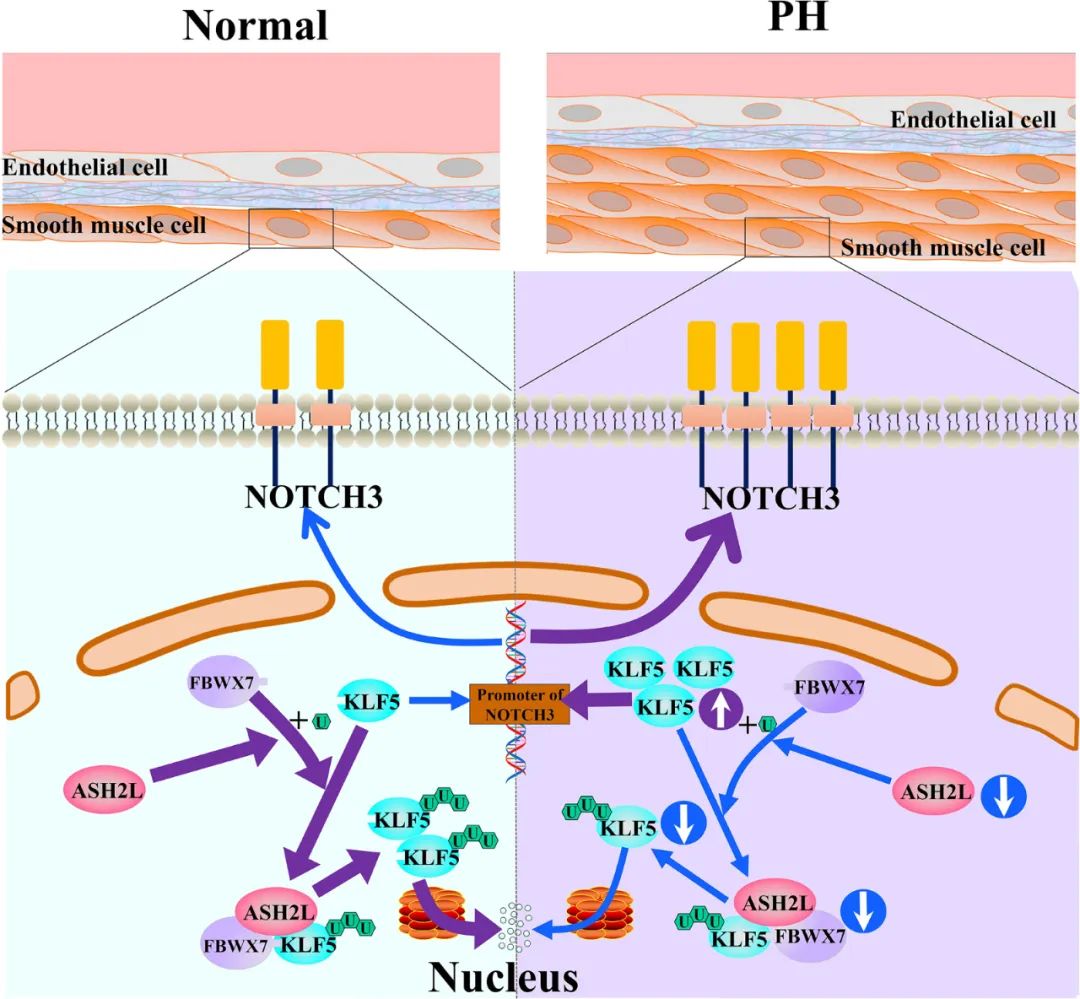
肺血管重塑作为肺动脉高压发生的核心环节,对于其机制的深入探索有助于推动该病的完善治疗。本研究首次发现ASH2L非组蛋白甲基化依赖途径调控肺动脉高压肺血管重塑的作用机制,系统性地解释了ASH2L对KLF5独特的蛋白降解调节机制。这一发现拓宽了对肺动脉高压发病机制的理解,同时为肺动脉高压的防筛诊治康提供了新的思路和靶点。
陆军军医大学第二附属医院呼吸科范晔教授、陆军军医大学第三附属医院高血压内分泌科祝之明教授及无锡市人民医院重症医学科王大鹏教授为该文的通讯作者,陆军军医大学第二附属医院呼吸科张静副研究员为该文的第一作者,陆军军医大学第二附属医院为该文的第一和通讯作者单位。本研究得到了香港城市大学生物医学系黄聿教授的大力指导,并获得了国家自然科学基金和重庆市自然科学基金的资助。
文章链接:
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.124.325539
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)