首页 > 医疗资讯/ 正文
主动脉夹层/动脉瘤(AAD)是一种严重且危及生命的疾病,其特点是缺乏有效的药物治疗。基因疗法已成为治疗AAD的一种有前途的方法。然而,基因治疗的临床应用受到重大挑战的阻碍,包括当前医疗实践中创新基因药物的稀缺以及缺乏简化的基因药物递送机制。此研究集中在一个独特的基因靶点tRF-Gly-CCC上,它属于小分子非编码tsRNA,对维持血管平滑肌细胞功能和调节炎症细胞反应至关重要。但是在体内如何将基因药物递送到AAD病灶部位,值得研究。
2024年12月9日,青岛大学转化医学研究院于涛/亓洪昭课题组在Journal of controlled release发表了题为“Activated Neutrophil membrane-coated tRF-Gly-CCC nanoparticles for the treatment of aortic disp/aneurysm”的研究论文,开发了一种活化的中性粒细胞膜仿生纳米颗粒(neu MCs),以负载tRF-Gly-CCC的聚合物纳米颗粒为核心,活化的中性粒细胞膜为外层。活化的中性粒细胞膜具有双重功能,即保护tRF-Gly-CCC的稳定和促进靶向递送至AAD位点。

首先,研究者通过临床和动物的血管样本,筛选出了一个差异表达显著的tsRNA,即tRF-Gly-CCC。通过在血管平滑肌细胞和巨噬细胞中过表达tRF-Gly-CCC,发现能够维持血管平滑肌细胞的收缩表型,抑制MMPs的分泌。此外还能够降低巨噬细胞中IL-1β和IL-6的表达。
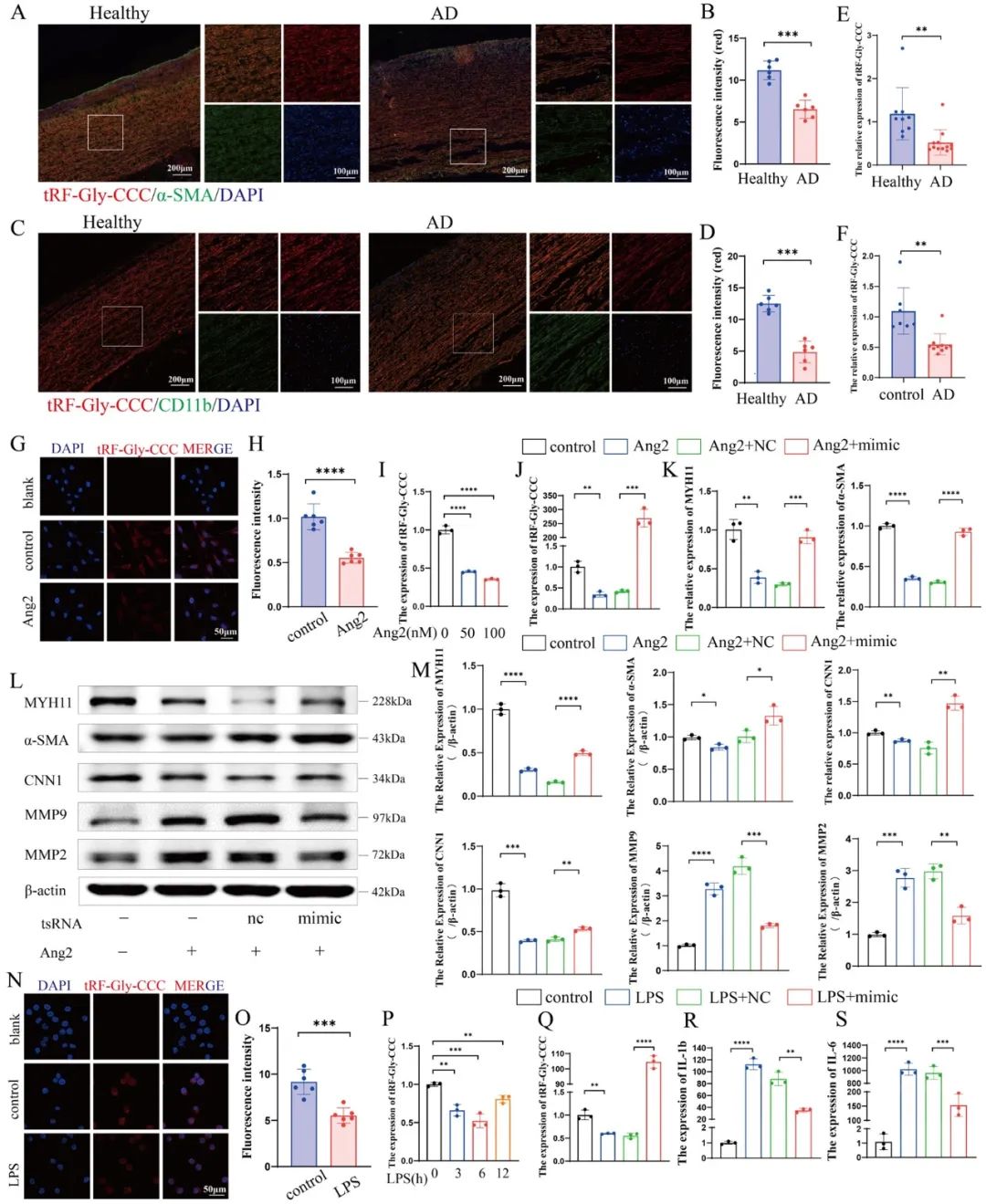
为了将其递送至AAD病灶部位,研究者从患者的血液中提取了活化的中性粒细胞,并将其包被在以tRF-Gly-CCC为基础的纳米颗粒外层,制作了neu MCs,并对neu MCs的负载能力以及粒径、表面电位等做了一系列的表征。在细胞中,活化的neu MCs的递送效率远高于未活化的neu MCs,并且也显示出与tRF-Gly-CCC转染一致的保护效果。
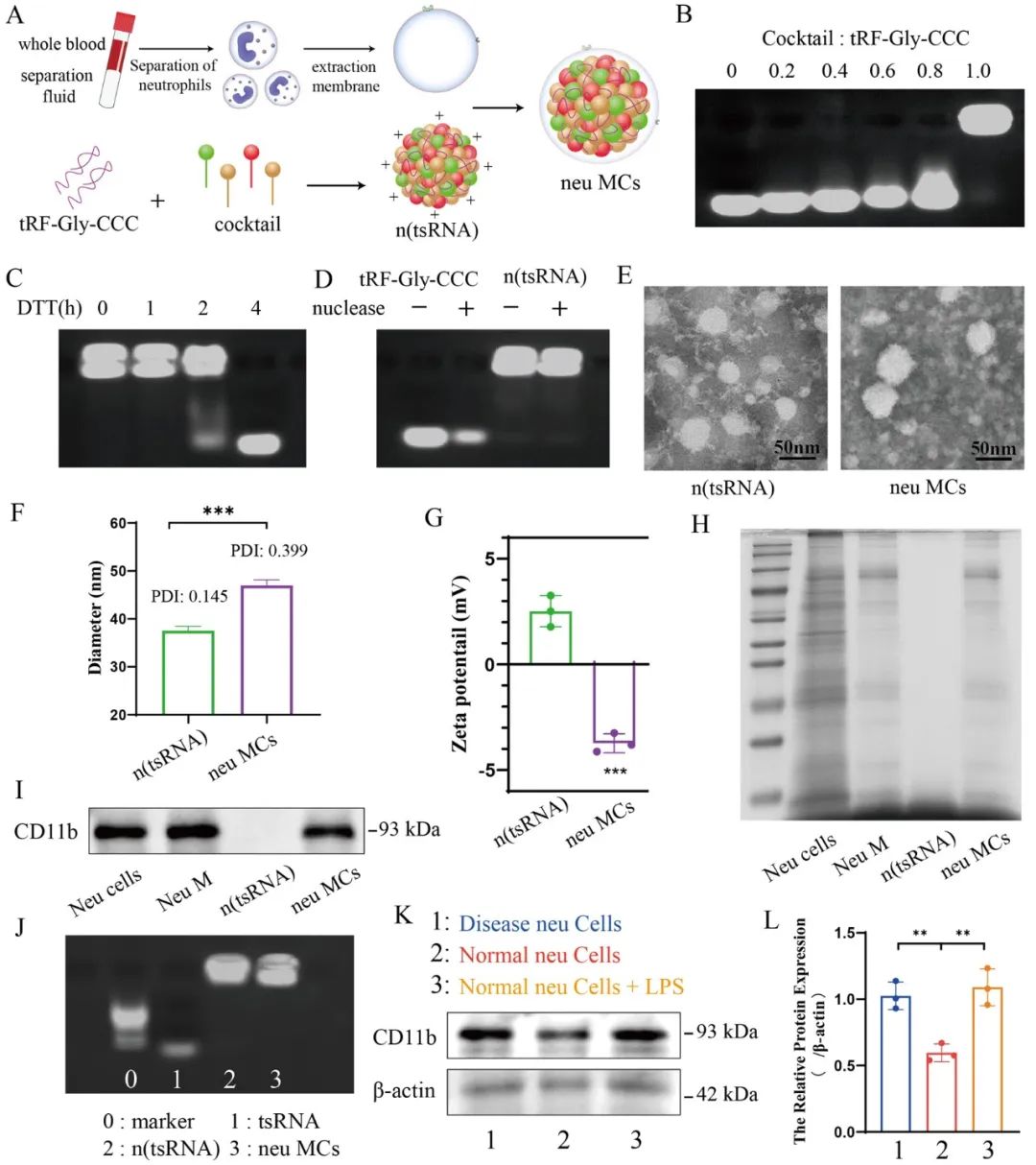
进一步的实验结果显示,相对于n(tsRNA),neu MCs能够在血液循环中更加稳定,向AAD病灶部位富集作用也更强。最后,体内实验结果显示,neu MCs对于AAD有着显著的治疗效果,显著降低了AAD的发生率、小鼠死亡率以及主动脉的管径。分子生物学实验结果显示,neu MCs对于维持血管平滑肌的收缩表型以及一些关键因子的表达有着显著的效果,并且neu MCs非常安全,无明显的毒副作用。
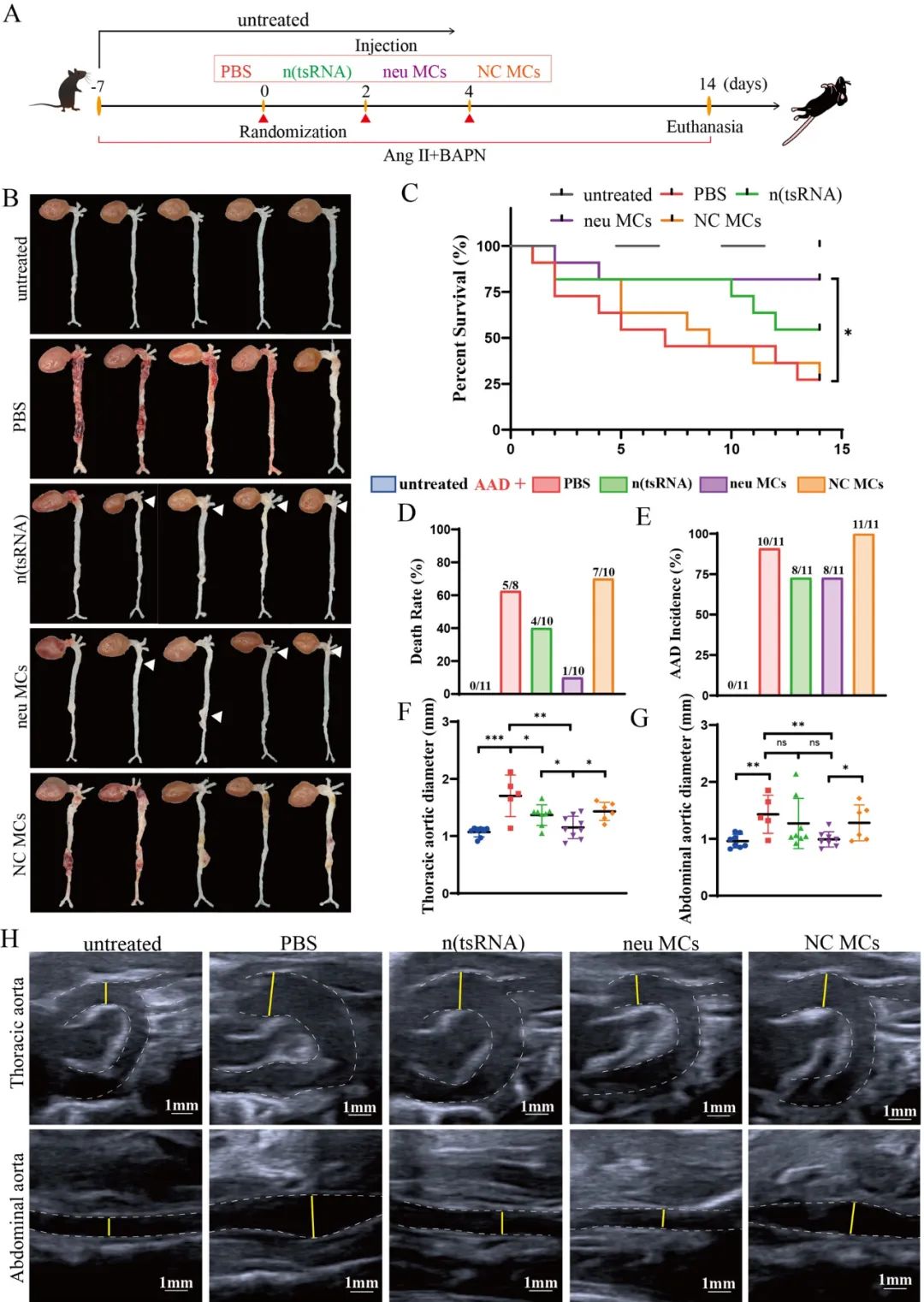
综上,本研究发现了一个新的AAD治疗靶点tRF-Gly-CCC。在此基础上,研究者构建中性粒细胞膜仿生纳米颗粒neu MCs,实现了基因药物的体内递送,减少了小鼠的AAD死亡率。
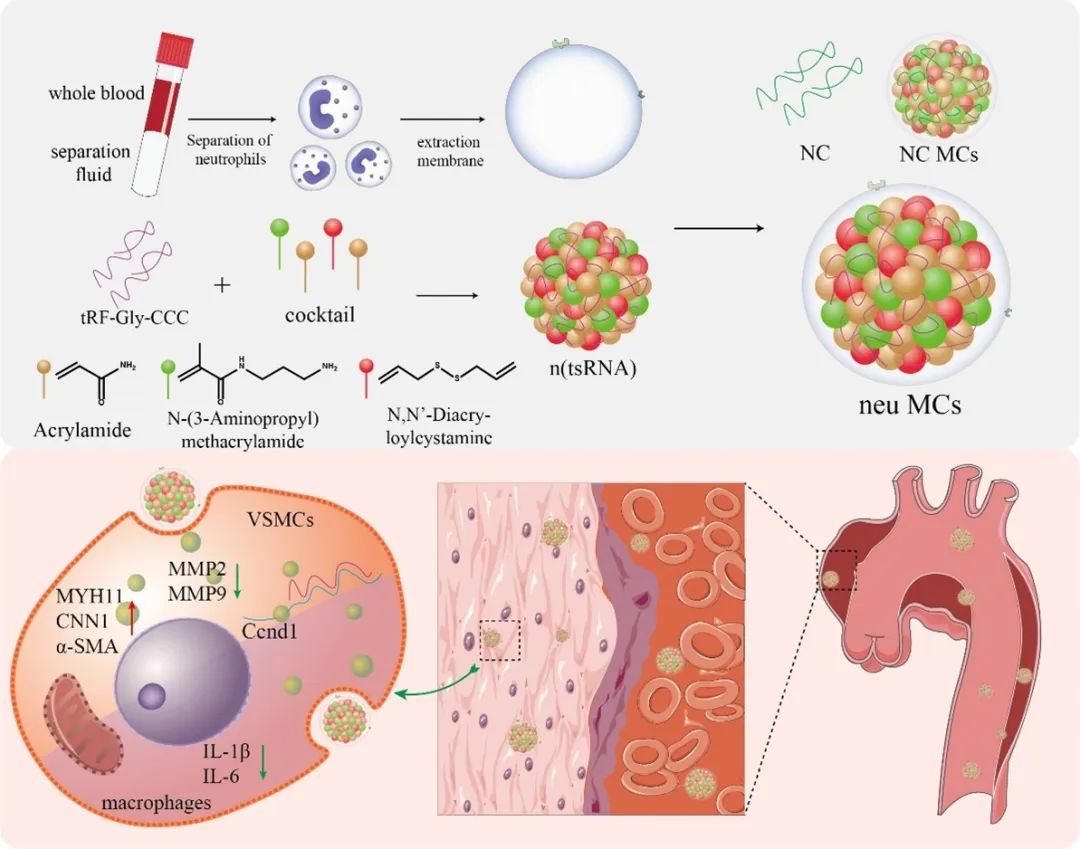
本文的共同第一作者是青岛大学转化医学研究院硕士研究生李天翔和基础医学院杨艳艳副教授,通讯作者为青岛大学转化医学研究院再生医学中心于涛教授和亓洪昭教授。该研究得到了国家自然科学基金(No.82270442, 82370425)和山东省自然科学基金(ZR2022MH027)的资助。
原文链接:
https://doi.org/10.1016/j.jconrel.2024.12.015
猜你喜欢
- BMC Oral Health:成年女性创伤性上颌中切牙撕脱伴双颌牙槽突的正畸治疗1例
- Chin Med:针刺可改善餐后不适综合征患者的症状、血清胃饥饿素和自主神经系统:一项随机对照试验
- 这个麻醉意外,医患双方“两败俱伤”
- 问诊分析:这一跤摔得好,摔出个囊腔型早期肺癌!
- 安贞医院周玉杰领衔:强效降压25.2 mmHg!微创手术有望为中国高血压患者带来新选择
- 一药双效!JAMA超10万人研究发现,疱疹疫苗可能帮你远离痴呆
- 广东疫情信息发布侧记:发言者未戴口罩背后有“隐情”
- JAHA:血压和心率变异性对妊娠结局的影响
- J Int Soc Prev Community Dent:瑜伽竟可以促进口腔健康?
- 牛皮癣严重时可出现残毁畸形
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)