首页 > 医疗资讯/ 正文
BCMA CAR-T双相扩增
BCMA CAR-T细胞疗法显著改善了复发或难治性多发性骨髓瘤(RRMM)的治疗,其主要毒性一般为细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)、免疫效应细胞相关血液毒性(ICAHT)和感染等,而双相CAR-T细胞在体内扩增的罕见现象及其相关的严重毒性尚未系统描述和研究。
近日中国医学科学院血液病医院(中国医学科学院血液学研究所)安刚教授团队于《Journal for ImmunoTherapy of Cancer》发文,报告了BCMA CAR-T后一例罕见的双相CAR-T扩增及其诱导的免疫效应细胞相关噬血细胞性淋巴组织细胞增生症样综合征(IEC-HS)和严重的多微生物感染;为了深入了解潜在的免疫动态,作者还使用高维光谱流式细胞术(SFC)阐明两个扩增峰时免疫细胞成分和功能的变化。第一作者为严文强熊玉、吕瑞医生,通讯作者为安刚教授。

研究结果
患者经过6个周期的D-Pd治疗后达到严格意义的完全缓解(sCR)和微小残留病(MRD)阴性(NGS,灵敏度10-6)。由于多次干细胞动员失败而接受来那度胺的维持治疗和定期随访,经过1年的维持治疗后患者选择BCMA CAR-T维持缓解。清淋化疗前的IgG为11.5g/L。
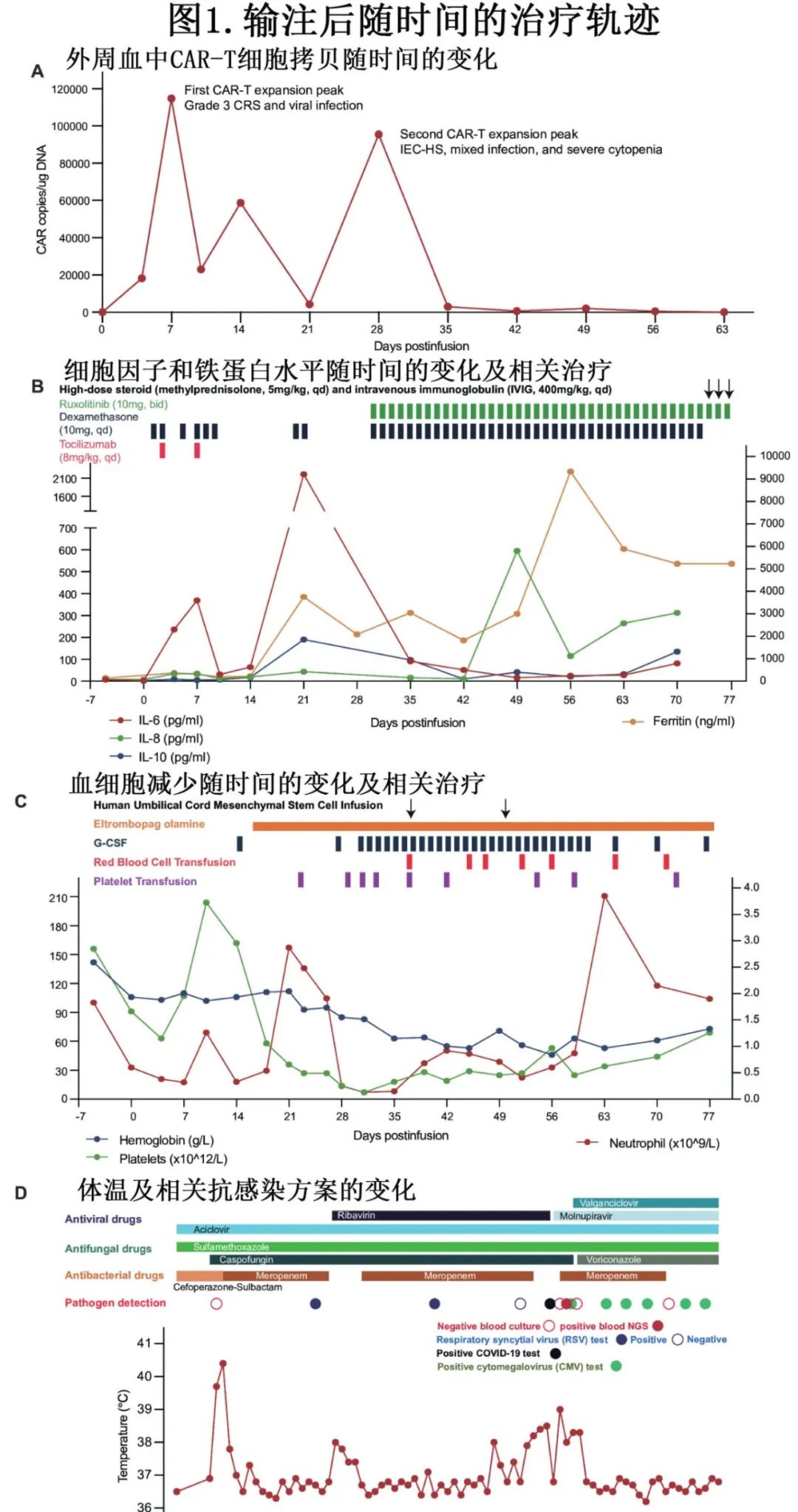
患者于2024年1月16日接受标准Fc(氟达拉滨40mg,环磷酰胺400 mg,第5天至第3天)清淋预处理,并接受学术性CAR-T输注,剂量为6×106/kg。输注后CAR-T细胞在第7天出现初始扩增高峰,随后逐渐下降(图1A)。患者出现3级CRS,第0天出现高热和寒战,第3天出现低血压;症状在托珠单抗、地塞米松和血管加压药物治疗后第7天消失(图1B)。在此期间,患者出现4级中性粒细胞减少症,给予粒细胞集落刺激因子(G-CSF)治疗(图1C)。到第21天,中性粒细胞水平恢复到接近正常,但血小板迅速显著下降;实验室检测显示铁蛋白、乳酸脱氢酶、白介素-6 (IL-6)、白介素-10 (IL-10)、丙氨酸转氨酶和天冬氨酸转氨酶升高,纤维蛋白原下降(图1B)。骨髓涂片证实存在噬血细胞。患者符合HLH-2004标准中的5项,H评分为215,确诊为免疫效应细胞相关噬血细胞性淋巴组织细胞增生症样综合征(IEC-HS)。胸部CT扫描显示双肺间质增厚和新的多发磨玻璃影,主要位于胸膜下区域,随后结合呼吸道合胞病毒PCR检测阳性证实为病毒感染。在此期间观察到外周血CAR-T细胞水平的第二个延迟峰值(图1A)。给予G-CSF、艾曲泊帕、芦可替尼和糖皮质激素治疗但未显著改善。考虑到患者的难治性血细胞减少症和高炎症状态,两次输注人脐带间充质干细胞(MSC,4×10⁷,每次40 mL)。中性粒细胞水平逐渐改善,但血红蛋白和血小板水平仍依赖于频繁输血(图1C)。第49天,尽管多次抗感染治疗,患者再次出现复发性高热,IL-8和铁蛋白升高(图1B和D)。常见病原检查发现COVID-19和巨细胞病毒(CMV)感染。外周血二代测序(NGS)检测显示多种病原体,包括空肠弯曲杆菌、粪肠球菌、黄曲霉、热带念珠菌、巨细胞病毒和人疱疹病毒6B,表明细菌、真菌和病毒混合感染。给予美罗培南、磺胺甲恶唑、伏立康唑、阿昔洛韦、莫诺拉韦和缬更昔洛韦联合抗感染治疗。患者体温恢复正常,但炎症状态和血细胞减少症持续存在(图1B和D)。第56天时,患者处于深度缓解(MRD阴性和sCR)。到第70天,患者出现神经系统症状,包括视力障碍、下肢无力和手指不灵活,检查显示双侧巴宾斯基征(babinski's sign)阳性。脑部MRI示脱髓鞘样改变,腰椎穿刺显示脑脊液无色,微白蛋白水平轻微升高。流式细胞术未检测到肿瘤细胞,但脑脊液NGS检测到CMV 1212拷贝。给予大剂量类固醇和免疫球蛋白休克治疗,但未明显改善。患者最终选择停止治疗,并于第94天在院外去世。
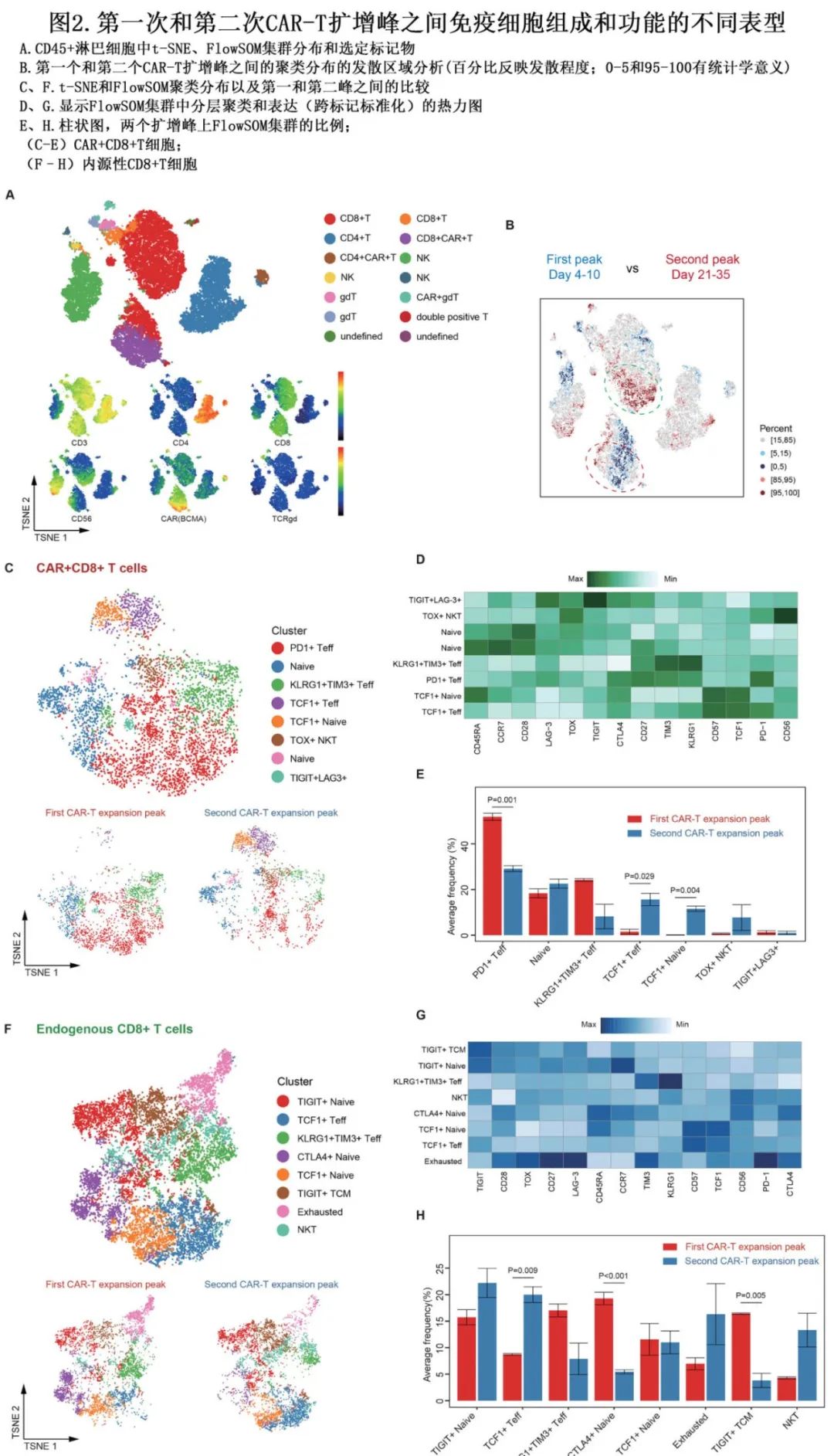
通过流式细胞术在两个CAR-T扩增峰鉴定出不同的T细胞成分
为了阐明双相CAR-T扩增峰的潜在机制,对两个扩增峰(第4-10天和第21-35天)采集的外周血样本进行了33色光谱流式细胞术检测,以表征免疫细胞组成和功能的变化。利用计算机驱动的FlowSOM对细胞类型标记(CD3、CD8、CD4、CD56、BCMA-CAR、TCRγδ)进行聚类,从CD45+淋巴细胞中鉴定出15个集群,主要对应于经典的NK/T谱系(CD8+T细胞、CD4+T细胞、γδT细胞、NK细胞、CAR+T细胞)(图2A)。第一个和第二个扩增峰之间的差异分析显示,主要差异在于内源性CD8+T和CAR+CD8+T群(图2B)。使用T分布随机近邻嵌入(t-SNE)和FlowSOM算法进一步分析了两个集群的特征,将激活/记忆T细胞标记物和检查点受体作为变量。在CAR+CD8+ T细胞中确定了8个集群,每个集群表达不同水平的检查点并表现出不同的功能(图2C-D)。比较两个扩增峰后发现,PD-1+ T效应细胞是第一个扩增峰的主要成分,而第二个CAR-T扩增峰中TCF1+T效应细胞/Naïve集群显著更高(p<0.05,图2E)。对于内源性CD8+T成分,使用t-SNE和FlowSOM算法确定了另外8个具有不同表达水平的相关标记的集群(图2F-G)。与CAR+CD8+ T细胞相似,TCF1+Teff组在延迟的第二个扩增峰期间,在内源性CD8+T细胞群中所占比例高于第一个扩增峰(p=0.009,图2H)。与之相反,早期T细胞集群(包括CTLA-4+ Naïve和TIGIT+T中央记忆组)在第一个峰值时明显更频繁(p<0.05,图2H)。
总结
该患者在CAR-T细胞输注后出现罕见的双相CAR-T扩增模式,导致复杂的免疫效应细胞相关毒性,包括CRS、ICAHT、IEC-HS和致命的混合感染。尽管给予现行的标准治疗,但未解决这些不良反应,最终导致患者死亡。
该病例报告强调了罕见双相CAR-T扩增现象,描述了BCMA CAR-T治疗后相关的免疫细胞动力学,并证实脐带MSC输注可以有效改善高级别ICAHT。该病例为双相CAR-T扩增和相关的免疫效应细胞相关毒性提供了新的见解。
参考文献
Yan W, Xiong Y, Lv R, et al. Uncommon biphasic CAR-T expansion induces hemophagocytic lymphohistiocytosis-like syndrome and fatal multiple infections following BCMA CAR-T cell therapy: a case report. Journal for ImmunoTherapy of Cancer 2024;12:e010080. doi:10.1136/ jitc-2024-010080
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)