首页 > 医疗资讯/ 正文
免疫检查点阻断(ICB)对胶质母细胞瘤(GBM)的免疫治疗来说是一种潜在的方法,但其临床疗效受到血液肿瘤屏障(BTB)和免疫抑制肿瘤微环境的严重挑战。
有鉴于此,东南大学居胜红教授、Jinbing Xie和新加坡国立大学陈小元教授等人通过共包封方法,将抗程序性死亡配体1抗体(aPD-L1)加载到氧化还原响应性胶束中,并通过紫杉醇(PTX)诱导的免疫原性细胞死亡(ICD)进一步放大ICB效力,以重振局部抗GBM免疫反应。该胶束可穿过BTB并保留在还原性肿瘤微环境中,而不会改变aPD-L1的生物活性。aPD-L1和PTX联合抑制了原发性和复发性GBM,积累了细胞毒性T淋巴细胞,并在原位携带GBM的小鼠中诱导持久免疫记忆,从而增强了ICB的疗效。该研究认为,促进有效抗体递送并与化疗药物诱导的ICD结合的共包封方法表明,化学免疫疗法可能会重新编程局部免疫,以增强针对GBM的免疫疗法。相关工作以“Redox-responsive polymer micelles co-encapsulating immune checkpoint inhibitors and chemotherapeutic agents for glioblastoma therapy”为题发表在Nature Communications。

【文章要点】
该研究首先通过流式细胞术确定了多种胶质瘤细胞系都具有显著的PD-L1表达,为在GBM中使用抗PD-L1疗法提供了支持。而为了将aPD-L1和PTX整合到单个胶束中,作者还设计了angiopep2-aPD-L1@PTX纳米胶束(A2-APM)。如图1所示,为了构建A2-APM,作者首先将抗体、马来酰亚胺聚乙二醇多聚L-赖氨酸(Mal-PEG-PLL)和2-[(2-[(4-琥珀酰亚胺)羰基]氧乙基)二硫基]乙基-4-琥珀酰胺基碳酸酯[记为SC-(CH2)2-S-S-(CH2)2-SC]进行共价偶联。然后,Mal-PEG-PLL通过静电相互作用包封带负电荷的PTX以产生PTX共负载的胶束,并通过点击反应进一步将马来酰亚胺片段与血管肽-2肽(angiopep-2 peptide,A2)进行结合。
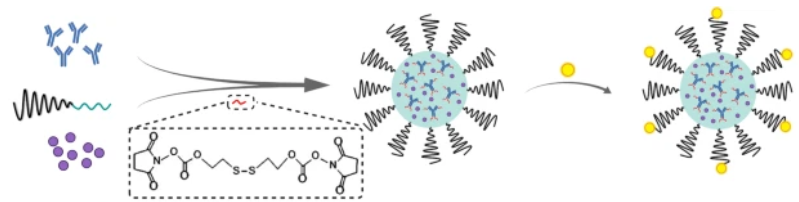
图1 A2-APM
修饰在胶束表面的靶向A2肽可以进行BTB渗透,而GBM的还原型微环境则可裂解交联链并触发aPD-L1从胶束中的释放,同时又不会改变其结构和功能,这进一步提高了ICB的GBM选择性。同时,胶束的解离加速了PTX在肿瘤微环境中的释放。快速释放的PTX不仅对GBM细胞表现出优异的抑制特性,而且通过诱导ICD促进ICB治疗,使肿瘤对PD-1/PD-L1阻断敏感(图2)。本研究旨在提供一种适用的化学免疫治疗方法,以生物安全有效的方式解决ICB治疗脑恶性肿瘤的局限性。
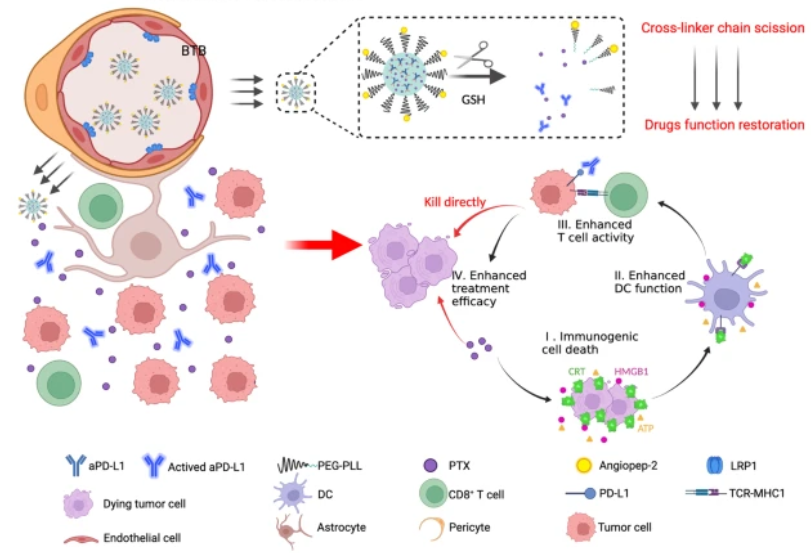
图2 抗肿瘤治疗示意图
原文链接:
https://www.nature.com/articles/s41467-024-44963-3
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)