首页 > 医疗资讯/ 正文
抗体-药物偶联物 (ADC)由linker、payload、单克隆抗体 (mAb) 组成。它结合了高特异性靶向能力和强效杀伤作用的优势,实现了对癌细胞的精准高效杀灭,已成为抗癌药物研发的热点之一。自第一个 ADC 药物Mylotarg ®于2000年获得FDA批准以来,截至2021 年 12 月全球共有 14 款 ADC 药物获批用于血液系统恶性肿瘤和实体瘤,此外,目前还有100多个ADC候选者处于临床试验的不同阶段。
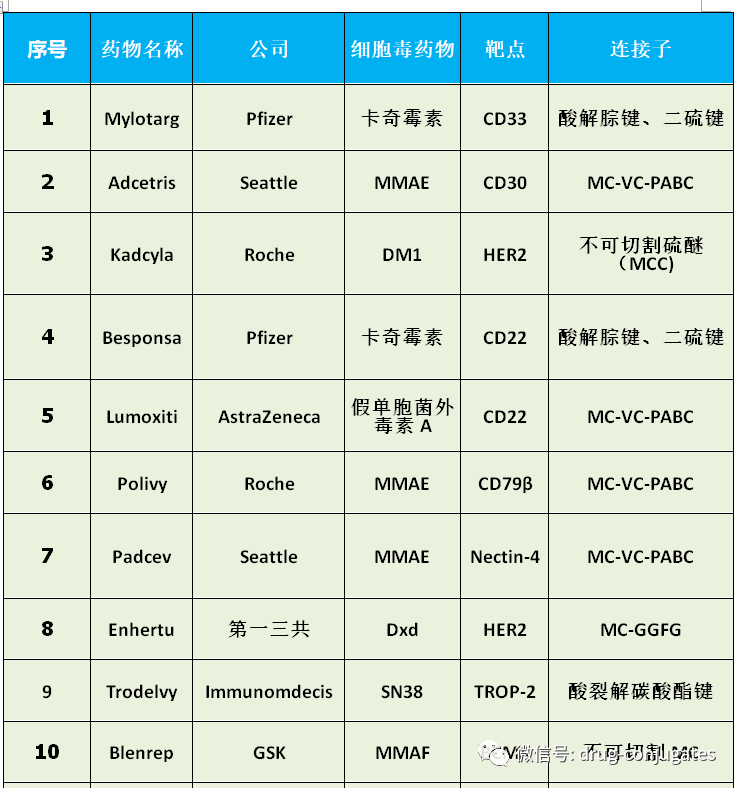
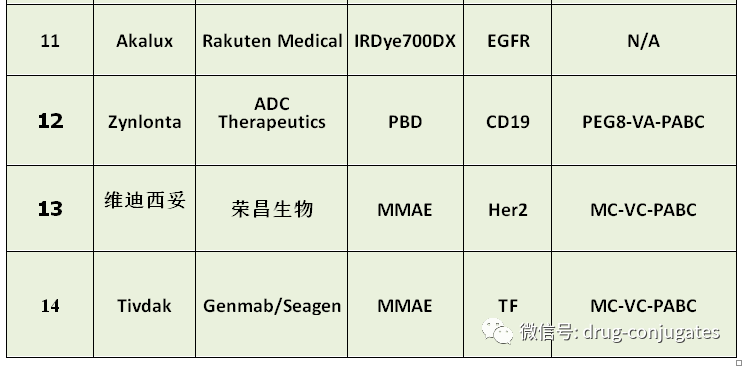
2021 年美国有 34,130 人死于前列腺癌 (PCa)。目前针对难治性转移性前列腺癌、可用治疗选择有限,预后较差。抗体-药物偶联物 (ADC) 在Pca的进展还不尽如人意!
已获批的用于治疗前列腺癌的ADC药物
177Lu-PSMA-617 (Pluvicto : 诺华 )
2022年3月23日,诺华(Novartis)宣布,美国FDA已经批准该公司的靶向放射性配体疗法Pluvicto(lutetium Lu 177 vipivotide tetraxetan,177Lu-PSMA-617)上市,用于治疗前列腺特异性膜抗原(PSMA)阳性的、经治疗进展的去势抵抗前列腺癌(mCRPC)患者。Pluvicto此次获批是依据三期临床VISION的数据,治疗总缓解率(ORR)为30%,其中完全缓解率(CR)为6%,治疗降低38%的死亡风险。Pluvicto是全球首个获批的以PSMA为靶点的治疗性药物(PS:诺华的多肽核素偶联物应该算PDC)。
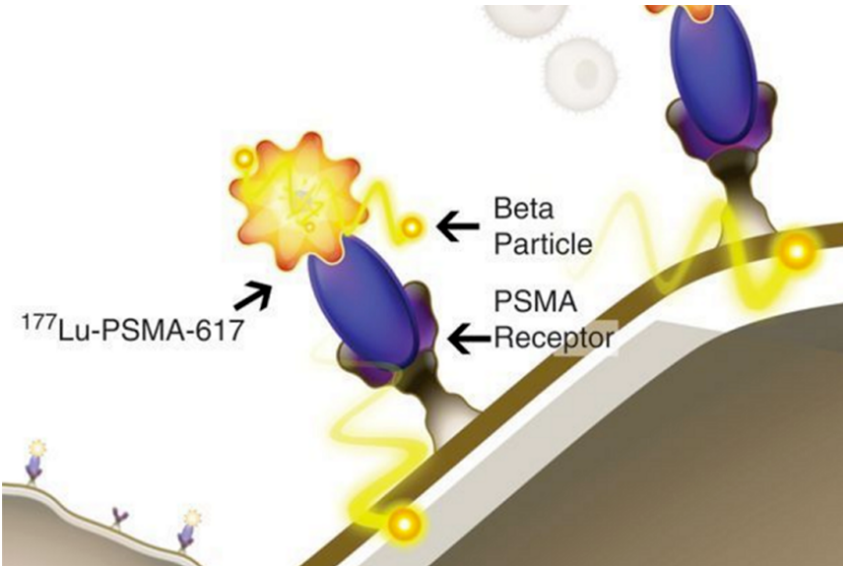
迄今为止,还没有 ADC 被批准用于前列腺癌 (PCa)的ADC,下面就来看看 ADC 在前列腺癌中的靶点和全球的临床试验进展。
抗体-药物偶联物 (ADC) 结构
ADC由抗体、有效载荷和化学接头组成。理想的 ADC 药物在血液循环中保持稳定,精准到达治疗目标,并最终在目标附近(例如癌细胞)释放细胞毒性有效载荷。每个要素都会影响 ADC 的最终疗效和安全性,总体而言,ADC 开发需要考虑所有这些关键组成部分,包括靶点、抗体、细胞毒有效载荷、接头以及偶联方法的选择。
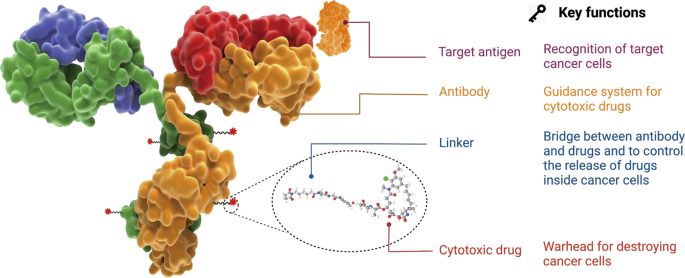
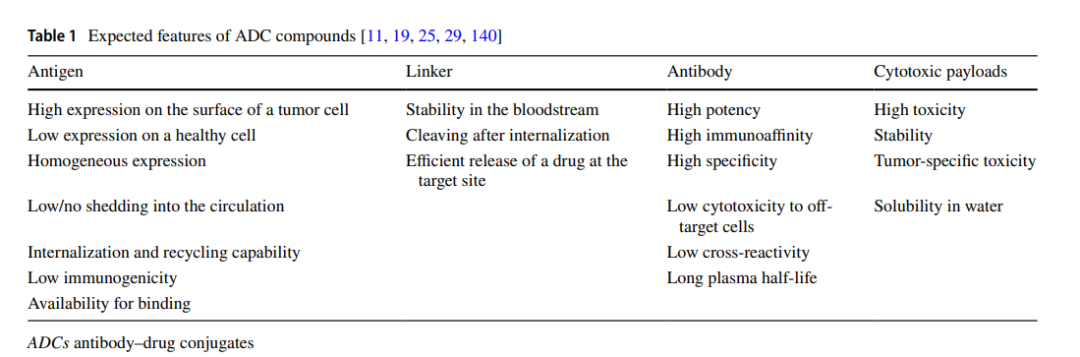
ADC结构及关键要素
靶向前列腺癌的ADC靶点及临床进展
雄激素剥夺疗法(ADT)是前列腺癌 (PCa)治疗重要疗法。然而,特别是对于去势抵抗性疾病,治疗选择还包括化学疗法、抗雄激素疗法、放射性同位素疗法、基因靶向疗法、免疫检查点抑制剂和自体细胞免疫疗法。
靶向前列腺癌(PCa)的重要靶点包括:包括前列腺特异性膜抗原 (PSMA)、前列腺六跨膜上皮抗原 1 (STEAP-1)、溶质载体家族 44成员4 (SLC44A4)、滋养层细胞表面抗原(Trop-2) 和 B7-H3,下面分别介绍这些靶点的情况及在临床阶段的ADC药物。
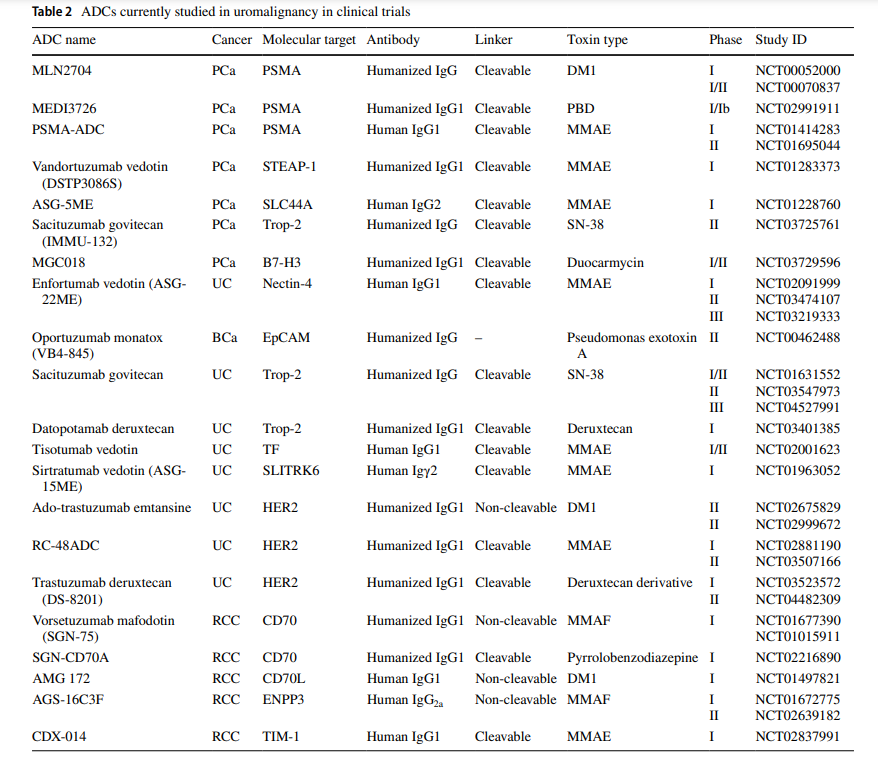
PSMA
PSMA 是一种 II 型跨膜糖蛋白,对前列腺具有高度特异性,具有催化 N-乙酰天冬氨酰谷氨酸水解为谷氨酸和 N-乙酰天冬氨酸的羧肽酶活性。它由一个 19 个氨基酸的内部结构域、一个 24 个氨基酸的跨膜结构域和一个 707 个氨基酸的外部结构域组成。PSMA的FOLH1(叶酸水解酶 1)基因位于 11 号染色体上,其表达受雄激素信号传导的调节。PSMA 的最高表达出现在前列腺上皮细胞表面,而在前列腺外肾近端小管、小肠空肠刷、雪旺细胞和星形胶质细胞内观察到其表达较低。激活后,PSMA 在细胞内迅速内化。
PSMA 水平在 PCa 中比在良性前列腺中高 1000 倍,并且在雄激素剥夺和抗雄激素治疗期间增加。此外,PSMA 在肿瘤相关的新血管系统中表达。临床前 PCa 研究表明,PSMA 通过 MAPK 和 PI3K-AKT 途径参与增殖、迁移和存活。PSMA 表达与肿瘤分期、Gleason 评分、诊断时的前列腺特异性抗原 (PSA)、肿瘤血管生成和原发性 PCa 中的 ERG(红细胞转化特异性相关基因)阴性状态相关;
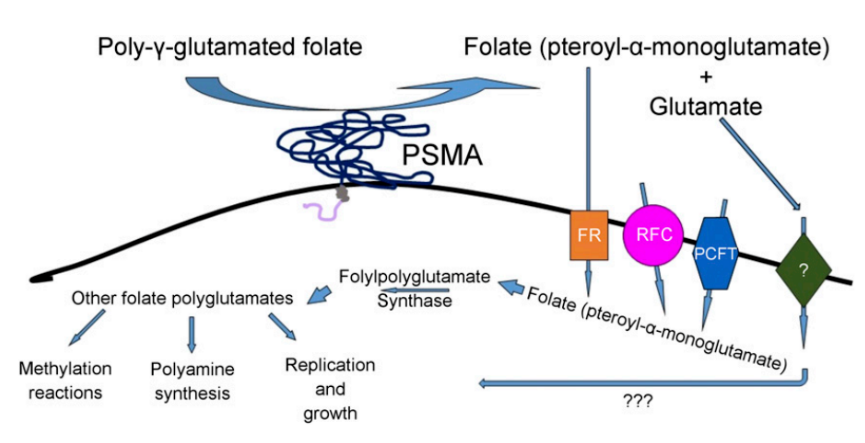
靶向PSMA的ADC临床进展
在临床试验中研究的抗 PSMA ADC 包括 MLN2704、PSMA-ADC MEDI3726。
NCT00052000是一项I期非随机试验,旨在评估MLN2704的剂量限制毒性(DLT)、最大耐受剂量(MTD)和药代动力学。该研究招募了 23 名激素治疗失败的 mCRPC 患者。使用传统的 3 + 3 剂量递增方案,剂量范围在 18 - 342 mg/m2.最常见的 CTC 1-2 级 AE 包括疲劳 (65%)、恶心 (56%) 和腹泻 (39%)。35% 的患者出现神经病变(13% CTC 1 级,22% CTC 2 级)。只有 13% 的患者有 CTC 3 级药物相关毒性,没有报告 CTC 4 级毒性。没有达到 MTD。最常见的DLT是发热性中性粒细胞减少症。
NCT00070837是基于NCT00052000的积极研究结果进行的临床 I/II 期试验,该试验旨在评估 MLN2704 的剂量、药代动力学、免疫原性和肿瘤反应。共招募了 62 名 mCRPC 患者。剂量范围为 60-462 mg/m2,四种不同的给药方案静脉内给药。周围神经病变是该药物最常见的不良反应,发生在 71% 的入组患者中。在 10% 的病例中,神经病变具有临床意义(CTC 3/4 级)。其他常见的 AE 包括恶心 (61%)、疲劳 (60%)、厌食和腹泻 (39%)。仅在 5 名患者 (8%) 中观察到超过 50% 的 PSA 下降。没有PR 或完全缓解 (CR),35% 的患者实现了疾病稳定 (SD)。
NCT01414283 I 期临床试验为了确认抗 PSMA ADC 在紫杉烷难治性 mCRPC 患者中的作用。建立MTD 是主要终点。该研究招募了 52 名患者,他们接受了 0.4-2.8 mg/kg PSMA ADC 最多四个周期,Q3W。确定了为MTD (2.5 mg/kg)。中性粒细胞减少是剂量限制因素,给药后 2 周达到最低点。大约 50% 的患者获得了有希望的抗肿瘤反应,测量结果为循环肿瘤细胞转化或 PSA 降低。
NCT01695044 II 期试验是 NCT01414283 I 期试验的延续。该试验是一项单臂研究, mCRPC 患者(n= 119)被分为未接受过化疗(n= 35)或多西他赛预处理(n= 84) 组。
NCT02991911 I/Ib 期试验旨在评估 MEDI3726 在对恩杂鲁胺或阿比特龙无反应后在 mCRPC 患者中的安全性、药代动力学、免疫原性和抗肿瘤活性。33 名患者接受了 MEDI3726。由于 AE (90.9%),研究结果受到限制,包括 45.5% 患者的 CTC 3 级或 4 级;。中位无进展生存期 (PFS) 为 3.9 个月,中位 OS 为 10.6 个月。临床前研究表明,MEDI3726 的活性取决于磷酸化的组蛋白 H2AX,并在异种移植物和细胞系研究中显示出活性。
5D3-DM1是一种新型抗PSMA抗体,其特殊特性使其成为一种很有前途的药物,其疗效结果最近由Huang等人发表。5D3-DM1的特点是比J591抗体具有更高的亲和力、快速内化和中心体定位能力、持久性和有效的药物释放。该药物在体外和体内均具有良好的抗肿瘤活性。在 PSMA 阳性细胞中观察到反应,但在 PSMA 阴性细胞中几乎没有抗肿瘤作用。毒性较低,没有任何明显的肾脏或肝脏损伤。
STEAP-1
STEAP-1 蛋白是一种 339 个氨基酸的细胞表面抗原,可能充当离子通道或蛋白质转运蛋白。在人类中,STEAP-1 基因位于 7 号染色体上。一项 IHC 研究证实了它在前列腺上皮细胞中的高表达,特别是在细胞-细胞连接处。在 PCa 的每个临床阶段都观察到 STEAP-1 表达。在非前列腺组织中,STEAP-1 在膀胱细胞中适度表达,并且在除 PCa 之外的癌症中过度表达,例如尤文肉瘤、膀胱癌、结肠癌和卵巢癌。STEAP 通过调节肿瘤和基质之间的细胞内通讯来调节肿瘤生长。STEAP-1 表达谱使其成为有前景的药物靶点。此外,STEAP 被用于基于肽的疫苗。一项针对 PCa 和 BCa 异种移植物的临床前研究表明,抗 STEAP 抗体能够抑制肿瘤生长。
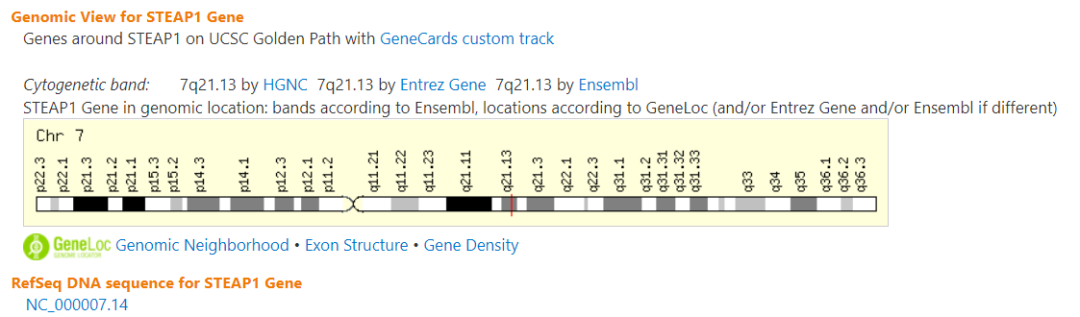
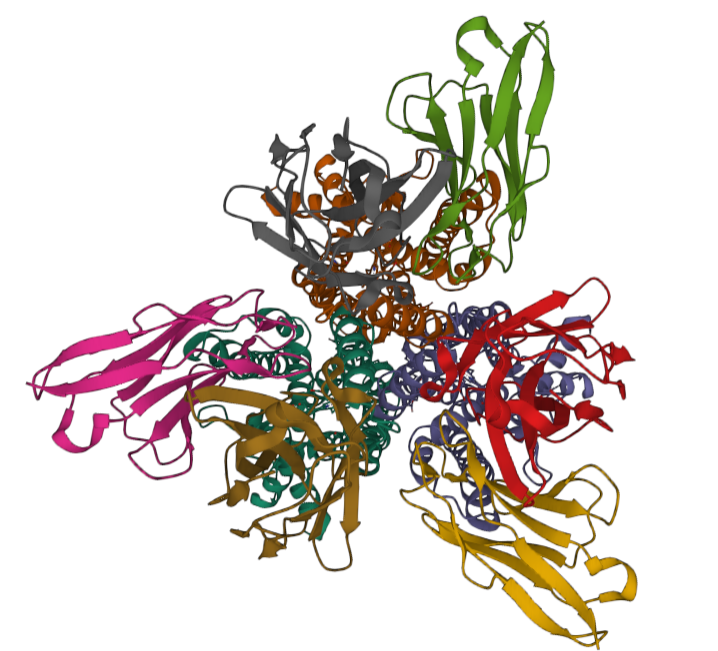
PDB:6Y9B Cryo-EM structure of trimeric human STEAP1 bound to three Fab120.545 fragments
靶向STEAP-1的ADC临床进展
Vandortuzumab vedotin (VV) 是目前在 PCa研究中的唯一靶向STEAP-1的 ADC。NCT01283373 是一项 I 期研究,评估了 mCRPC 患者增加剂量 VV (DSTP3086S) 的安全性和药代动力学。共有 84 名患者入组。剂量递增组包括每 3 周接受 0.3-2.8 mg/kg VV 静脉注射(28 名),每周接受治疗(7 名)。初始扩展组中的 10 名患者接受 2.8 mg/kg 治疗,两个扩展队列中 39 名患者接受 2.4 mg/kg 治疗。最常见的 AE 是疲劳 (56%)、周围神经病变 (51%) 和恶心 (38%)。77 名患者中有 31% 有 3 级或 4 级 AE。那些接受过 >2 mg/kg 的研究药物实现了 18% 的 PSA达到了50% 下降、放射学反应 (6%) 和循环肿瘤细胞转化 (59%)。该试验证实 DSTP3086S ADC 具有可接受的安全性,并在 mCRPC 患者中显示出活性。
SLC44A4
SLC44A4 或胆碱转运蛋白样蛋白 4 是属于胆碱转运蛋白家族的跨膜蛋白.SLC44A4 参与非神经元乙酰胆碱合成并且在上皮分泌性前列腺细胞中观察到其表达。IHC 研究显示 SLC44A4 在几种肿瘤中的表达上调,包括 85% 的原发性 PCa。在分化较差的肿瘤中证明了其较高的表达。体内研究揭示了 SLC44A4 定向抗体在雄激素依赖性和非依赖性肿瘤异种移植物中的抗肿瘤活性。ASG-5ME 靶向 SLC44A4 的 ADC药物
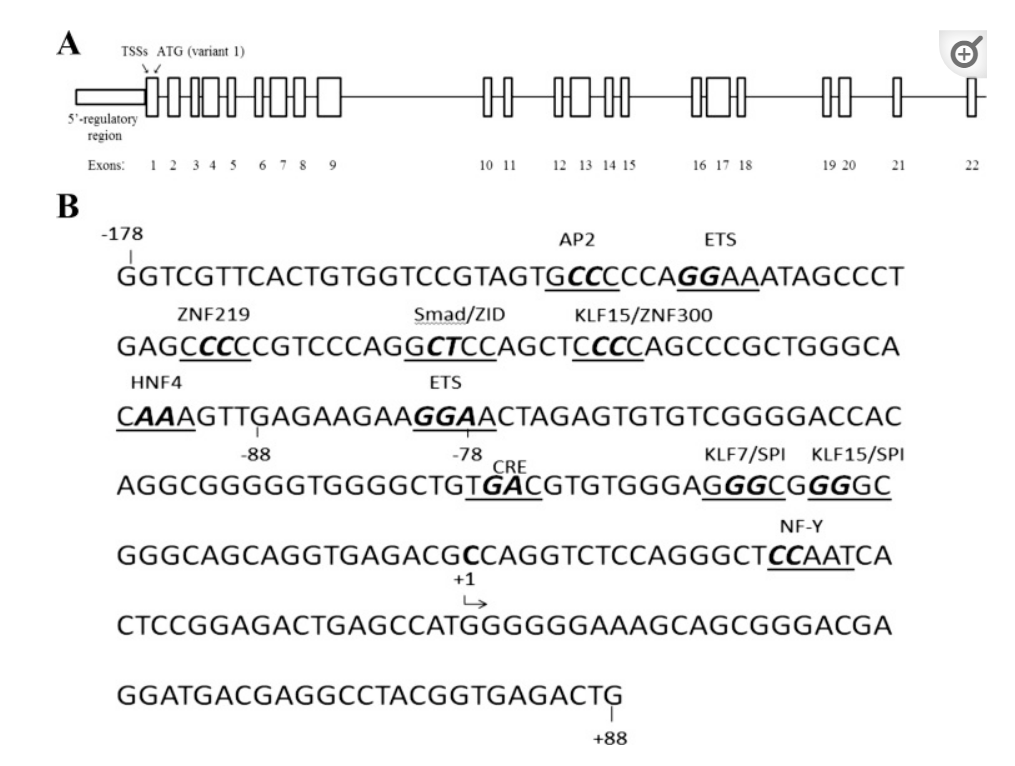
靶向SLC44A4的ADC临床进展
NCT01228760 是一项 I 期临床试验,确定转移性或非转移性 CRPC 患者中 ASG-5ME 的 MTD。该研究分为两部分——第一部分确定 ASG-5ME 的安全剂量,第二部分评估安全性和抗肿瘤活性。共有 46 名患者参加了该研究。26 名患者被纳入剂量递增组,该组分为 7 个队列。剂量0.3-3 mg/kg。20 名患者被纳入剂量扩展队列并接受 2.4 或 2.7 mg/kg 的研究药物。25% 的评估患者实现了 PSA 反应,下降 > 50%。根据 RECIST 1.1 标准,SD 和 PD 是最常见的结果,而最常见的 AE 是疲劳和腹泻。研究期间发生了两人死亡。
Trop-2
Trop-2 是一种表面跨膜糖蛋白,尤其存在于前列腺细胞中。Trop-2的主要功能仍然未知;然而,根据文献,它调节前列腺细胞自我更新、细胞间粘附和细胞外相互作用。在 PCa 中,Trop-2 通过调节 α5β1 整合素依赖性信号通路驱动转移潜能并支持 PCa 生长。Trop-2 在 > 70% 的 PCa 中上调,但在前列腺外延伸、CRPC 和神经内分泌癌的肿瘤中其表达更高。
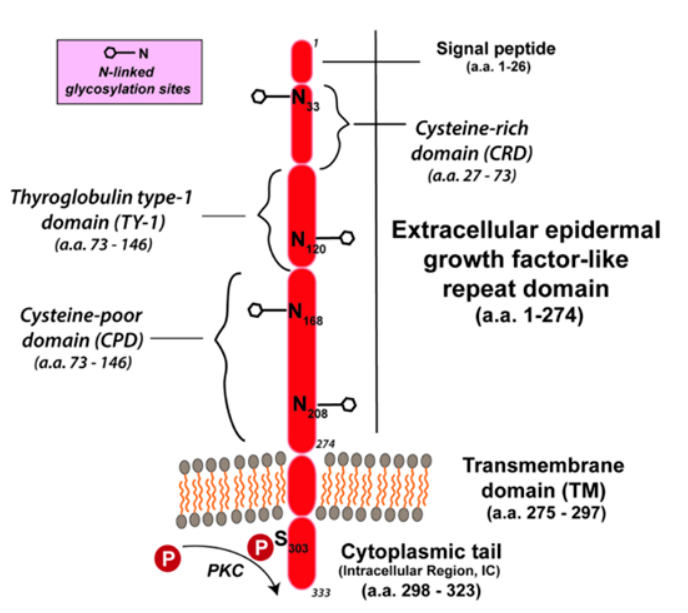
靶向Trop-2的ADC临床进展
NCT03725761 是一项正在进行的 II 期研究,旨在确定 SG 在使用新一代抗雄激素(恩杂鲁胺、阿帕鲁胺或醋酸阿比特龙)取得进展的 mCRPC 患者中的安全性和有效性。主要终点是 PSA 反应率,定义为治疗 9 周或之前 PSA 下降 ≥ 50%。次要终点包括影像学 PFS、OS 和毒性率。55 名患者将参加该研究。
B7-H3 (CD276)
免疫检查点分子B7-H3,又称为CD276,是免疫调节蛋白B7-CD28家族的膜蛋白成员,是与程序性死亡受体-1 ( PD-L1) 细胞外结构域的序列相似的I型膜蛋白。在正常人体组织中,B7-H3表达水平较低,但在多种肿瘤癌症中,B7-H3异常高表达,其在肿瘤发生发展、免疫逃逸等多个过程中发挥重要作用,与肿瘤的不良预后相关。在 PCa 中,其表达与 Gleason 评分、肿瘤分期、淋巴结转移和去势抵抗性疾病相关。此外,B7-H3 表达与 PCa 中的 BRCA2 和 ATM 突变相关。
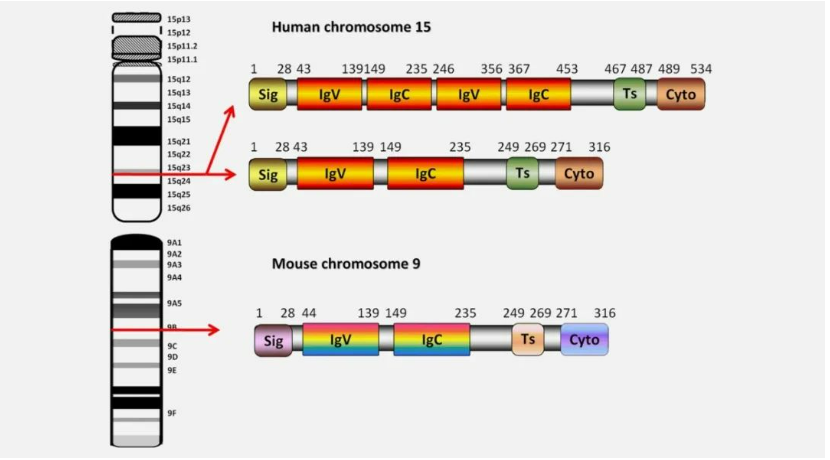
靶向B7-H3的ADC临床进展
MGC018 具有良好活性和安全性。I 期剂量递增研究常见的DLTs为中性粒细胞减少症,疲劳。剂量:3 mg/kg ,Q3W。研究中55.5% 的 mCRPC 患者实现了 PSA 反应。在最近的欧洲医学肿瘤学会大会上,在实体瘤患者中展示了 MGC018 的 NCT03729596 I 期队列剂量扩展研究的初步结果。该研究招募了化疗和下一代激素治疗后的 mCRPC 患者;53.8% 实现了 PSA 响应, PR25%。点评
点评
靶向前列腺癌(PCa)的重要靶点包括:包括前列腺特异性膜抗原 (PSMA)、前列腺六跨膜上皮抗原 1 (STEAP-1)、溶质载体家族 44成员4 (SLC44A4)、滋养层细胞表面抗原(Trop-2) 和 B7-H3。
虽然很多针对前列腺癌的ADC的设计与目前已上市的linker和payload相似,但临床结果没有特别惊人,不同的抗体即使同一个靶点也会存在很大的差异。
国内站在前人的基础上,已验证的靶点合适适应症才是王道!瞎BB FIC的都是耍流氓!
参考文献:
[1] Antibody drug conjugate: the “biological missile” for targeted
cancer therapy. Signal Transduction and Targeted Therapy (2022) 7:93
[2] The matrix in cancer. Nat Rev Cancer. 2021 Feb 15. doi: 10.1038/s41568-020-00329-7. Epub ahead of print. PMID: 33589810.
[3] Current status and future prospects of antibody–drug conjugates in urological malignancies. doi: 10.1111/iju.14925
[4] Antibody–Drug Conjugates in Uro‑Oncology. doi.org/10.1007/s11523-022-00872-3
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)