首页 > 疾病防控/ 正文
12月29日,浙江博锐生物制药有限公司(简称“博锐生物”)三特异抗体BR110(CMG1A46)的临床试验申请获国家药品监督管理局批准,这是全球首个获批临床的CD3/CD19/CD20三抗产品。该产品由恩沐生物开发,博锐生物已与其达成独家合作和授权,引进CMG1A46在大中华区(包括中国大陆、香港、澳门及台湾)的独家临床开发、生产及商业化权益。
国产三特异性抗体开发重大突破
公开信息显示,BR110是以CD3、CD19和CD20为靶点的同类首创T细胞Engager三特异性抗体,它能够同时靶向T细胞表面的CD3以及肿瘤细胞上的两个不同的生物标记物CD20和CD19,通过拉近肿瘤细胞和T细胞的空间距离,激活T细胞,杀伤表达CD19和/或CD20的肿瘤细胞。

第62届美国血液学会年会(来源:ASH)
去年12月,在ASH年会上,恩沐生物公布了BR110(CMG1A46)治疗非霍奇金淋巴瘤(NHL)的临床前研究数据。根据大会摘要,由于BR110(CMG1A46)与肿瘤细胞表面的CD19和CD20都具有很高的亲和力,因此它不仅可以靶向CD19+/CD20+DLBCL细胞,还可以针对CD19-/CD20+DLBCL细胞,以及CD20低表达的DLBCL细胞。
体外研究中,BR110(CMG1A46)能够以剂量依赖性方式通过人外周血单个核细胞(PBMC)介导肿瘤细胞裂解。与基于IgG形式的常规“1:1”CD3xCD20双特异性抗体相比,CMG1A46显示出更强的效力和安全性。此外,研究还显示,在同时表达CD19和CD20的细胞,以及仅表达CD19或CD20的细胞中,BR110(CMG1A46)均能诱导有效的肿瘤裂解。
体内研究显示,在移植了人类PBMC的NOD小鼠模中,BR110(CMG1A46)显示出了强大的肿瘤抑制活性,并诱导了CD19+/CD20+Jeko-1淋巴瘤和CD19+/CD20- A20-hCD19肿瘤的快速消退。
在食蟹猴中的药代动力学研究表明,以1mpk(mg/kg)剂量给药时,BR110(CMG1A46)在血清中的半衰期超过70小时。给药剂量高达10mpk(mg/kg)时也未导致显著的不良反应。首次给药后24小时内,CMG1A46可使外周血中的B细胞被迅速完全消除。完成最后一次给药后(1mpk),外周B细胞消除可持续至少28天。
总结来说,在体外和体内实验中,BR110(CMG1A46)表现出比传统的“1:1”IgG格式的其他CD3xCD20双特异性抗体更好的效力和安全性。在食蟹猴中的初步研究显示,BR110(CMG1A46)在血清中具有天然IgG样半衰期,且毒性可控。这些数据表明,作为一种新型的CD19/CD20靶向T细胞衔接三特异性抗体,BR110(CMG1A46)具有非常好的抗肿瘤潜力,临床开发前景令人期待。
此次IND申请获批不仅是BR110迈向临床开发阶段的关键里程碑,也是对恩沐生物三特异性抗体TRIAD技术平台成药性的重要验证,同时也代表了国产三特异性抗体开发的又一突破。
曾经免疫新秀 已成抗癌“老炮”
进入肿瘤的综合治疗阶段,免疫疗法成为国自然C位。一方面作为靶向药物对抗血液系统肿瘤,一方面作为新辅助免疫疗法让实体瘤达到缩瘤、降期的目的,一时之间,癌症免疫治疗成为肿瘤内外科的宠儿。
当年PD-1单抗全球大卖,在肿瘤治疗界投下“重磅炸弹”,带动靶向治疗、精准治疗、个体化治疗等一批前沿治疗理念蓬勃发展,也推动肿瘤医学进入综合治疗阶段。
从2013年癌症免疫治疗被Science期刊评为年度十大科学突破之首开始,针对单靶点的特异性抗体研发异常火热,各路药企纷纷寻找成药性大、有潜力的靶点进行挖掘布局。
任重道远:单抗未魇 双抗出道
原癌基因激活后通过一系列免疫生化反应所引起的细胞非特异性增殖是癌细胞增生扩散的基石。单克隆抗体将生化反应途中的关键蛋白质作为特异性抗原,通过免疫反应杀死肿瘤细胞、引起肿瘤细胞凋亡或者抑制癌细胞增殖。然而潜在可成药靶点抗原终归有限,科研人员不得不将目光投入到单克隆抗体的改造上来,针对抗原抗体结合位点,合成具备识别多个抗原靶点的多抗,让药物进入肿瘤病灶可以多线路作战。
理想是璀璨的,然而要实现多抗的治疗效果,必须让同一抗体的多抗靶点派上用场,这便从一开始限制了抗体的活动空间。针对血液系统肿瘤,多抗体在血浆里面有广阔的发挥空间,作为癌细胞和抗肿瘤淋巴细胞之间的媒介,为杀死癌细胞提供一个平台即可,而进入实体细胞的生化反应通路就显得艰难重重。不过,癌症患者群体是如此庞大,一隙之功已是万钧之力。
PS:双抗为肿瘤细胞和T淋巴细胞提供了结合平台
已上市的4款双抗药物中,罗氏的Hemlibra全球销售额突破百亿人民币大关。截至2021年11月,国内已有近70款双抗药物进入临床试验,多是针对血液系统肿瘤大开大合挥动板斧,以期将癌细胞按在地上摩擦。
不甘落后:三抗曙光乍现
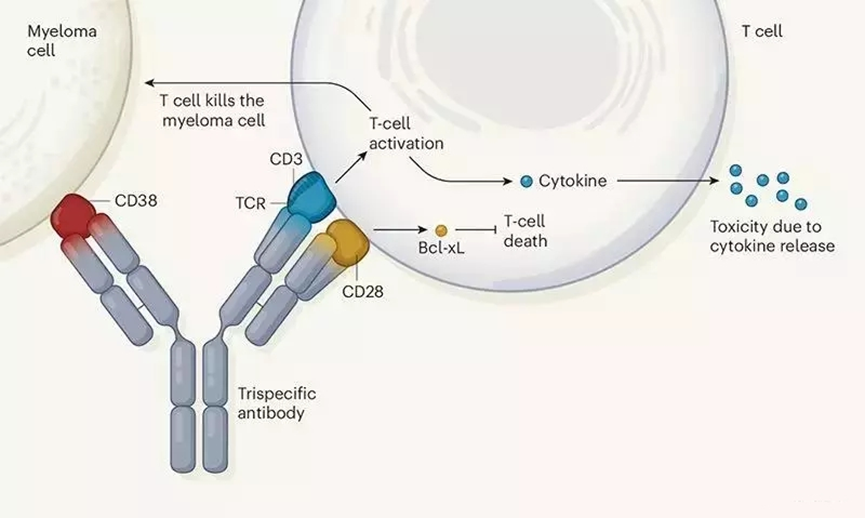
随着特异性靶点研究的不断完善,抗体改造技术也逐渐精进,三抗药物随即呼之欲出。2019年赛诺菲公司研发出一款针对CD38、CD3、CD28的三特异性抗体并应用于骨髓瘤小鼠模型。2019年11月18日Science子刊Nature Cancer收录了该研究成果。

研究成果(图源:Nature Cancer)
宾夕法尼亚大学佩雷尔曼医学院Carl June博士针对该研究在Science期刊专门做了评议,认为三特异性抗体为抗癌免疫治疗提供了第三条前进方向。

研究成果(图源:Nature Cancer)
双抗已凸显出庞大的医疗产业价值,三抗会不会成为癌症免疫治疗的另一个扛鼎之作?各大药企纷纷布局,科创板块的创新药企也以此作为新药研发的突破口,然而,多数仍旧停留在动物实验的庞杂数据中,未能同时交出安全性与有效性的双优答卷,这一赛道期待破局。
恩沐生物开发的三特异性抗体BR110(CMG1A46)新药研究申请(IND)被国家药监局批准,意味着全球首款抗CD3/CD19/CD20的三抗产品可以从动物实验进入临床试验,这一领域的又一缕曙光来得可谓及时。
参考来源:
[1]https://doi.org/10.1038/d41586-019-03495-3
[2]https://doi.org/10.1038/s43018-019-0004-z
[3]https://news.medlive.cn/all/info-progress/show-55752_53.html
[4]http://www.bioraypharm.com/index.php?m=content&a=index&classid=5&id=24
[5]https://www.anewsday.com/post/216585.html
猜你喜欢
- 研究发现:喜欢吃肉的人,更容易得这种病,很难治好!
- 跳绳这项运动坚持多久之后能减肥
- 赋能县域医疗|两项中国原创研究为心血管病防治提供全新策略
- Clin Otolaryngol:北京同仁医院发文内耳畸形伴听力损失儿童在人工耳蜗植入后耳石与平衡功能变化
- 崩漏怎么治疗呢?什么是崩漏
- 新冠引发患儿脑炎案例多发,冬季儿童呼吸道疾病药荒如何解决?
- Molecular Psychiatry:CLN5 缺陷如何引发神经退行?多组学分析锁定关键代谢通路与潜在靶点
- 华润江中全国高校巡讲圆满收官!集结青春新“食”力,用创意燃爆校园!
- 循证视角: 富含IgM的强化免疫球蛋白为新生儿及儿童脓毒症管理带来多重获益
- 关于白蛋白的知识,你需要明明白白?
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)