首页 > 医疗资讯/ 正文
脓毒症是一种因感染引发的危及生命的器官功能障碍,全球每年发生超过5000万例,死亡率高达20%。尽管现代医学在抗感染和支持治疗方面取得了进步,脓毒症尤其是脓毒性休克的死亡率依旧居高不下, ICU的死亡率甚至可达40%至50%。脓毒症的复杂病理机制涉及失控的炎症反应、免疫功能失调、内皮损伤以及微循环障碍。近年来,精准医学理念推动了对脓毒症不同亚型的识别,促使辅助治疗策略逐渐向个体化转变。

维生素作为重要的微量营养素,参与氧化还原反应、能量代谢和免疫调节,其在脓毒症中的作用受到广泛关注。尤其是维生素C、D及维生素B族(B1、B9、B12)因其多靶点调节优势,被认为可能成为脓毒症辅助治疗的潜在选择。本文通过系统综述2016年至2025年的相关文献,分析各类维生素的作用机制、临床试验结果及其应用前景,旨在为临床提供科学依据并探讨未来研究方向。
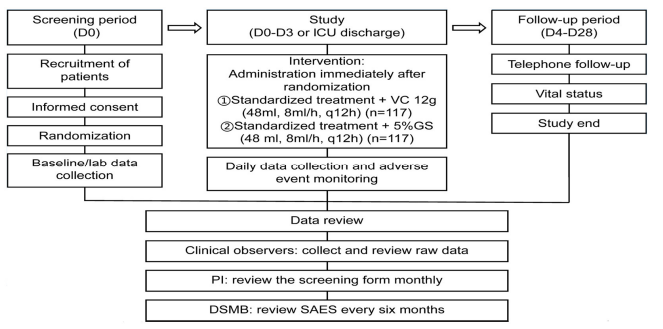
图:CEMVIS研究的临床试验流程
维生素C的治疗潜力
维生素C作为一种强效抗氧化剂,能减轻氧化应激,促进内源性儿茶酚胺合成,改善微循环,有望改善脓毒症患者预后。2017年,Marik等提出的高剂量维生素C联合硫胺素及氢化可的松的“HAT方案”引发热议。然而,随后包括VITAMINS、ACTS、CITRIS-ALI及LOVIT等大规模随机对照试验均未明确证实其降低死亡率的效益,部分研究甚至提示可能存在潜在风险。
近期的C-EASIE多中心随机试验强调早期(入院6小时内)使用维生素C,发现重症脓毒症患者(SOFA≥6)器官功能障碍有所缓解,且减少了肾脏替代治疗需求。结合对LOVIT生物学亚型的进一步分析显示,不同炎症表型对维生素C的反应存在显著差异,提示精准分层治疗的重要性。MIMIC-IV数据库回顾性研究亦发现,脓毒症相关性急性肾损伤患者使用维生素C与降低院内死亡率相关,但仍需随机试验进一步验证。
当前,维生素C普遍补充尚无足够证据推荐,临床应用应考虑患者个体特征、补充时机和剂量策略。正在进行中的中国CEMVIS试验,探索超高剂量维生素C在脓毒症中的疗效,期待为该领域提供更明确的指导。
硫胺素(维生素B1)在脓毒症中的作用
硫胺素是能量代谢关键酶的辅酶,支持线粒体功能,参与三羧酸循环。在脓毒症患者中,硫胺素缺乏较为常见,且与乳酸酸中毒、肾功能不全风险升高相关。研究表明,硫胺素单药补充在缺乏患者中可显著提高无肾替代治疗的生存率。
然而,多项随机对照试验及荟萃分析尚未显示硫胺素单独使用能显著降低死亡率,但其对代谢指标如乳酸水平有积极影响。与维生素C及氢化可的松联合使用的“HAT方案”虽改善SOFA评分及乳酸水平,但未转化为显著的生存优势。硫胺素安全耐受性良好,建议针对确诊缺乏的高风险患者进行补充,尤其是在消化系统疾病、酗酒及长期抗生素应用患者中。
维生素D的免疫调节潜力
维生素D通过其活性形式1,25-二羟基维生素D作用于免疫细胞,调节炎症反应,增强抗菌肽如LL-37的产生。临床研究表明,维生素D缺乏与脓毒症患者预后不良相关。
2024年Ashoor等随机临床研究指出,高剂量维生素D3(50,000 IU)显著降低机械通气患者的炎症指标及SOFA评分,缩短住院时间,且安全性良好。大规模数据库研究亦发现维生素D补充与28天死亡率下降相关。尽管如此,系统综述显示临床试验结果存在较大异质性,剂量、起始时间及基线维生素D水平差异是主要因素。只有部分患者达到推荐的血清25(OH)D浓度(>30 ng/mL),这可能影响了疗效的显现。
叶酸及其他维生素B族的作用及挑战
维生素B族包括硫胺素(B1)、核黄素(B2)、吡哆醇(B6)、叶酸(B9)和钴胺素(B12),是细胞代谢必需的辅酶,参与能量代谢、核酸合成及同型半胱氨酸代谢,在调节氧化应激和免疫反应中发挥作用。
叶酸在脓毒症中的作用复杂。一项30例脓毒性休克患者研究发现,部分患者叶酸水平升高反而与28天死亡率及机械通气时间延长相关,提示叶酸过量可能与细胞利用障碍和代谢紊乱有关。临床上,叶酸补充剂需谨慎应用,尤其在肾脏替代治疗患者中,活性叶酸补充(如叶酸钙)可有效纠正缺乏。当前指南推荐根据患者状况选择合适剂量及给药途径。
钴胺素(维生素B12)缺乏与高同型半胱氨酸血症及内皮功能障碍相关,部分研究表明血清B12水平异常无论偏高或偏低均可能预示预后不良。维生素B族补充需基于个体缺乏状况,制定个性化方案。
营养状态与肠道微生态的影响
营养状态是脓毒症患者预后的重要影响因素。多种营养评分如修订版Glasgow预后评分(mGPS)、营养风险评分(mNUTRIC)均显示营养不良与死亡率显著相关。与此同时,肠道菌群失调是脓毒症发病机制的重要组成部分。患者肠道菌群多样性降低,有益菌减少,致病性菌群增生,导致肠屏障功能受损,细菌及内毒素易入血,加剧全身炎症反应和免疫失衡。
肠道菌群通过短链脂肪酸调节免疫反应,促进调节性T细胞分化,抑制NF-κB活化,增强抗菌能力。抗生素滥用加剧菌群破坏,增加感染风险。当前肠道菌群调节策略包括益生菌、益生元、粪菌移植等,但疗效尚需进一步验证,风险控制亦是重点。未来脓毒症治疗可能结合个体菌群和代谢物谱,实现精准干预。
结论
脓毒症是临床重大挑战,维生素C、D及B1在辅助治疗中展示出一定潜力,但目前证据尚不足以普遍推荐。叶酸及维生素B12相关研究尚处起步阶段。补充策略应基于患者个体营养状态及代谢表型,避免盲目高剂量补充。精准营养支持及结合肠道菌群调节的综合治疗,有望提升脓毒症患者预后。未来需设计多中心、大样本、分层随机临床试验,推动维生素治疗规范化和个体化发展,促进脓毒症综合治疗水平提升。
原始出处
Radkowski, P.; Gogojewicz, A.; Charasna, J.; Pilaczyńska-Szcześniak, Ł.; Grabarczyk, Ł. The Role of Vitamins in Sepsis: A Narrative Review. Nutrients 2025, 17, 3330. https://doi.org/10.3390/nu17213330
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)