首页 > 医疗资讯/ 正文
平滑肌肉瘤是一种恶性软组织肿瘤,在转移阶段预后仍然很差,通常仅持续数月。除手术和放疗外,该肿瘤实体的常规治疗由化疗方案决定。除抗血管生成有效药物外,几乎没有已确立的靶向治疗选择。本文报告一名 70 岁男性转移性平滑肌肉瘤患者的案例,该患者除接受肿瘤部分切除术和放疗外,还通过九线肿瘤治疗,在四年内实现了长期控制。此处报告的生存期远高于批准的标准治疗下的预期生存期。该患者长期治疗的关键在于对癌组织进行全面的泛癌种panel测序(CCP,即基因组DNA的下一代测序)以寻找分子靶点。检测到一个同源重组修复(HRR)基因的功能缺失突变,从而能够使用PARP抑制剂奥拉帕利进行治疗。另一个特点是加用了烷化剂替莫唑胺;这种联合治疗的疗效此前仅在子宫平滑肌肉瘤中得到证实,但在本文报告的这名男性患者中也被证明是一种有效的治疗策略。尽管先前应用的化疗累积剂量较高,但靶向肿瘤治疗耐受性良好且有效。该病例报告表明,对肿瘤组织进行系统性分子测序并在分子肿瘤委员会上进行讨论,对于确定分子靶点结构以优化转移性平滑肌肉瘤的姑息性全身治疗具有重要价值。此外,该病例报告还表明,奥拉帕利/替莫唑胺联合治疗可能也是HRR功能缺失的非子宫平滑肌肉瘤的一种有效治疗方法。
背 景
平滑肌肉瘤(LMS)是成人中的恶性软组织肉瘤(STS),表现出高度的分子异质性。除组织病理学诊断外,通过蛋白质组聚类可区分出三种平滑肌肉瘤分子亚型。此外,软组织肉瘤亚型可通过DNA甲基化特征来表征。子宫平滑肌肉瘤(uLMS)由于具有不同的细胞遗传学和基因表达模式,被区分为与其他部位平滑肌肉瘤不同的独立实体。转移性平滑肌肉瘤目前主要采用化疗治疗;除多靶点酪氨酸激酶抑制剂(Multi-TKI)帕唑帕尼外,目前几乎没有其他靶向治疗选择。转移性平滑肌肉瘤的总生存期较差,中位生存期不足两年。在肿瘤免疫学方面,平滑肌肉瘤的肿瘤微环境(TME)具有特殊性;软组织肉瘤中有效的免疫检查点抑制剂(ICB)治疗需要富含B细胞的三级淋巴结构;尽管平滑肌肉瘤肿瘤微环境的细胞组成可预测ICB的疗效,但ICB尚未被批准用于治疗。最近,已有HER2靶向CAR-T细胞治疗用于难治性肉瘤的报道,而其他细胞免疫疗法尚未在该实体瘤中确立。
本文报告一名转移性平滑肌肉瘤患者的治疗情况,该患者通过九线治疗在四年内实现了长期控制。其关键在于泛癌种panel测序,检测到一个同源重组修复(HRR)功能缺失突变,从而能够使用PARP抑制剂奥拉帕利进行治疗。奥拉帕利联合替莫唑胺的疗法目前仅在子宫平滑肌肉瘤中确立,但在本例男性患者的腹膜后肉瘤中也被证明是有效且可耐受的。
病 例
患者男,70 岁,因弥漫性背痛于 2020 年 2 月接受计算机断层扫描(CT),发现腹膜后肿块(大小 4×6×8 cm,位置:L2椎体高度)。当时患者总体状况良好,东部肿瘤协作组(ECOG)体力状况评分为 1 分。后续正电子发射断层扫描-CT(PET-CT)未发现其他恶性典型高代谢结构。除药物控制的动脉高血压和伴甲状腺功能亢进的结节性甲状腺肿外,患者无其他已知基础疾病。CT引导下肿块穿刺诊断为 75 mm大小、中分化、增殖活跃(Ki67 60-70%)的平滑肌肉瘤(LMS)。2020 年 2-4 月,患者初始接受 3 个周期的新辅助化疗,方案为多柔比星(75 mg/m²)联合异环磷酰胺(5 g/m²),通过输液港给药。治疗期间出现 3 级神经毒性(CTCAE标准),导致治疗中断。2020 年 6 月,患者接受经腹正中切开腹膜后肿瘤切除术及淋巴结清扫术。病理分期:pT2 pN1(1/6,无脉管癌栓),cM0,R2(镜下残留),L0(无淋巴管侵犯),V0(无静脉侵犯),Pn0(无神经侵犯),法国国家癌症中心肉瘤分级系统(FNCLCC)评分为2+2+1分,微卫星稳定,美国癌症联合委员会/国际抗癌联盟(UICC/AJCC)2017分期为II期。2020 年 8-9 月,患者接受辅助放疗(25 次×2 Gy,总剂量 50 Gy;R2区域加量 16 Gy)。2020 年 10 月CT显示肿瘤进展,累及肺部及左侧第1肋骨(LWK1)。2020 年 11 月-2021 年 10 月,患者接受二线治疗药物曲贝替定,共 14 个周期;治疗期间因出现WHO IV度中性粒细胞减少及合并十二指肠炎的上消化道出血,剂量需减至 60%。2021 年 11 月,患者出现骨、肌肉及双肺肿瘤进展,并新发孤立性肝转移,遂换用帕唑帕尼(800 mg/d)治疗。因持续白细胞及血小板减少,2022 年 2 月治疗剂量逐步减至 400 mg/d。2022 年 3 月肿瘤进一步进展,治疗方案改为吉西他滨/多西他赛(2022 年 3-10 月),并对孤立性肝转移灶行经动脉化疗栓塞(TACE)。2022 年 11 月,患者出现肺部及T9椎体肿瘤进展,治疗换用艾日布林。2023 年 2 月,该治疗下肿瘤再次进展,故 2023 年 3-6 月改用帕博利珠单抗行免疫检查点抑制剂(ICB)治疗。治疗后肿瘤仍进展(累及肺、第9胸椎[BWK9]、肝脏、胰腺),2023 年 6-8 月重新启用多西他赛单药治疗(2 个周期,减量至 60 mg/m²)。2023 年 8 月,患者出现T9椎体椎管浸润的疾病进展(PD),2023 年 9 月需接受放疗(T9椎体:30 Gy;椎管内软组织成分加量:39 Gy)。2023 年 10-12 月,经医保批准报销后,患者接受卡博替尼治疗(超说明书使用)。同时,2023 年 8 月对活检肿瘤组织进行全面测序,并在分子肿瘤委员会上讨论检测结果。分子病理学结果总结于表1:除TP53基因的致癌性功能缺失突变外,还发现RAD51B基因c.1111 C>T突变,该突变编码翻译终止密码子,推测可导致翻译提前终止,进而引起同源重组修复(HRR)基因功能缺失。这一发现为 2024 年 1 月肿瘤再次进展时的后续治疗提供了依据。基于HRR基因功能缺失突变,患者开始接受奥拉帕利联合替莫唑胺治疗。初始剂量为替莫唑胺 50 mg/m²+奥拉帕利 200 mg每日两次(BID),并逐步递增至目标剂量:替莫唑胺 75 mg/m²(第1-7天),奥拉帕利 200mg BID(第 1-7 天),每 21 天为一个周期。治疗期间,肝外病灶稳定,2024 年 5 月对肝转移灶行第二次TACE,耐受性良好且无并发症。治疗时间线见图1。截至 2024 年 9 月,患者总体状况改善,疾病稳定,且无明显治疗相关副作用。值得注意的是,患者体力状况持续保持ECOG 2分。尽管经历了九线治疗,患者仍能借助轮椅独立就诊,生活质量良好。
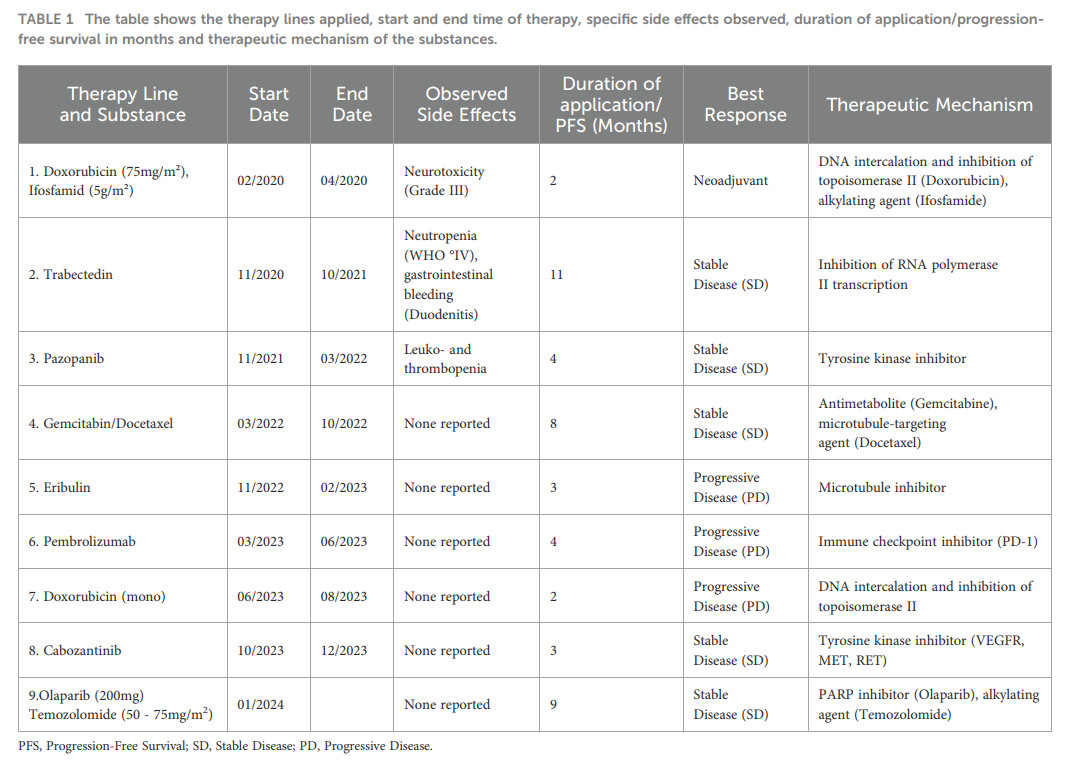
▲表1 患者所接受的治疗线、治疗开始和结束时间、观察到的具体副作用、应用持续时间/无进展生存期(以月为单位)以及治疗机制
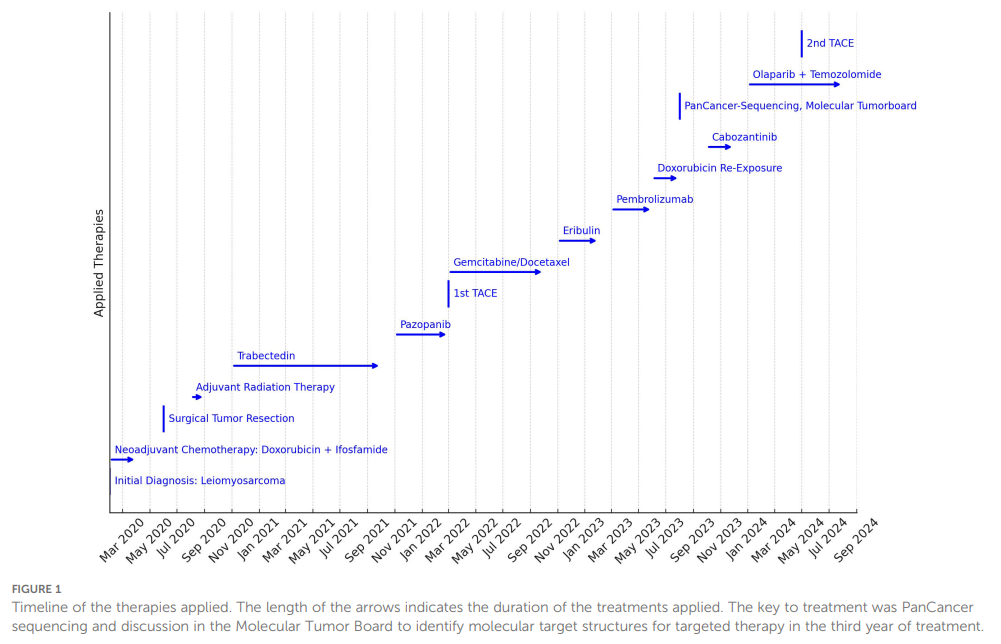
▲图1 治疗时间轴
讨 论
本文报告一例转移性平滑肌肉瘤病例接受九线治疗实现癌症长期控制。该患者第八和第九线治疗的关键在于通过泛癌种NGS测序识别肿瘤组织中的分子靶点,并在分子肿瘤委员会上讨论检测结果。
初始化疗
患者的初始治疗包括新辅助化疗(多柔比星联合异环磷酰胺)、肿瘤切除术及辅助放疗。选择多柔比星联合异环磷酰胺的联合治疗,其基本原理是通过新辅助治疗缩小肿瘤以利于肿瘤切除;然而,在非新辅助治疗指征的情况下,多柔比星联合异环磷酰胺与多柔比星单药相比,在总生存期(OS)方面未显示出优势。
曲贝替定和多靶点酪氨酸激酶抑制剂(作用于VEGFR、PDGFR、KIT)帕唑帕尼是复发情况下已确立的二线和三线药物。当疾病再次进展时,选择了含吉西他滨的治疗方案(吉西他滨联合多西他赛)。SARC-002研究显示,该联合方案在子宫平滑肌肉瘤(uLMS)中具有更高的缓解率和更长的无进展生存期(PFS),但TAXOGEM研究(纳入了子宫平滑肌肉瘤和非子宫平滑肌肉瘤患者)显示,该联合方案与吉西他滨单药相比无优势。后续的艾日布林治疗可认为与达卡巴嗪疗效相当,但也未显示出任何长期疾病控制效果。
免疫检查点阻断治疗
在本病例中,使用PD-1抑制剂帕博利珠单抗的免疫检查点抑制剂(ICB)治疗无效。这与SARC028研究结果一致,该研究中纳入的所有平滑肌肉瘤(LMS)患者均未显示出治疗反应。有趣的是,原则上可观察到ICB在软组织肉瘤(STS)中的疗效存在一定异质性,据报道未分化多形性肉瘤的缓解率高达 40%。富含B细胞的三级淋巴结构似乎在ICB治疗STS的有效性中发挥关键作用。此外,肿瘤微环境(TME)中存在MYC/MTORC1通路激活的上皮样恶性细胞及CLEC5A/SPP1阳性的M2样免疫抑制性巨噬细胞的STS,对ICB治疗显示出更高的反应。在本病例中,既往化疗暴露可能导致了一定程度的B细胞耗竭,从而降低了ICB的疗效。
多激酶抑制剂:帕唑帕尼、卡博替尼
多靶点酪氨酸激酶抑制剂(multi-TKI)帕唑帕尼基于PALETTE研究获批用于软组织肉瘤(STS)的二线治疗。本病例中,帕唑帕尼实现了 4 个月的疾病控制,而PALETTE研究中其无进展生存期(PFS)为 4.6 个月。
多靶点酪氨酸激酶抑制剂卡博替尼(抑制MET、VEGF、AXL、RET、ROS1、TYRO3、MER、KIT、TRKB、FLT3、TIE-2)用于第八线治疗。该药物尚未获批用于软组织肉瘤,既往研究报告其在软组织肉瘤中的 6 个月无进展生存率为 49%,在骨肉瘤中为 33%。
在本病例中,尽管患者既往接受过化疗、免疫检查点抑制剂及多靶点酪氨酸激酶抑制剂治疗,但仍实现了 3 个月的疾病控制。本病例表明,尽管既往接受过多靶点酪氨酸激酶抑制剂治疗,在平滑肌肉瘤中连续使用另一种多靶点酪氨酸激酶抑制剂仍可具有一定治疗效果。
泛癌种检测、分子肿瘤委员会、奥拉帕利/替莫唑胺
本病例报告后续治疗的关键在于泛癌种测序及将患者情况提交分子肿瘤委员会讨论。采用TSO 500panel进行全面基因组分析(CGP),对癌症相关基因进行了单核苷酸变异(SNV)、插入和缺失(indels)、拷贝数变异(CNV)、肿瘤突变负荷(TMB,[突变数/兆碱基])及微卫星不稳定性(MSI)检测。突变诊断结果总结于表2。此外,检测到低TMB状态(5.98 muts/Mb)及微卫星稳定(MSS,9 个标志物中 7 个稳定,1个无法评估)。TP53基因c.743G>A突变在ClinVar突变数据库中被评估为致病性突变。在IARC TP53突变数据库中,基于酵母转录反式激活试验,该变异被列为无功能变异,目前在获批或超说明书用药范围内均无针对性治疗方案。
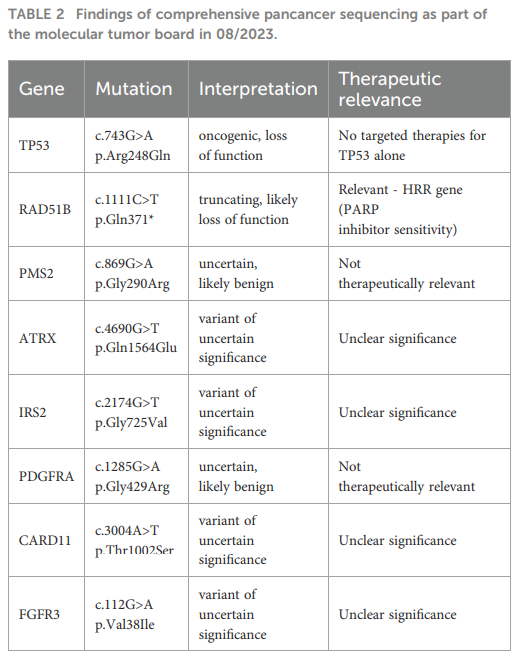
▲表2 2023年8月分子肿瘤委员会进行的综合全癌测序的结果
RAD51B基因c.1111C>T突变产生翻译终止密码子,因此推测导致翻译提前终止,进而使编码蛋白功能丧失。同源重组修复(HRR)基因的这种功能丧失突变是超说明书使用PARP抑制剂奥拉帕利治疗的依据之一。PDGFRA和PMS2基因的突变在ClinVar数据库中被评估为意义未明变异(VUS),因此,基于现有数据,无法对这两个序列变异的临床相关性得出确定性结论。但它们被归类为推测良性的罕见变异。
基于泛癌种测序结果,分子肿瘤委员会确认可采用PARP抑制剂(如奥拉帕利或卢卡帕利)进行治疗。这些药物已获批用于治疗BRCA突变(胚系和/或体细胞)的铂敏感复发高级别浆液性上皮性卵巢癌。上述变异可能导致无义介导的mRNA降解或翻译提前终止,进而导致相应编码蛋白功能丧失。
HRR基因功能丧失突变患者中使用PARP抑制剂已被描述为肉瘤的主要治疗选择之一。在Nira-Panc研究中,已探讨PARP抑制剂尼拉帕利单药治疗对(包括)携带RAD51B突变的一线进展期胰腺癌的疗效(6 个月无进展生存率为 40%,中位无进展生存期为 4.4 个月,中位总生存期为 9.1 个月)。已有初步实验证据表明尼拉帕利对HRR缺陷型软组织肉瘤有效。
鉴于PARP抑制剂靶向治疗的基本可能性,第九线治疗选择了奥拉帕利联合烷化细胞毒药物替莫唑胺。在分子肿瘤委员会讨论中,已确认的RAD51B功能丧失突变被认定为主要可作用靶点,该突变赋予肿瘤“BRCAness”表型,并预测对PARP抑制剂敏感。同时也考虑了其他变异:致病性TP53突变缺乏靶向治疗方案,PDGFRA和PMS2变异被归类为意义未明变异(VUS),因此无法作为治疗依据。针对RAD51B突变的多种治疗策略进行了权衡。铂类化疗是HRR缺陷型肿瘤的潜在选择,但由于患者既往治疗史广泛,且希望采用毒性更低的口服方案,故暂缓使用。PARP抑制剂单药治疗是另一重要选择。奥拉帕利联合替莫唑胺的联合治疗依据来源于临床前数据及一项针对RAD51重组缺陷型子宫平滑肌肉瘤(uLMS)的II期研究结果。然而,PARP抑制剂用于其他肉瘤亚型的治疗目前仅在极少数病例报告中有所描述。替莫唑胺与奥拉帕利的协同效应见图2。
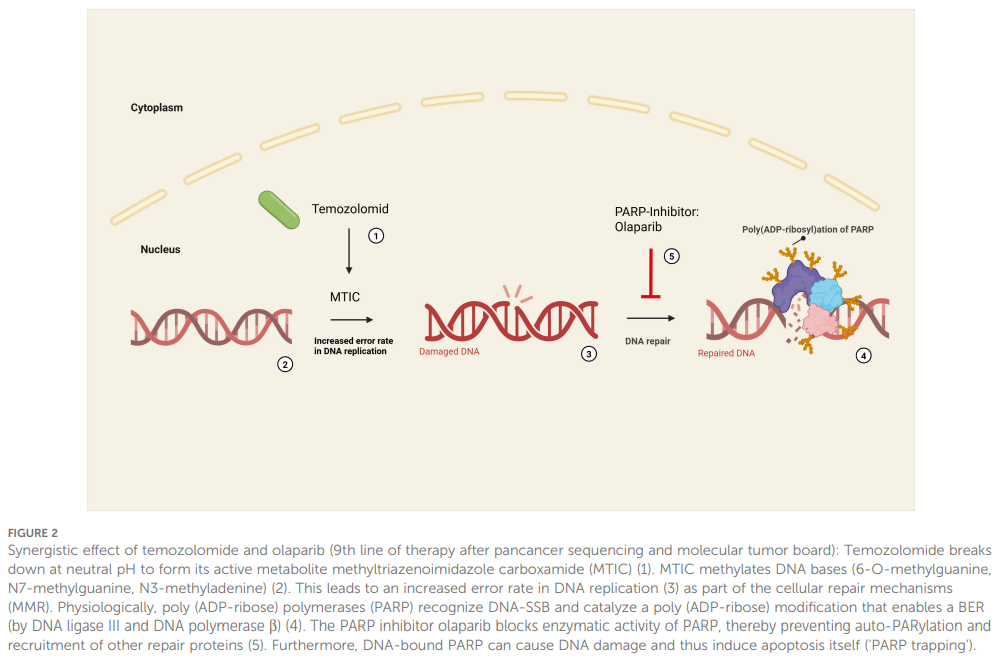
▲图2 替莫唑胺和奥拉帕利的协同作用
ULMS与非ULMS
本病例报告证实了奥拉帕利联合替莫唑胺在男性非子宫平滑肌肉瘤(non-uLMS)患者中的疗效,而该联合疗法此前仅在子宫平滑肌肉瘤(uLMS)中进行过研究。在9个月的观察期内,患者对该治疗的反应使疗效较前四线治疗提高了一倍以上。
本病例报告表明,针对uLMS的这一治疗策略对non-uLMS也可能有效,且uLMS独特的细胞遗传学特征不一定会影响分子靶向治疗。从这个角度而言,平滑肌肉瘤的病理学分型(uLMS与non-uLMS)并未反映出临床治疗上的相似性。通过泛癌种测序检测到的分子靶点结构的存在,是本病例治疗选择的唯一决定性因素,这也提示,即使更高分辨率的分子病理分型也未必能预测最佳治疗策略。
本病例中发现的RAD51B同源重组修复(HRR)缺陷赋予肿瘤“BRCAness”表型,即对同源重组修复通路缺陷的易感性,类似于携带BRCA1/2基因突变的肿瘤。具有BRCAness表型的癌细胞通常对PARP抑制剂敏感,这是因为聚腺苷二磷酸核糖聚合酶(PARP)的抑制会阻断DNA单链断裂(SSB)修复,而在HRR缺陷的情况下,双链断裂(DSB)会累积,最终导致细胞死亡(“合成致死”)。
值得注意的是,在平滑肌肉瘤(LMS)的全外显子测序(WES)和转录组测序中,大多数病例存在HR缺陷及与HRD相关的Alexandrov COSMIC突变特征AC3(Alexandrov COSMIC mutation signature AC3),且这些特征以剂量依赖方式预测对奥拉帕利的敏感性。uLMS比non-uLMS更易出现HRD,在癌症基因组图谱(TCGA)中,HR缺陷型uLMS的比例在所有肿瘤类型中位居前列;对比分析显示,uLMS的BRCA2纯合缺失率最高。本病例报告也证实了non-uLMS中存在BRCAness表型,提示在non-uLMS的治疗考量中可纳入PARP抑制剂治疗这一选择。
局限性
在本文病例中,奥拉帕利/替莫唑胺联合治疗所产生的长期治疗反应可能未受既往治疗的影响。然而,由于软组织肉瘤(STS)中免疫检查点抑制剂(ICB)的疗效依赖于B细胞,因此可推测既往耗竭B细胞的化疗降低了ICB的疗效。未来需要开展前瞻性研究以提供通用建议,但在治疗肉瘤时,应牢记既往耗竭B细胞的治疗可能对ICB疗效产生负面影响。
多柔比星单药化疗再暴露与初始应用(联合异环磷酰胺)相比无效,因此仅治疗 2 个月后便换用卡博替尼。本病例提示,以多柔比星作为一线药物进行肿瘤再挑战无效。迄今为止,科学文献中对软组织肉瘤(STS)的化疗再挑战研究非常有限。
原则上,在治疗过程中进行再次活检和/或液体活检,并通过新的泛癌种测序以检测肿瘤演进过程中的逃逸突变及可能的新治疗靶点结构是有用的。在本病例报告完成时,患者在第九线治疗下疾病稳定,因此尚未进行再次测序。
鉴于TP53的高变异丰度(VAF)以及肉瘤是李-法美尼综合征(LFS)的主要恶性肿瘤,可考虑进行胚系检测。但由于患者拒绝,未进行此项检测。
结论与展望
本病例报告记录了转移性非子宫平滑肌肉瘤经9线治疗后的长期病程,据我们所知,此类情况尚未见文献报道。本报告中的生存期远超过标准治疗下的预期生存期。尽管既往化疗累积剂量较高,但靶向治疗仍显示出疗效且耐受性良好。
治疗的关键在于泛癌种测序,其揭示了RAD51B基因突变,从而为PARP抑制剂治疗提供了可能。所选联合治疗方案奥拉帕利/替莫唑胺此前仅在子宫平滑肌肉瘤中进行过研究,但在本病例中,尽管患者先前接受过多线疗效欠佳的治疗,该方案仍显示出良好疗效。
尽管非子宫平滑肌肉瘤具有自身的分子病理学特征,但针对子宫平滑肌肉瘤的治疗策略可能对其有效,且子宫平滑肌肉瘤独特的细胞遗传学特征并非此类治疗的必要前提。这也支持在晚期疾病中开展泛癌测序并提交分子肿瘤委员会讨论。对于转移性平滑肌肉瘤,建议进行泛癌种测序并尽早提交分子肿瘤委员会讨论。
参考文献:
Klein CR, Koob S, Tischler V, Heine A, Brossart P, Feldmann G, Mayer K. Chronification of metastatic leiomyosarcoma in 9 lines of therapy by precision oncology: a case report and review of the literature. Front Oncol. 2025 Sep 2;15:1626478. doi: 10.3389/fonc.2025.1626478. PMID: 40963850; PMCID: PMC12436135.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)