首页 > 医疗资讯/ 正文
特发性肺纤维化(IPF)是一种慢性、进行性肺间质纤维化疾病,病因不明,预后较差,患者未经治疗的平均生存期仅为3-5年。目前,临床上使用吡非尼酮和尼达尼布等抗纤维化药物可延缓疾病进展,但并不能根治,且部分患者耐受性差。鉴于此,开发安全有效的新疗法迫在眉睫。 电针作为传统中医特色治疗方法,通过刺激特定穴位调节机体功能,已被证实能改善IPF患者的呼吸困难症状,但其具体分子机制尚不清楚。近年来,铁死亡作为一种依赖铁离子和脂质过氧化的细胞死亡方式,被认为在肺纤维化发生发展中起重要作用。研究电针对铁死亡相关通路的影响,有助于揭示其治疗肺纤维化的潜在机制。

本研究创新性地结合转录组学与蛋白质组学,多尺度解析了电针对博来霉素诱导肺纤维化大鼠模型的治疗机制。研究首次证实电针通过调控铁死亡及PI3K-AKT信号通路,实现对肺纤维化病理过程的干预,显著改善肺功能和减少肺组织纤维沉积。
研究人员采用SPF级SD大鼠,分为正常组、模型组及电针治疗组。肺纤维化模型通过单次膀胱内注射博来霉素建立。电针于诱导后第15天开始,选择背部肺俞(BL13)、肾俞(BL23)及足三里(ST36)穴位,每周三次,连续治疗4周。 肺功能评估采用肺功能测试系统,检测肺活量(Vital Capacity, VC)、肺吸气阻力(RI)及动态肺顺应性(Cdyn)。肺组织通过HE及Masson染色观察炎症及纤维化病理变化,免疫组化检测胶原Ⅰ(Collagen I, COL-I)及α-平滑肌肌动蛋白(α-SMA)表达。ELISA检测血清炎症因子白介素-4(IL-4)和肿瘤坏死因子-α(TNF-α),羟脯氨酸(Hydroxyproline, HYP)检测肺组织胶原含量。 此外,采用转录组学和蛋白质组学技术,分析肺组织中差异表达基因和蛋白,结合加权基因共表达网络分析(WGCNA)和基因集富集分析(GSEA),筛选与电针治疗相关的关键通路和基因模块。通过检测铁离子(Fe³⁺、Fe²⁺)、脂质过氧化物(LPO)、丙二醛(MDA)、谷胱甘肽(GSH)和超氧化物歧化酶(SOD)水平,评估铁死亡过程。线粒体超微结构由电子显微镜观察,蛋白免疫印迹检测PI3K-AKT信号通路相关蛋白表达。
研究结果
1、肺功能与组织损伤改善:电针治疗显著改善模型组大鼠体重下降,降低肺系数,提升肺活量和动态肺顺应性,降低肺吸气阻力。组织学显示电针减轻肺泡破裂、炎症细胞浸润及胶原沉积,Szapiel和Ashcroft评分显著下降。
2、炎症因子及纤维化指标下降:电针显著降低血清IL-4与TNF-α水平,减少肺组织中HYP含量及COL-I、α-SMA表达,提示抑制肺纤维化过程。
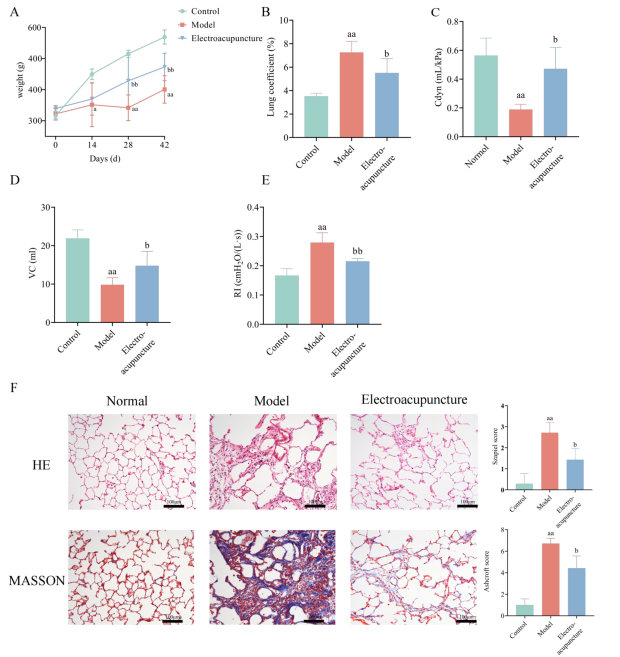
图:电针改善了肺系数、肺功能和肺组织损伤
3、多组学分析揭示关键通路:转录组学发现电针调控的差异基因富集于PI3K-AKT、FoxO、细胞外基质-受体相互作用及NF-κB信号通路。蛋白质组学分析表明电针相关蛋白涉及铁死亡、谷胱甘肽代谢及氧化还原过程。
4、铁死亡相关指标改善:电针显著降低肺组织中Fe³⁺、Fe²⁺、LPO和MDA水平,增加GSH和SOD含量,调节氧化还原平衡。电子显微镜显示电针缓解线粒体肿胀和结构破坏。
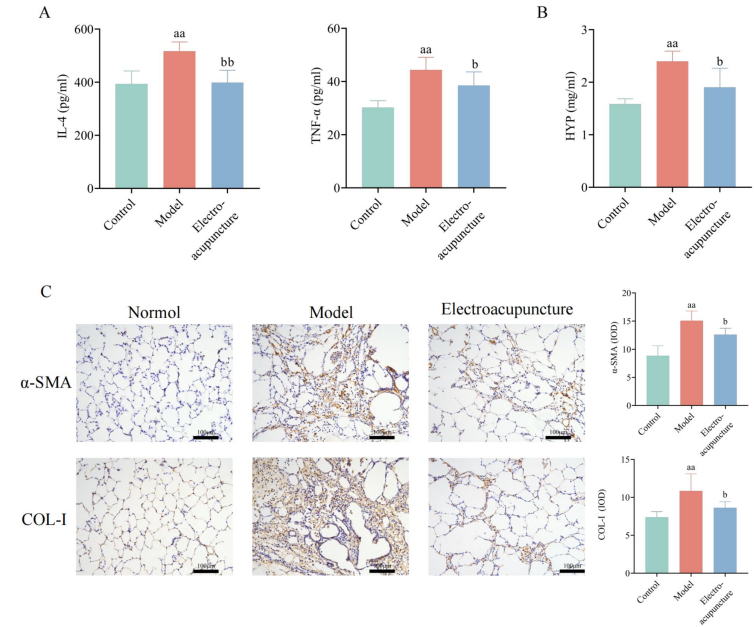
图:电针可降低炎症因子水平并减少胶原沉积
5、信号通路调控验证:免疫印迹显示电针减少肺组织中p-Akt和p-FoxO3磷酸化水平,抑制PI3K-AKT通路活化,推测其介导铁死亡调控。
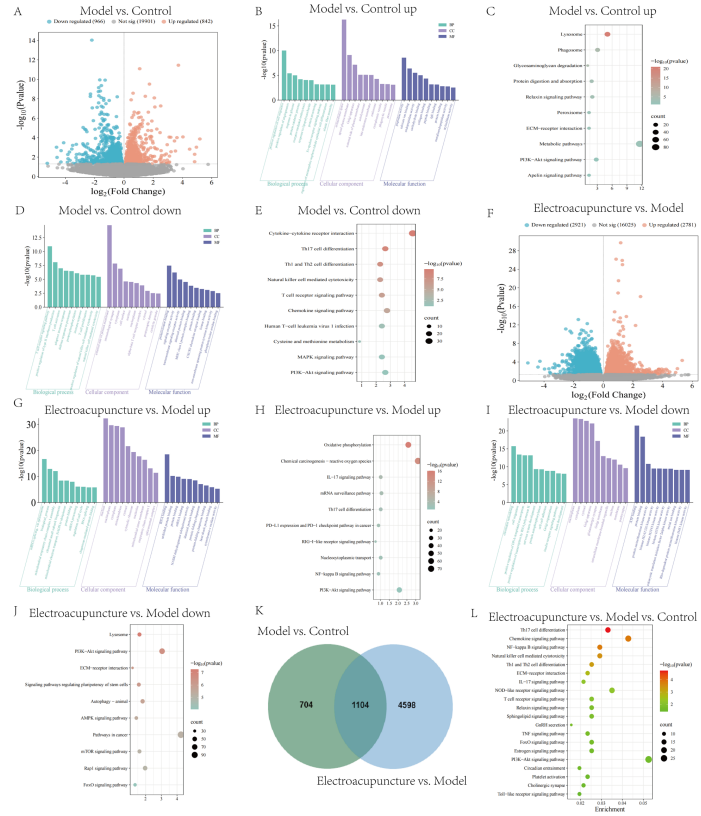
图:转录组的差异表达与功能富集分析
结论
电针通过多重分子机制调控铁死亡及PI3K-AKT信号通路,减轻博来霉素诱导的肺纤维化病理改变,改善肺功能和纤维组织沉积。这为电针作为肺纤维化辅助治疗手段提供了理论依据。
局限性及未来展望
研究尚未通过铁死亡特异性抑制剂进行功能验证,分子机制仍需进一步探讨。未来需设计多中心大样本随机临床试验,规范电针治疗参数,明确不同病程患者的疗效差异,推动电针临床转化。
原始出处
Tian Y, Song Q, Lu R, et al. Electroacupuncture stimulation improves pulmonary fibrosis by modulating ferroptosis in rats: multiscale analysis of transcriptome and proteome. Chin Med. 2025;20(1):129. Published 2025 Aug 20. doi:10.1186/s13020-025-01184-0
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)