首页 > 医疗资讯/ 正文
慢性疼痛患者常表现焦虑和抑郁等情感障碍。急性应激暴露降低疼痛反应,称为应激诱导镇痛。与之相反,慢性或反复应激暴露增强疼痛反应,称为应激诱导痛觉异常。2025年8月8日南京医科大学第一附属医院杨春、徐州医科大学曹君利团队在Molecular Psychiatry杂志发表文章揭示了急性和慢性应激通过下丘脑室旁核中不同神经元集群差异性调控疼痛反应。

1 急性应激缓解疼痛,慢性应激促进疼痛发生
接受急性应激(单次30分钟束缚应激)半小时后小鼠的缩爪潜伏期延长、缩足反射阈值增加,表明疼痛阈值增加。CFA疼痛模型小鼠在接受急性应激24小时后可引起显著的疼痛阈值增加,这种缓解疼痛的作用仅能持续1天。接受慢性应激(单次4小时束缚应激,连续5天)半小时后小鼠的缩爪潜伏期减短、缩足反射阈值减小,表明疼痛阈值减少,引起超敏反应。CFA疼痛模型小鼠在损伤后2周疼痛消失,在接受慢性应激后疼痛小鼠仍表现出痛觉异常,并能加重焦虑和抑郁样行为。这些结果表明急性应激缓解疼痛,慢性应激促进疼痛发生。
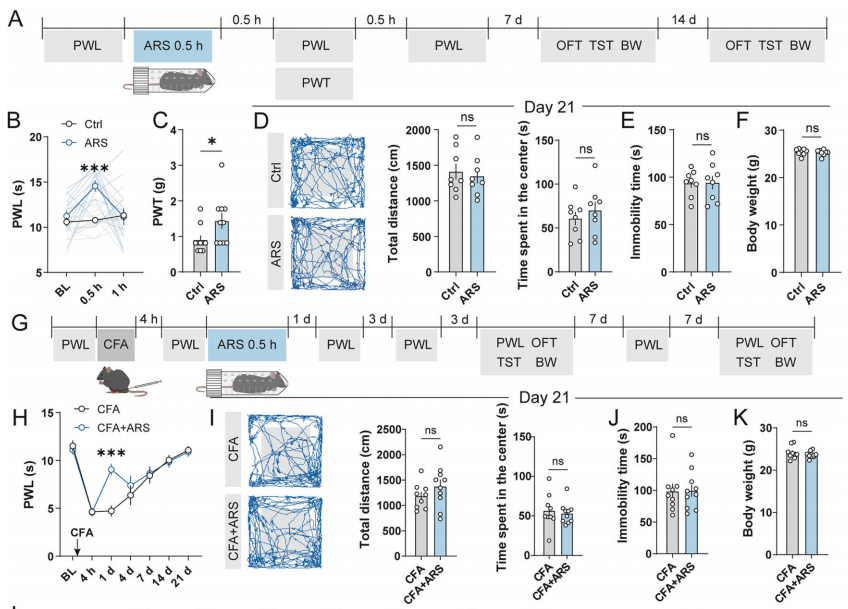
图1、急性应激缓解疼痛
2 下丘脑不同神经元群差异性调控急性和慢性应激对疼痛的调控作用
进一步通过免疫荧光实验筛选急性应激和慢性应激引起大脑神经元活性变化的脑区,其中下丘脑室旁核(PVN)在上述两种应激中均被显著激活。有意思的是,急性应激激活的神经元主要位于前侧-中侧PVN区域,而慢性应激激活的神经元主要位于中侧-后侧PVN区域,存在解剖学位置的差异性。另一方面,急性和慢性应激激活的神经元类型也存在差异性:急性应激显著激活PVN谷氨酸能和CRH阳性神经元,慢性应激显著激活PVN脑区OXT神经元。
通过cFOS工具小鼠标记急性应激激活的神经元群(TRAP-ARS神经元),抑制这类神经元群后可显著阻断急性应激引起的疼痛阈值增加,也能阻断急性应激在CFA疼痛模型中的镇痛作用。化学激活TRAP-ARS神经元群后可引起小鼠疼痛阈值的增加,并能在CFA疼痛模型中发挥短暂的镇痛作用。类似的,通过cFOS工具小鼠标记慢性应激激活的神经元群(TRAP-CRS神经元),抑制这类神经元群后可显著阻断慢性应激引起的痛觉超敏反应,也能阻断慢性应激在CFA疼痛模型中促进疼痛发生的作用,改善焦虑和抑郁行为。化学激活TRAP-CRS神经元群后可引起小鼠疼痛阈值的降低,并能在CFA疼痛模型中促进疼痛发生,引起焦虑和抑郁样行为。
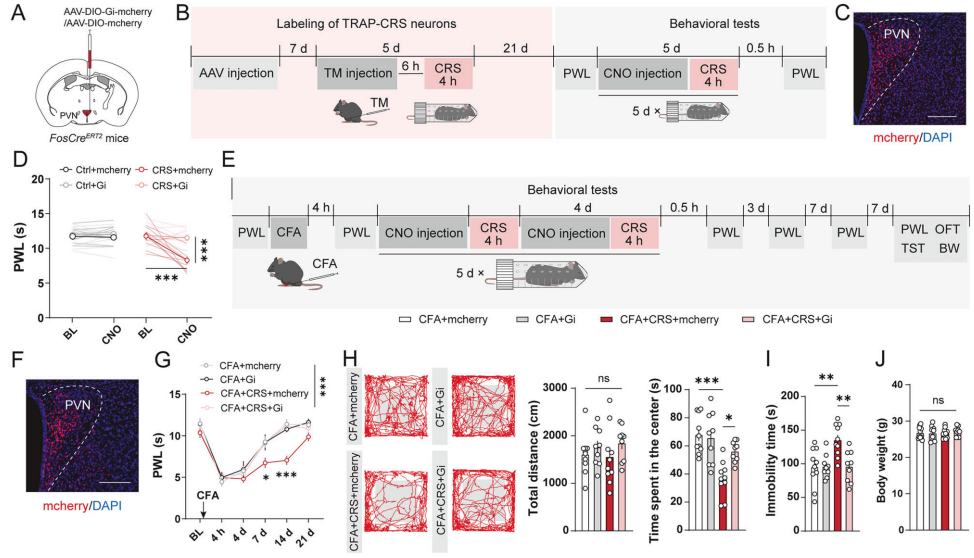
图2、抑制慢性应激激活的神经元群后可缓解疼痛,改善焦虑和抑郁行为
3 下丘脑-蓝斑环路调控急性应激的缓解疼痛,下丘脑-外侧隔核调控慢性应激的促进疼痛作用
病毒示踪实验发现PVN脑区TRAP-ARS神经元可投射到外侧隔核(LS)、蓝斑(LC)、终纹床核、中缝背核等区域,TRAP-CRS神经元可投射LS、腹侧被盖区、中缝背核等脑区。急性应激可激活LC脑区神经元,抑制LS神经元,慢性应激可激活LS脑区神经元。利用病毒工具特异性抑制投射到LC脑区的PVN脑区TRAP-ARS神经元(简称PVN TRAP-ARS→LC环路)可显著阻断急性应激引起的疼痛阈值增加,也能阻断急性应激在CFA疼痛模型中的镇痛作用。化学激活PVN TRAP-ARS→LC环路后可引起小鼠疼痛阈值的增加,并能在CFA疼痛模型中发挥短暂的镇痛作用。
特异性抑制投射到LS脑区的PVN脑区TRAP-CRS神经元(简称PVN TRAP-CRS→LS环路)可显著阻断慢性应激引起的痛觉超敏反应,也能阻断慢性应激在CFA疼痛模型中促进疼痛发生的作用。化学激活PVN TRAP-CRS→LS环路后可引起小鼠疼痛阈值的降低,并能在CFA疼痛模型中促进疼痛发生。
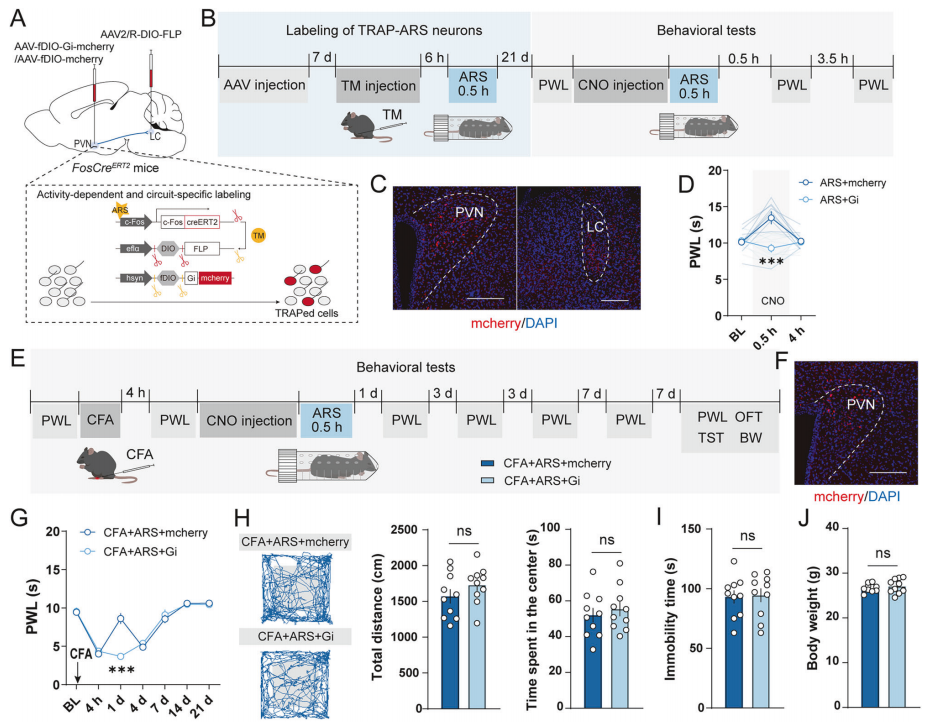
图3、下丘脑-蓝斑环路调控急性应激的缓解疼痛
总结:
本文揭示了下丘脑室旁核作为关键核团,在急性应激和慢性应激在镇痛和痛觉超敏中的具体环路机制。
参考文献
https://doi.org/10.1038/s41380-025-03144-4
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)