首页 > 医疗资讯/ 正文
罕见病虽然单一病种患者数量稀少,但全球累计患者超过4亿人,其中70%-80%由遗传因素导致。尽管过去15年基因测序技术显著提升了罕见病的诊断能力,但仍有数千种疾病的遗传机制尚未阐明。罕见病研究面临患者招募困难、资金投入不足、专业知识分散等核心挑战,导致许多患者经历漫长的"诊断之旅"仍无法确诊。模式生物(如酵母、果蝇、斑马鱼和小鼠)因其与人类基因的高度保守性、实验可操作性和成本优势,成为验证候选基因致病性、解析疾病机制和筛选治疗靶点的重要工具。然而临床基因发现与基础研究之间长期存在断层,为此加拿大罕见病模型与机制网络(RDMM)于2014年应运而生,通过建立科学家注册系统和资助评审机制,架起了临床医生与模式生物学家的合作桥梁。

在方法层面,RDMM网络构建了双向协作框架。模式生物研究人员通过注册系统详细登记其研究基因(分为已开展研究的Tier 1基因、可快速建立的Tier 2基因,以及基于基因本体论自动关联的Tier 3基因),形成覆盖10,062个人类基因的专家数据库。临床医生则提交包含候选基因和遗传证据的两页申请,经临床咨询委员会(CAC)评估后,由生物信息学核心(BIC)匹配最合适的模式生物专家。科学咨询委员会(SAC)对合作提案进行评审,中选团队将获得3万加元启动资金,整个流程仅需4周即可完成。技术实现上,注册系统采用Java Web架构,集成Spring Boot和MySQL数据库,并通过API实现跨国数据共享。该系统具有高度模块化特性,支持自定义研究领域分类和隐私分级,已被全球多个研究网络适配使用。
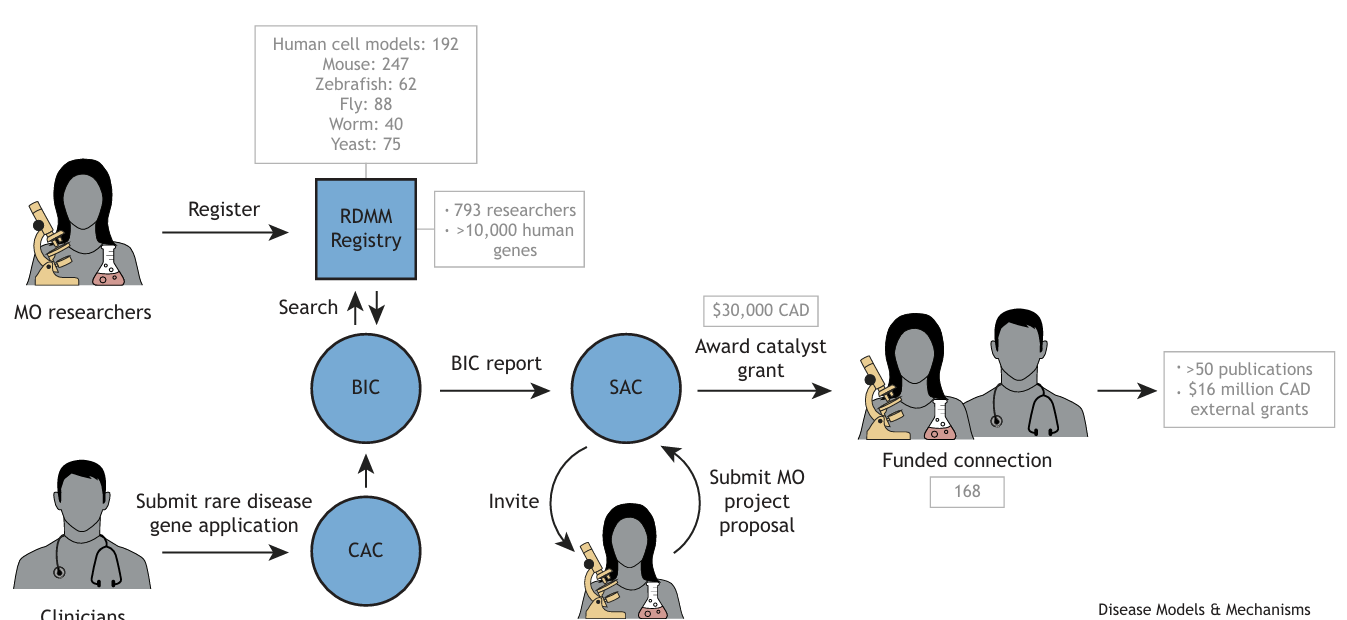
图1:加拿大罕见病模型与机制(RDMM)网络路径图
经过十年发展,RDMM网络已资助168个合作项目,其中三分之一使用小鼠模型,三分之一使用斑马鱼,其余涉及果蝇、酵母等多种模式生物。这些合作产出了50余篇科学论文,并衍生出总金额达1600万加元的后续资助项目。典型案例包括建立HARS1基因酵母模型,发现组氨酸补充可挽救特定Charcot-Marie-Tooth综合征突变型的蛋白聚集表型,为精准治疗提供依据。网络国际化进程成效显著,欧洲、澳大利亚、日本和新加坡相继建立协作节点,并与美国ModelMatcher平台实现数据互通,已完成11项跨国研究匹配。注册系统功能持续扩展,除罕见病外已应用于儿童癌症等研究领域,形成覆盖17,602个基因的全球专家网络。
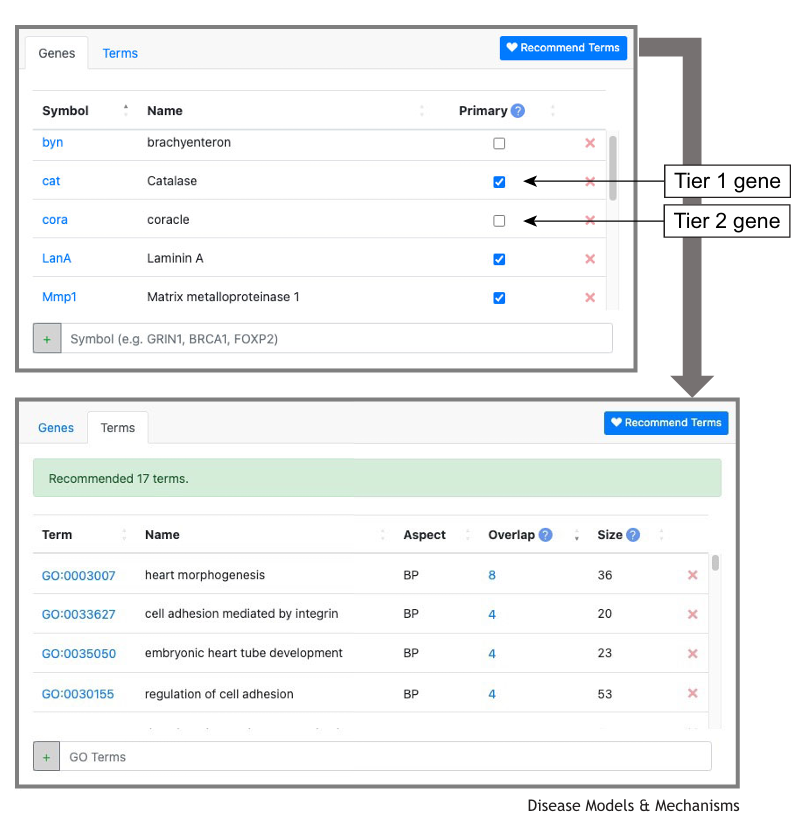
图2:RDMM注册系统中的基因录入流程
当前RDMM网络已进入第三个资助周期,其成功经验凸显三个关键要素:轻量化的快速评审机制、灵活可扩展的技术平台,以及持续的双向社区动员。未来挑战在于进一步扩大模式生物专家的注册覆盖率,并加强临床医生对协作渠道的认知。随着Solve-RD等国际项目的推进,罕见病研究正从分散走向协同,RDMM网络将继续分享其管理流程和开源软件,推动建立更多区域节点。这种全球协作模式不仅加速致病基因的功能解析,更通过整合不同模式生物的优势,为开发靶向治疗方案提供多维度研究平台,最终缩短罕见病患者的诊断与治疗等待时间。
原始出处:
Rogic, S., Poirier-Morency, G., Hister, P. & Pavlidis, P. (2025). Global partnerships in rare disease research. Disease Models & Mechanisms 18, dmm052401. doi:10.1242/dmm.052401
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)