首页 > 医疗资讯/ 正文
血管平滑肌细胞(VSMC)在维持血管稳态以及调控血压(BP)过程中发挥关键作用。其关键机制是以钙依赖的蛋白激酶MLCK和磷酸酶复合体MLCP协同调节肌球蛋白轻链MLC20 Ser19位点磷酸化,启动肌动蛋白-肌球蛋白交叉桥循环,进而介导血管收缩和舒张。细胞迁移诱导蛋白(CEMIP)在平滑肌组织中具有极高的表达水平。然而,CEMIP是否调节血管平滑肌细胞的收缩及血压尚未可知。
2025年7月1日,天津医科大学朱毅、李博川团队在Circulation Research上在线发表了题为“CEMIP Maintains Vascular Contractility by Controlling PP1c-MLC20 Cascade in SMCs”的研究论文,揭示了CEMIP作为平滑肌收缩的“Gatekeeper”,通过抑制磷酸酶复合体MLCP核心元件PP1c,进而维持MLC20磷酸化,来维持血管收缩的作用。本研究为血管平滑肌收缩维持机制以及血压调控的探索提供了新的理论依据。

CEMIP最早在人遗传性耳聋的耳蜗细胞中被发现,随后CEMIP被证明在骨关节炎、克罗恩病、软骨纤维化以及肺纤维化中起关键作用。不仅如此,在肿瘤性疾病如结肠癌、直肠癌、人乳头状瘤病毒和宫颈肿瘤病变中检测到CEMIP具有中等或高表达水平,而在正常宫颈外上皮中检测到较低水平。然而,其在心脑血管疾病中的作用尚未明确。
研究者基于生物信息学数据库,使用定量转录组学分析,对人体62种主要器官和组织的CEMIP表达情况进行检测,发现CEMIP在平滑肌中显著高表达,进而对小鼠肌性组织检测发现其高度表达在主动脉和肠系膜动脉。基于此,研究者进一步分析CEMIP在血管内膜层和中膜层的表达情况,均发现人主动脉和小鼠主动脉中的CEMIP主要存在于平滑肌细胞。为探究CEMIP是否响应平滑肌收缩和分泌表型变换,研究者观察了血清饥饿诱导的收缩表型和恢复血清诱导的分泌表型,发现CEMIP在收缩表型出现,在分泌表型时消失。但CEMIP缺失时仅下调收缩相关蛋白,而不影响分泌相关蛋白。这些结果表明,CEMIP在平滑肌中的高表达为其发挥收缩功能提供了必要条件。
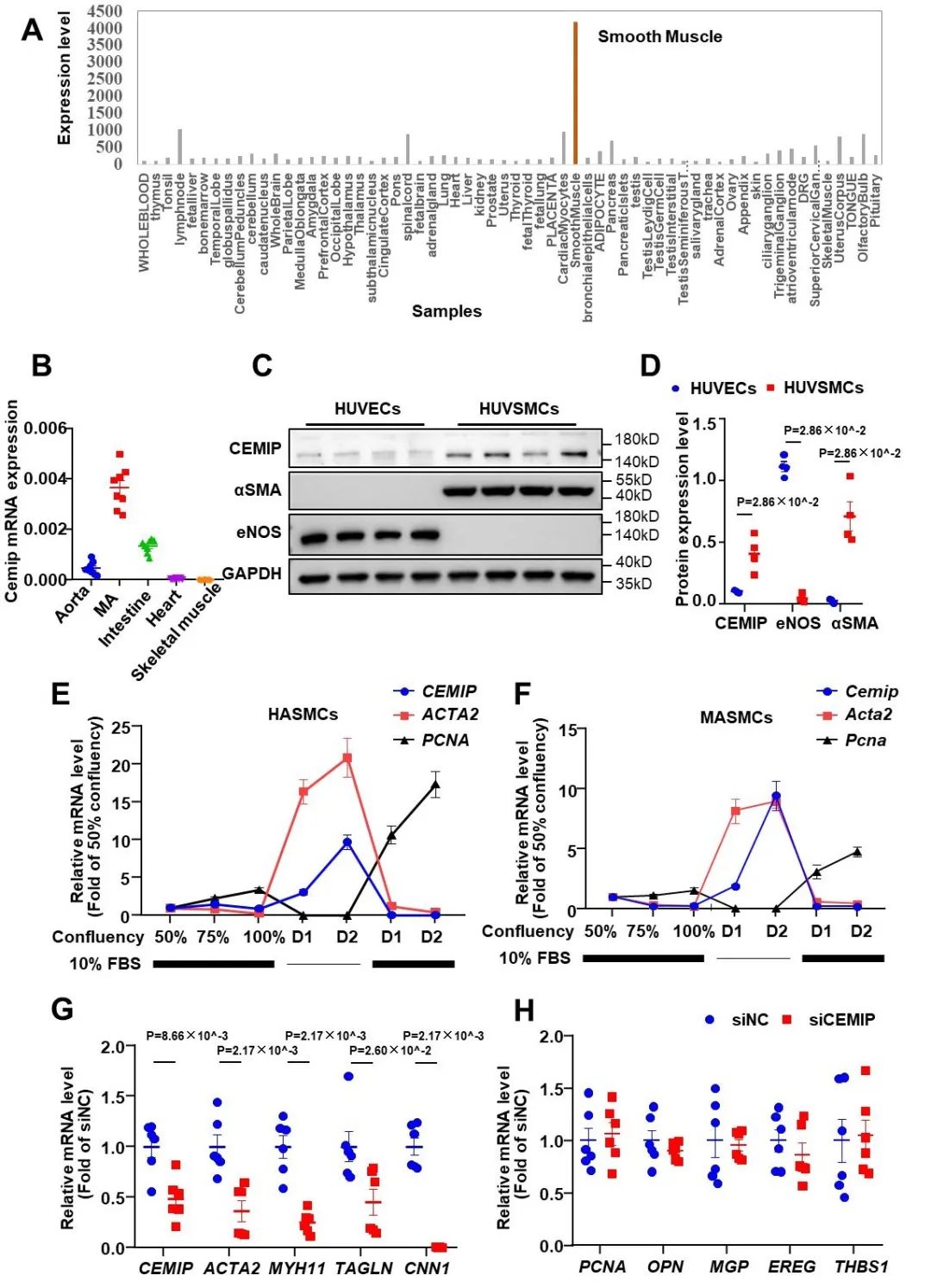
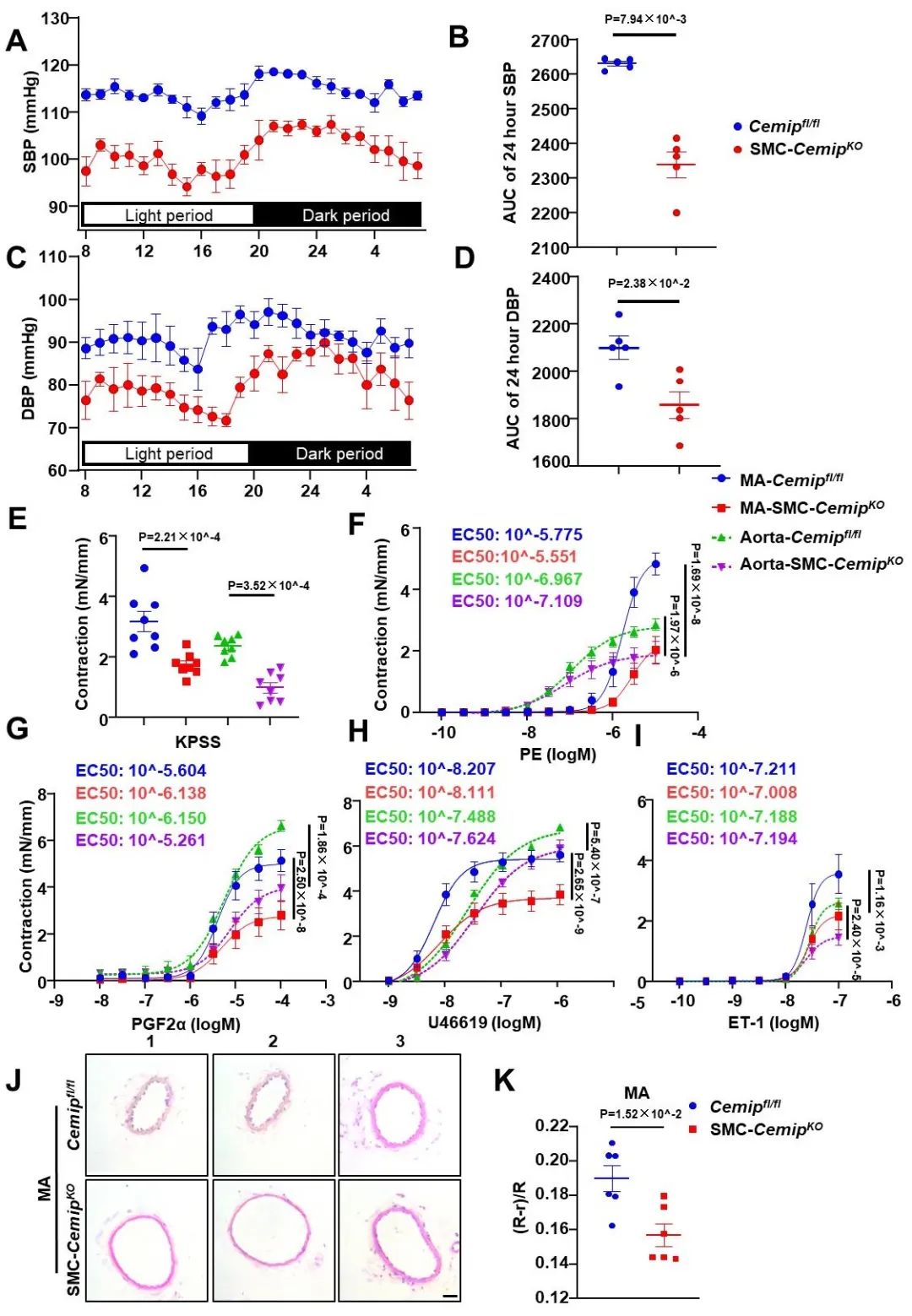
为此,研究者构建了平滑肌特异性敲除CEMIP小鼠,通过遥测监测血压发现平滑肌缺失CEMIP显著下调收缩压水平。进一步使用血管环实验证实,平滑肌细胞缺失CEMIP显著降低KPSS、PE、PGF2α、U46619和ET-1等血管收缩刺激因子诱导的血管收缩。尽管CEMIP缺失会影响主动脉收缩能力,但其收缩障碍在肠系膜动脉这样的阻力血管体现更加明显。形态学实验也证实,与CEMIP敲除小鼠的主动脉相比,其肠系膜血管的血管壁更薄弱。
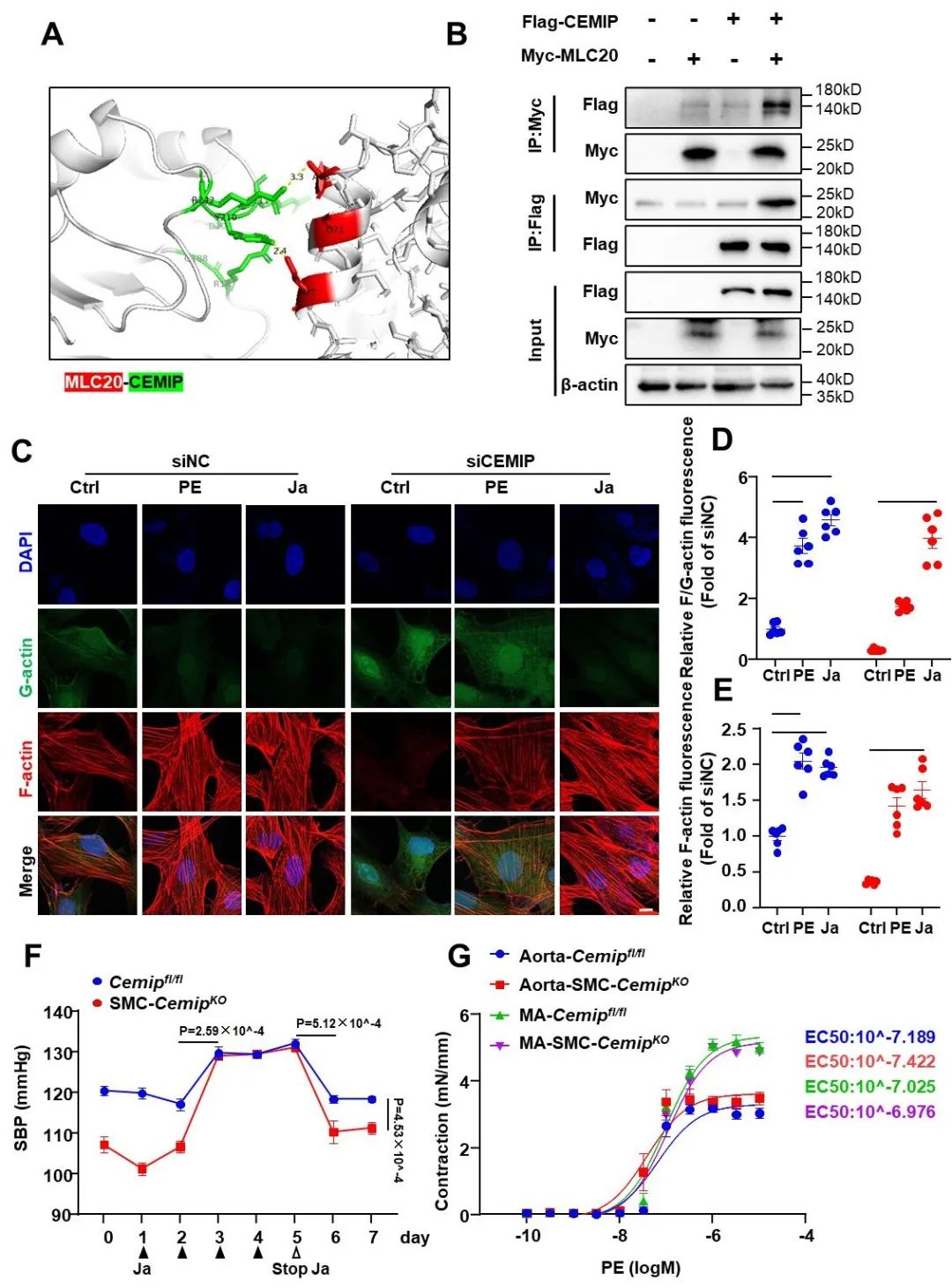
接下来,研究者在平滑肌中过表达CEMIP并进行结合蛋白组学分析,其中MLC20得分最高。结合预测分析和内外源性验证均证明,CEMIP与MLC20互相结合。F-actin聚合是MLC20介导平滑肌收缩最直接的下游反应,通过免疫荧光检测F-actin和G-actin染色发现,CEMIP敲除能够显著逆转PE介导的G-actin向F-actin转换,而给予F-actin聚合激动剂茉莉素内酯(Ja)则逆转CEMIP敲除引起的F-actin障碍。在体给予茉莉素内酯可以纠正CEMIP缺失引起的血管收缩障碍和血压下降。
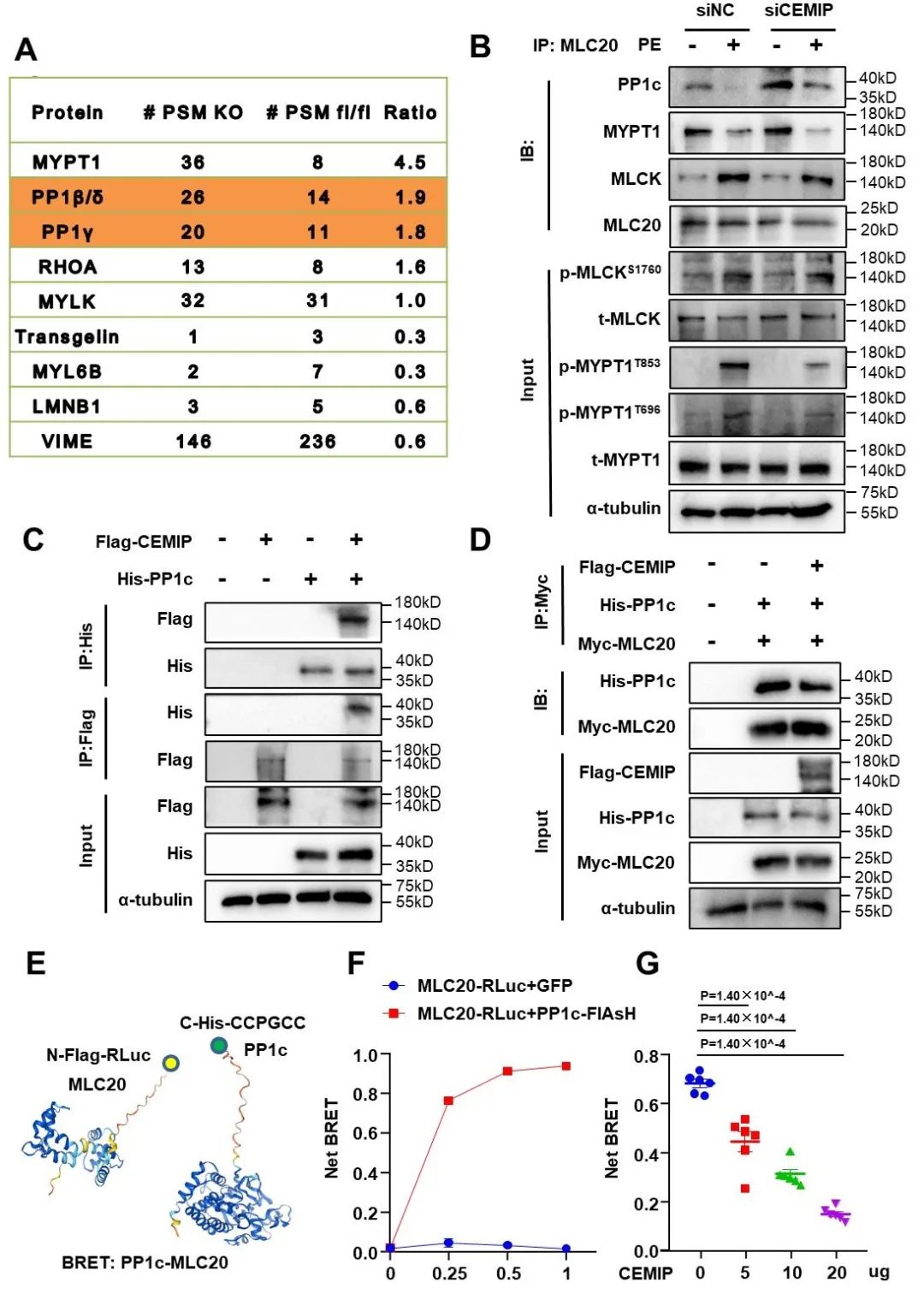
MLC20以Ca2+-CaM依赖性方式被MLCK磷酸化,并被Rho激酶调控的磷酸酶MLCP去磷酸化。研究者分离SMC-CemipKO小鼠平滑肌层,免疫共沉淀法下拉MLC20结合蛋白并进行蛋白组学分析,发现小鼠平滑肌缺失CEMIP后MLC20与蛋白磷酸酶催化亚基PP1c结合显著增加。PE诱导的PP1c与MLC20之间内源性相互作用的减少在CEMIP敲除后部分逆转,而PE诱导的MYPT1和MLCK (也称为MYLK)与MLC20的结合能力并不受到CEMIP敲低的影响。分子对接显示CEMIP N端结合MLC20,C端富含RVxF序列的部分结合PP1c,阻断PP1c与底物MLC20的接触并维持其磷酸化活性,进而促进F-actin聚合及平滑肌的收缩。CEMIP以浓度梯度依赖的方式阻断PP1γ/β亚型与MLC20的结合。
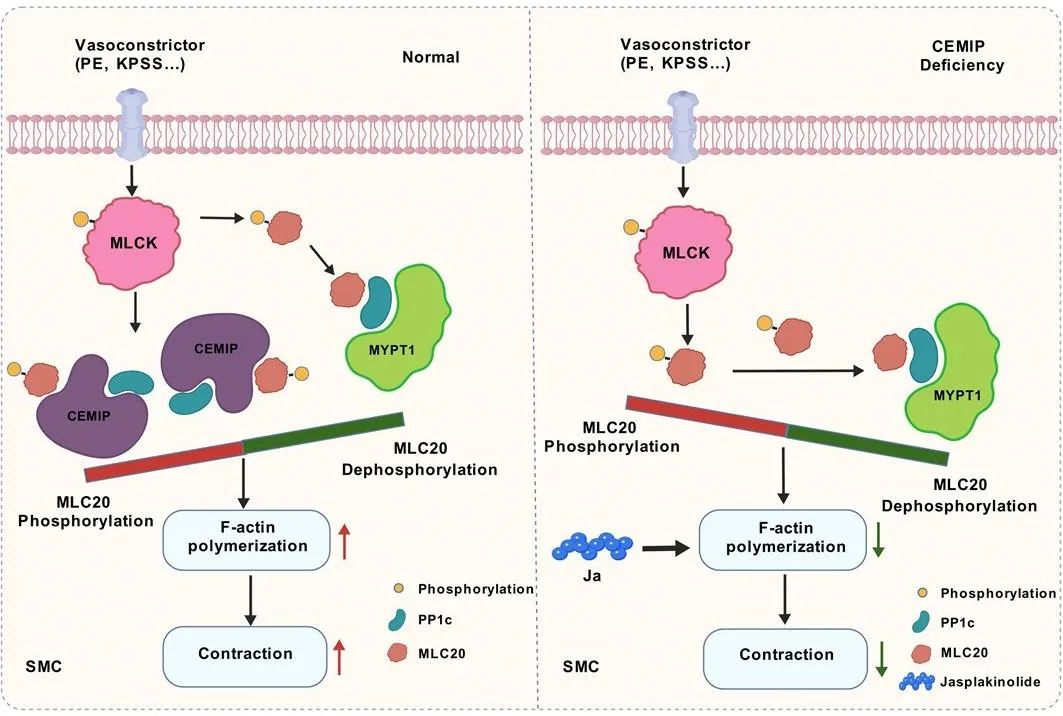
综上所述,本研究表明血管平滑肌在感受收缩刺激时(如K+、PE),收缩信号经MLCK传递至MLC20并使其磷酸化,F-actin聚合引发血管收缩。CEMIP的存在使其阻断MLC20与PP1c结合,持续磷酸化MLC20。当CEMIP缺失时,由于其不能结合PP1c并在物理上阻隔PP1c对MLC20的去磷酸作用,使血管收缩发生障碍并引起血压下降。外源性补充茉莉素内酯可以有效缓解CEMIP敲除引起的血压下降。
天津医科大学遗传学系李博川副教授以及病理生理学系朱毅教授为本文通讯作者。天津医科大学医学生理学专业袁泽博士研究生为论文第一作者。该课题是与北京大学基础医学院崔庆华教授与天津医科大学张锴教授合作共同完成,得到了国家自然科学基金重点项目以及面上项目等项目的支持。
原文链接:
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.125.326233
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)