首页 > 医疗资讯/ 正文
维生素E(vitamin E,VE)近年来被证实具有抗血管生成、抑制肿瘤增殖和调节免疫功能等多种抗癌特性。2025年5月28日,华中科技大学张志平教授及孔丽教授团队在《ACS Nano》期刊发表了一篇题为“Iterative Screening of Vitamin E-Based Functional Lipid Nanoparticles for mRNA Delivery”的论文。该研究创新性地将维生素E引入可电离脂质结构中,开发出一种名为VN2C1的脂质纳米颗粒(Lipid nanoparticles,LNP),用于mRNA药物的递送。在多种结肠癌模型(包括皮下肿瘤、腹膜转移和肝转移模型)中实现肿瘤抑制乃至治愈,并能显著增强PD-L1免疫检查点抑制剂的疗效,将原本免疫原性较低的“冷肿瘤”转变为免疫原性较高的“热肿瘤”,从而提升肿瘤对免疫治疗的响应。

研究团队巧妙地以维生素E分子作为可电离脂质的疏水尾部核心,通过精细调控N原子周围的空间位阻以及连接键的长度等关键结构参数,成功开发出一系列新型功能脂质分子VNxCyOz。经三次迭代优化后得到了最优的可电离脂质结构及其组分比例。
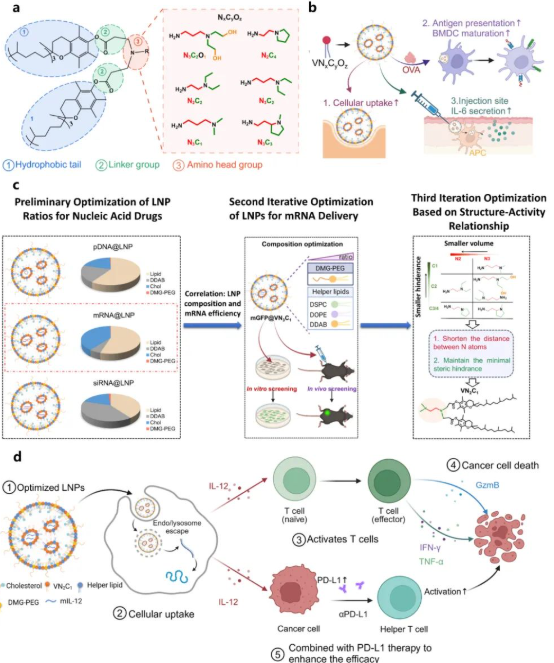
新型功能脂质分子VNxCyOz材料库及迭代优化思路
与传统商用脂质纳米颗粒(如SM102)相比,VNxCyOz LNP的细胞摄取效率显著提高了约1.8倍,这一提升主要归功于VE的引入。此外,研究者通过将VNxCyOz LNP与卵清蛋白及骨髓来源的树突状细胞共孵育,发现VNxCyOz LNP能够显著促进树突状细胞的成熟以及抗原肽的表达。这些结果表明,VNxCyOz LNP不仅在mRNA递送效率上表现出色,还具有激活免疫系统、增强抗原呈递的潜力,为免疫治疗提供了新的策略。
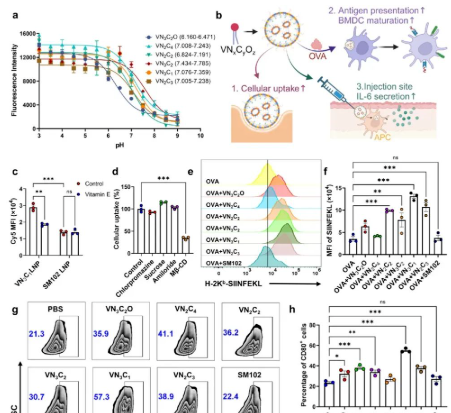
VNxCyOz LNP增强细胞摄取,促进 DC 成熟和抗原呈递
研究者进一步探索了VN2C1 LNP在包封mIL-12时的疗效,并在多种结肠癌模型中进行了系统评估。实验结果显示,在皮下瘤模型中,使用mIL-12@VN2C1 LNP治疗的小鼠,其疗效优于单独使用IL-12蛋白或mIL-12@SM102 LNP的对照组。在结肠癌肝转移模型中,通过全身给药的mIL-12@VN2C1 LNP几乎完全抑制了肝脏转移瘤和脾脏原发肿瘤的生长。此外,在结肠癌腹膜转移模型中,mIL-12@VN2C1 LNP也展现出良好的治疗效果,除一只小鼠外,其余所有小鼠均实现了完全治愈。在整个治疗过程中,未观察到IL-12全身给药通常伴随的体重下降等不良反应。
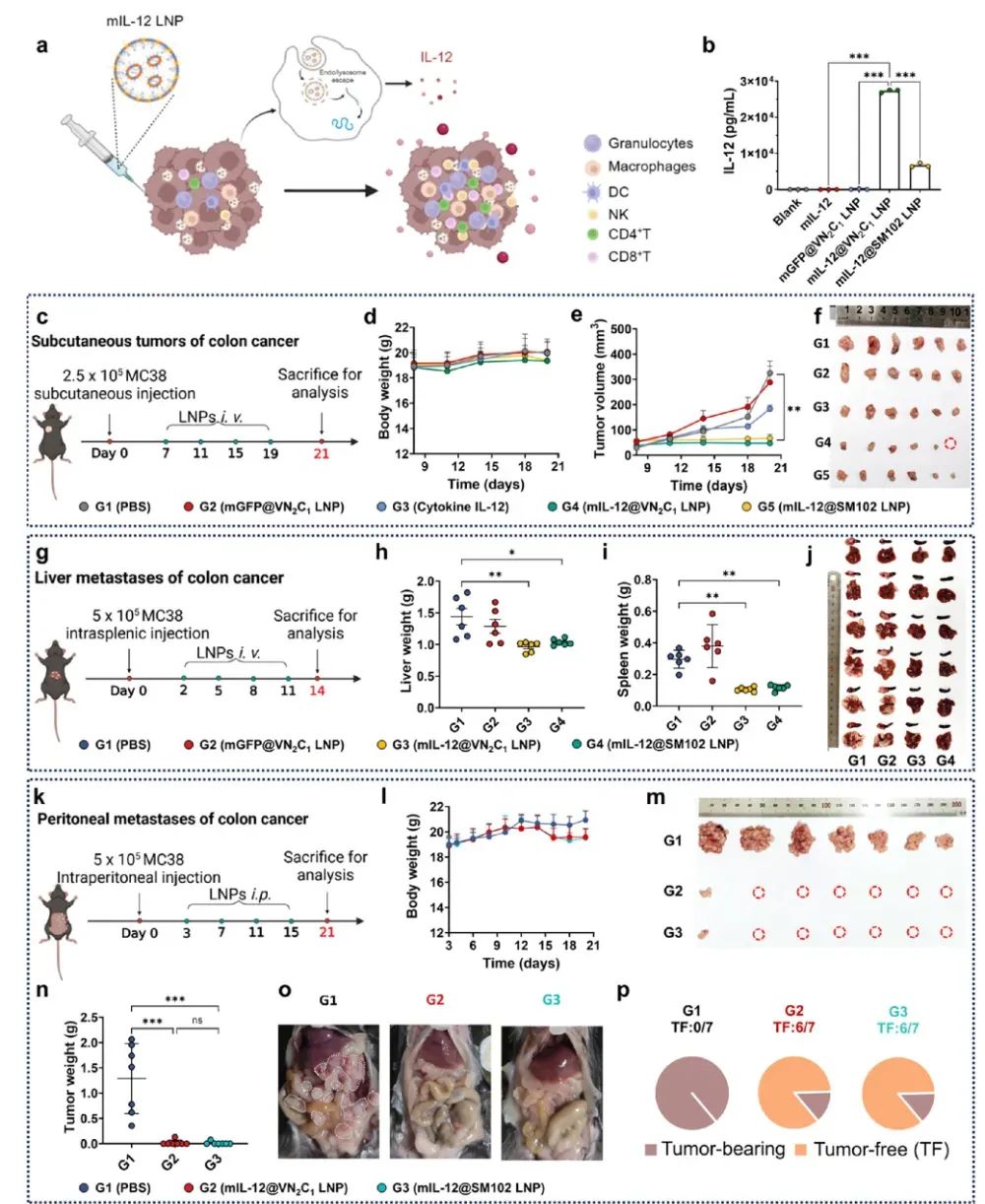
mIL-12@VN2C1 LNP在多种结肠癌模型中的抗肿瘤疗效
研究者探索了mIL-12@VN2C1 LNP与PD-L1阻断疗法的联合治疗效果。实验结果表明,联合治疗显著促进了树突状细胞(DC)的成熟,诱导CD8⁺T细胞分化,增强了肿瘤组织中免疫细胞的浸润,提升了T细胞总数、CD4⁺T细胞和CD8⁺T细胞数量,并显著提高了促炎性细胞因子IFN-γ和TNF-α的分泌以及颗粒酶B的表达。
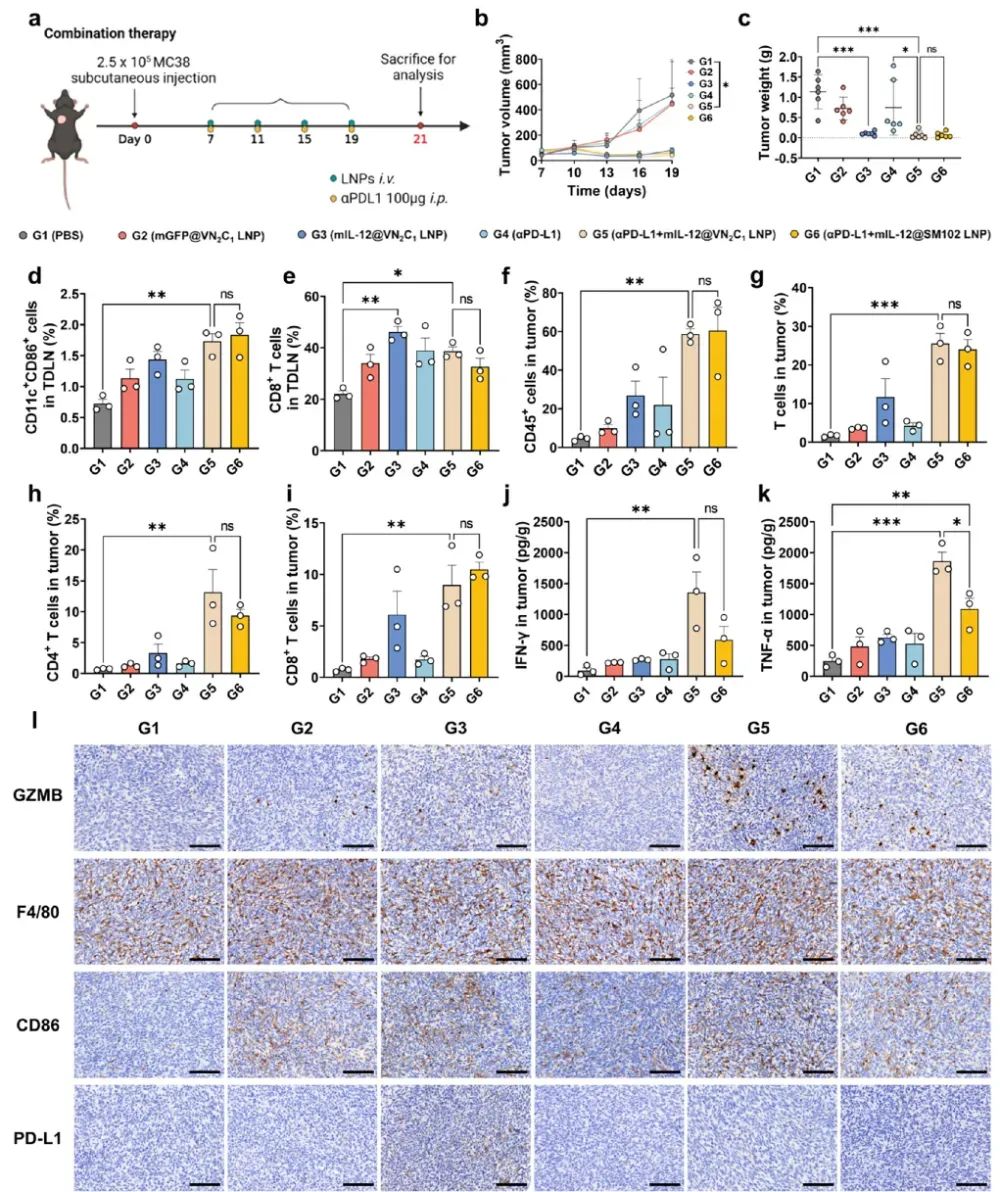
mIL-12@VN2C1 LNP与PD-L1阻断疗法的联合治疗效果及机制研究
这些结果进一步证实了树突状细胞在免疫检查点阻断疗法中的重要作用,尤其是在增强抗肿瘤免疫反应方面。联合治疗通过促进树突状细胞成熟和激活CD8⁺T细胞,显著增强了肿瘤微环境中的免疫活性,为提高免疫检查点阻断疗法的疗效提供了新的策略。
总的来讲,本研究通过引入基于VE的可离子化脂质,开发出一种高效的mRNA递送系统。这种VE衍生LNP不仅能够高效递送mRNA,还具有激活免疫系统的潜力。在多种结肠癌模型中,该系统展现出显著的抗肿瘤效果,通过递送mIL-12实现了肿瘤的完全缓解。此外,与PD-L1阻断疗法联合应用时,能够实现协同治疗效果,进一步增强抗肿瘤免疫反应。这种基于VE的LNPs具有强大的临床应用潜能,有望推动功能性核酸递送平台在癌症治疗领域的发展。
药学院2023级博士崔可鑫为论文第一作者,药学院张志平教授、孔丽教授为论文共同通讯作者,该项工作得到武汉市重点研发计划、国家自然科学基金等项目的支持。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.5c01378
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)