首页 > 医疗资讯/ 正文
摘要
本研究对2例伴有3-甲基戊二酸尿症的全身型肌张力障碍的患者(系姐妹)进行了临床表型分析及基因检测。通过病史采集、影像学及实验室检查,基因学分析,发现2例患者6号染色体上的Serac1基因存在纯合突变c.1687T>C该突变位点位于第16外显子,此前以青少年期起病的全身型肌张力障碍为主要临床表型的Serac1基因突变尚未在文献中报道。本研究首次发现Serac1该位点突变可引起全身型肌张力障碍,并可能为未来类似病例的诊断和治疗提供参考。
Serac1基因位于6q25.3,编码丝氨酸活性蛋白1,该蛋白负责磷脂酰甘油重塑,对线粒体功能和细胞内胆固醇运输起到至关重要的作用。该基因纯合或复合杂合突变可引起一系列临床表型,其中最典型的是MEGDHEL综合征(3-methylglutaconic aciduria,dystonia-deafness,hepatopathy,encephalopathy,Leigh-like syndrome),该病的典型表现为3-甲基戊二酸升高伴耳聋、脑病、肝炎及Leigh综合征,在两个家系中表现为痉挛性截瘫,3例患者表现为成人发病的全身型肌张力障碍。本文报告2例Serac1基因新突变位点导致青少年起病,以全身型肌张力障碍为主要症状并伴有3-甲基戊二酸尿的女性病例,以供参考。
1 临床资料
1.1 病例资料
患者1,女,12岁。因“姿势异常2年余”于2023年12月就诊于北京协和医院神经科门诊,2年前逐渐出现双上肢不自主向后扭动,腿不自主屈曲及躯干向右侧扭转,在站立时腿不能伸直,并在1年内病情逐渐发展行走能力逐渐下降,言语困难,口周不自主运动。门诊就诊时已完全失去行走能力,双上肢舞蹈样运动,无法闭口,不自主流涎,偶有咬舌,无生长发育迟缓,听力正常,检查观察到患者眼动充分,病理征阴性。患者1出生时为足月顺产,生长发育里程碑与同龄人并无差异,发病前学习成绩中等,无智力发育异常。
患者1父母既往体健并且否认近亲结婚,父母育有3女1子,患者1为第4个孩子,大女儿与患者1临床症状相似,10岁起出现不明原因姿势异常,并且1年内病情迅速进展,16岁因不明原因去世;二儿子体健,三女儿(患者2)出现较轻微的运动症状。患者家系图谱见图1。
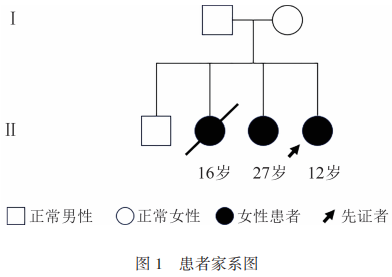
患者2,女,27岁,与患者1临床表现相似,但症状较轻微,17岁时出现了双下肢活动困难及手部活动异常,1年内症状加重并出现行走困难以及低音发音困难,此后10年内症状无进展,就诊时仍保留有行走及语言功能,患者2为足月顺产,生长发育里程碑无异常,发病前为高中学生,无智力发育异常。
1.2 检查检验
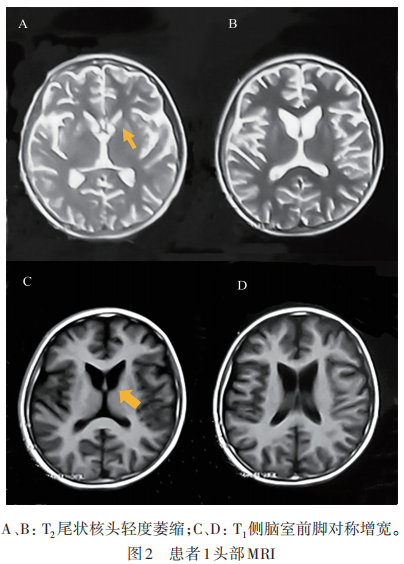
头部MRI可见患者1侧脑室前脚增宽,壳状核轻度萎缩(见图2)。
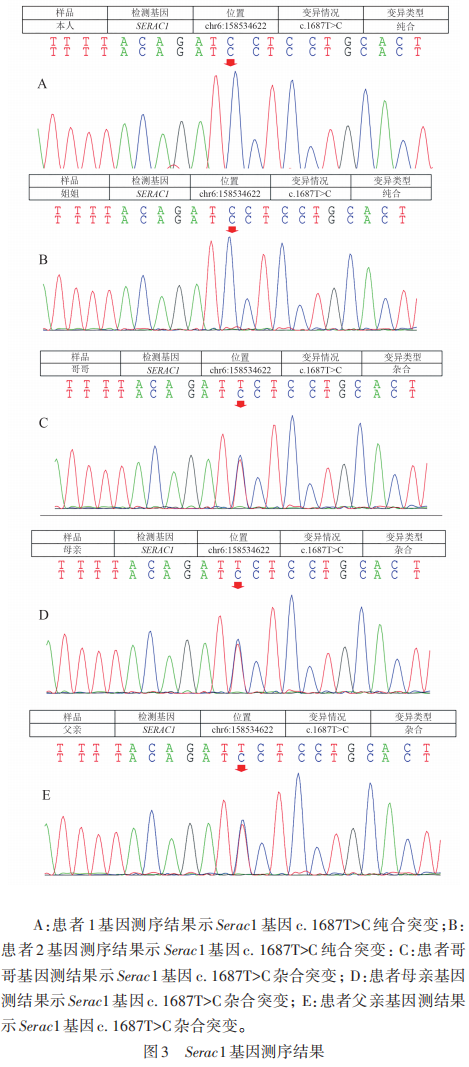
基因检测:收集患者家系外周静脉血并对其进行全外显子基因测序,结果发现在2例患者的Serac1基因中发现了一个未曾报道过的错义突变位点,导致纯合致病性Serac1基因变异 (NM_032861: c.1687T>C)(见图3)。根据《ACMG遗传变异分类标准与指南》,该位点变异被认为“likely pathogenic”(可能致病的),该位点ACMG证据链为PM1+PM2+ PP3_Moderate。Serac1基因中c.1687T>C突变在正常人基因库esp6500、千人基因组、ExACMAX、gnomADMAX均未发现。该错义突变分别来自父母双方两个携带者,错义变异对蛋白质结构/功能REVEL:0.804,该突变与MEGDHEL综合征相关。
对2例患者进行尿有机酸检测,检测出3-甲基戊二酸、3-甲基戊烯二酸含量均升高(患者1的3-甲基戊二酸含量 5.2,患者2的3-甲基戊二酸含量 8.3,参考值0.0~3.0;患者1的3-甲基戊烯二酸含量 7.0,患者2的3-甲基戊烯二酸含量 9.3, 参考值0.0~4.0)。血常规、血细胞形态学分析、肝肾功能检测、同型半胱氨酸检查、甲状腺功能检查铜蓝蛋白检查均无异常。
1.3 诊断
Serac1基因突变导致的全身型肌张力障碍。
1.4 治疗及预后
针对患者运动症状,予巴氯芬(10 mg 3次/d),苯海索(2 mg 2次/d)及氯硝西泮(2 mg 1次/d)。1月后随访2例患者,姿势异常症状稍改善;针对患者线粒体功能缺陷,加用辅酶Q10(10 mg 3次/d)及甲钴胺(0.5 mg 3次/d),1月后再次随访未见明显症状改善。
2 讨论
Serac1编码一种包含丝氨酸脂肪酶结构域的蛋白质位于线粒体相关膜组分中线粒体和内质网之间的界面,该蛋白是PGAP样蛋白结构域家族的成员,是磷脂酰甘油重塑的关键参与者,参与将磷脂酰甘油-34:1 (PG-34:1)重塑为磷脂酰甘油-36:1 (PG-36:1),对磷脂交换线粒体功能和细胞内胆固醇运输至关重要。该基因纯合或复合杂合突变引起功能缺陷较为罕见,发病率约为9/10 000 000,Wortmann等于2006年报道首例病例,目前已报道案例不超过100例。该基因突变可引起不同的疾病表型,较为常见的MEGDHEL综合征是线粒体疾病的一个亚型,该疾病显示出线粒体疾病的典型表现和进展过程,包括乳酸性酸中毒和3-甲基戊二酸(3-MGA)尿。MEGDHEL综合征一般在婴儿期起病,以听力障碍、肝功能障碍、喂养困难为起病症状,几乎所有个体都出现发育迟缓,全身性肌张力减退,脊柱侧弯,智力障碍,MEGDHEL综合征头部MRI主要表现为基底节区对称性异常信号,伴有小脑萎缩。除MEGDHEL综合征外,Serac1基因突变在两个家系中表现为青少年发病的伴有轻度智力障碍的复杂性遗传性痉挛性截瘫;在3个病例中表现为成年期起病的全身型肌张力障碍。以运动障碍为主要表现的Serac1功能缺陷患者除3-MGA-尿外,无典型MEGDHEL综合征表现。表现为遗传性痉挛性截瘫的两个家系患者临床表现为轻度认知障碍,青少年期起病出现缓慢进行性的下肢痉挛状态,头部MRI显示壳核及尾状核轻度萎缩;3例全身型肌张力障碍患者均表现为轻度认知障碍,成年早期出现进行性全身性多动性运动障碍。
在本文中,2例患者均于青少年期起病,除3-MGA-尿外,其余症状为姿势异常,不自主运动,发音困难,行走障碍,患者1头部MRI显示侧脑室前脚增宽,壳状核轻度萎缩,并未与此前报道Serac1功能缺陷病例具有相同的临床表现。值得注意的是2例患者突变位点相同,但疾病表现并不相似,患者2疾病表现及病情进展均较患者1轻微,但患者2尿液中的3-MGA含量较患者1高,似乎3-MGA的代谢情况与临床表现的严重程度并不相关。
尚无针对Serac1突变所致疾病的有效治疗方法,疾病管理方案旨在提供适当的支持性治疗。针对运动症状的药物治疗,如巴氯芬,左旋多巴等在少量患者中报告有效,针对口周不自主运动及过度流涎可联合肉毒毒素注射治疗。针对线粒体功能改善的“复合维生素鸡尾酒疗法”,例如含有辅酶Q10、核黄素和生物素的治疗并未被广泛推广,疗效尚不明确。本文中,2例患者使用巴氯芬、苯海索及氯硝西泮,姿势异常症状稍有缓解,1月后加用辅酶Q10及维生素B12未见明显疗效。
以青少年起病的全身型肌张力障碍为主要临床表现的Serac1基因缺陷尚无报道。我们目前的病例丰富了该疾病的临床表型,增加了Serac1基因突变范围,并强调该病因作为全身型肌张力障碍的病因诊断。
参考文献
[1]Tan J, Wagner M, Stenton SL, et al. Lifetime risk of autosomal recessive mitochondrial disorders calculated from genetic databases[J]. EBioMedicine, 2020, 54:102730.
[2]Maas RR, Iwanicka-Pronicka K, Ucar SK, et al. Progressive deafness-dystonia due to SERAC1 mutations:a study of 67 cases[J]. Ann Neurol, 2017, 82(6):1004-1015.
[3]Roeben B, Schüle R, Ruf S, et al. SERAC1 deficiency causes complicated HSP:evidence from a novel splice mutation in a large family[J]. J Med Genet, 2018, 55(1):39-47.
[4]Yan D, Chen S, Cai F, et al. Complicated hereditary spastic paraplegia caused by SERAC1 variants in a Chinese family[J]. Front Pediatr, 2021, 9:816265.
[5]Ashton C, Davis M, Laing N, et al. Novel SERAC1 variant presenting with adult-onset extrapyramidal dystonia-Parkinsonism phenotype:a case report[J]. Neurol Genet, 2023, 9(2):e200067.
[6]Finsterer J, Scorza FA, Fiorini AC, et al. MEGDEL syndrome[J]. Pediatr Neurol, 2020, 110:25-29.
[7]Wortmann SB, Vaz FM, Gardeitchik T, et al. Mutations in the phospholipid remodeling gene SERAC1 impair mitochondrial function and intracellular cholesterol trafficking and cause dystonia and deafness[J]. Nat Genet, 2012, 44(7):797-802.
[8]Wortmann S, Rodenburg RT, Huizing M, et al. Association of 3-methylglutaconic aciduria with sensori-neural deafness, encephalopathy, and Leigh-like syndrome (MEGDEL association) in four patients with a disorder of the oxidative phosphorylation[J]. Mol Genet Metab, 2006, 88(1):47-52.
[9]林晓霞,林希,严争,等. SERAC1基因变异致MEGDEL综合征2例并文献回顾[J]. 中华医学遗传学杂志,2023,40(9):1100-1106.
[10]Wortmann SB, de Brouwer APM, Wevers RA, et al. SERAC1 Deficiency [A]//Adam MP, Feldman J, Mirzaa GM, et al. GeneReviews® [M]. Seattle (WA):University of Washington, Seattle; 1993-2024.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)