首页 > 医疗资讯/ 正文
慢加急性肝衰竭(ACLF)具有潜在可逆性,需要精细化的临床分型以实现精准诊治和分类管理。基于国内外最新研究成果及临床实践,中华医学会肝病学分会重型肝病与人工肝学组、中华医学会肝病学分会终末期肝病营养与再生学组组织国内有关专家联合编写了我国首部ACLF诊治指南——《慢加急性肝衰竭诊治指南(2025年版)》(以下简称《指南》),旨在为临床实践中ACLF患者的诊断、治疗和个体化管理提供指导意见。
近期,首都医科大学附属北京佑安医院陈煜教授对《指南》要点进行解读。肝胆相照平台特将精华内容整理成文,供临床医生参考。
一 ACLF定义
目前在世界范围内,关于ACLF的定义众多但不尽相同,阻碍了相关研究数据的可比性,也给临床医生在诊治和管理ACLF时带来困惑。
表1 国际ACLF定义比较
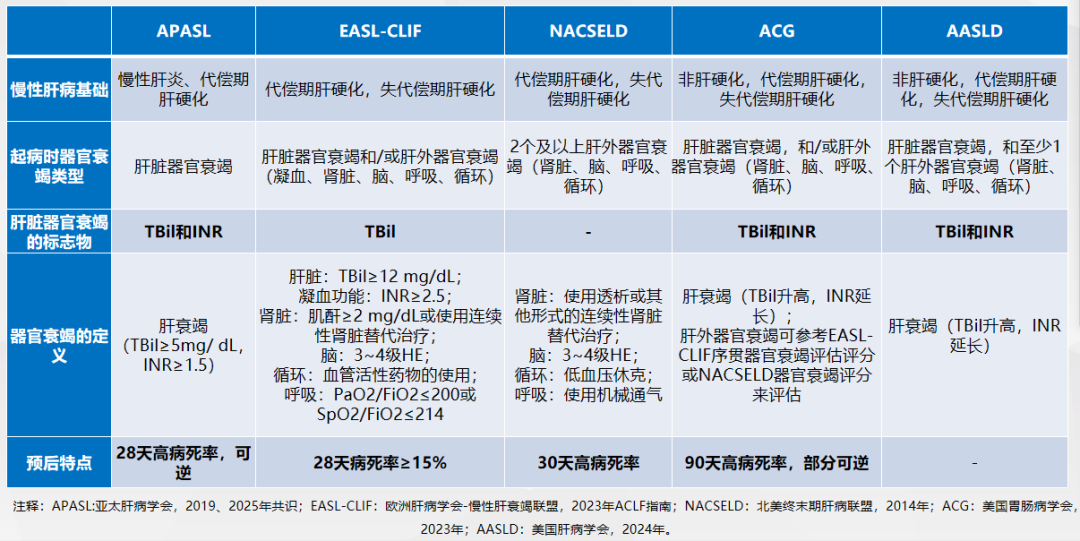
纵观上述定义,不同学会/组织对ACLF定义之间的差异在于慢性肝病基础(有无肝硬化、有无失代偿)、器官衰竭类型(肝脏衰竭和肝外器官衰竭)、器官衰竭定义、预后特点(高病死率、可逆性)。不同的ACLF定义导致诊断标准的不同,一些临床干预性研究因采用的诊断标准不同导致结果的差异,影响了ACLF相关研究结果的可比性及疾病的精准诊治,缩小这些差异或统一诊断标准是亟需解决的问题。
《指南》兼顾全球不同地区ACLF定义标准,确保定义的精确性和全面性,结合我国现状、临床实践经验及循证医学证据,提出相对统一的ACLF定义,即:ACLF是发生在慢性肝病基础(非肝硬化、代偿期肝硬化、失代偿期肝硬化)上的急性肝功能衰竭,表现为胆红素升高和凝血功能障碍,伴或不伴肝外器官功能衰竭,短期病死率高。
二 ACLF疾病负担
全球范围内,每年约有200万人因肝病死亡,占所有死亡人数的4%,绝大多数死于慢性肝病及其并发症。我国人口基数大,约有3.4~4.8亿慢性肝病患者,肝脏疾病负担沉重,而ACLF是造成慢性肝病患者死亡的主要原因之一。
三 ACLF病因
近年来,随着社会、经济、医疗水平等因素影响,以及抗HBV药物、乙型肝炎疫苗的普遍应用,我国ACLF患者慢性肝病的病因构成正在发生变迁,HBV感染占比逐渐减少,但目前仍占主导地位;代谢相关脂肪性肝病、酒精性肝病、自身免疫性肝病、药物性肝损伤比例逐年增加。
表2 ACLF常见病因分类

四 ACLF组织病理学表现
ACLF病理特征可表现为在慢性肝病病理损伤基础上,发生新旧程度不等的肝细胞亚大块坏死性病变,部分患者可伴有汇管周围的小胆管增生。有肝硬化基础的患者,部分硬化结节结构仍然存在。
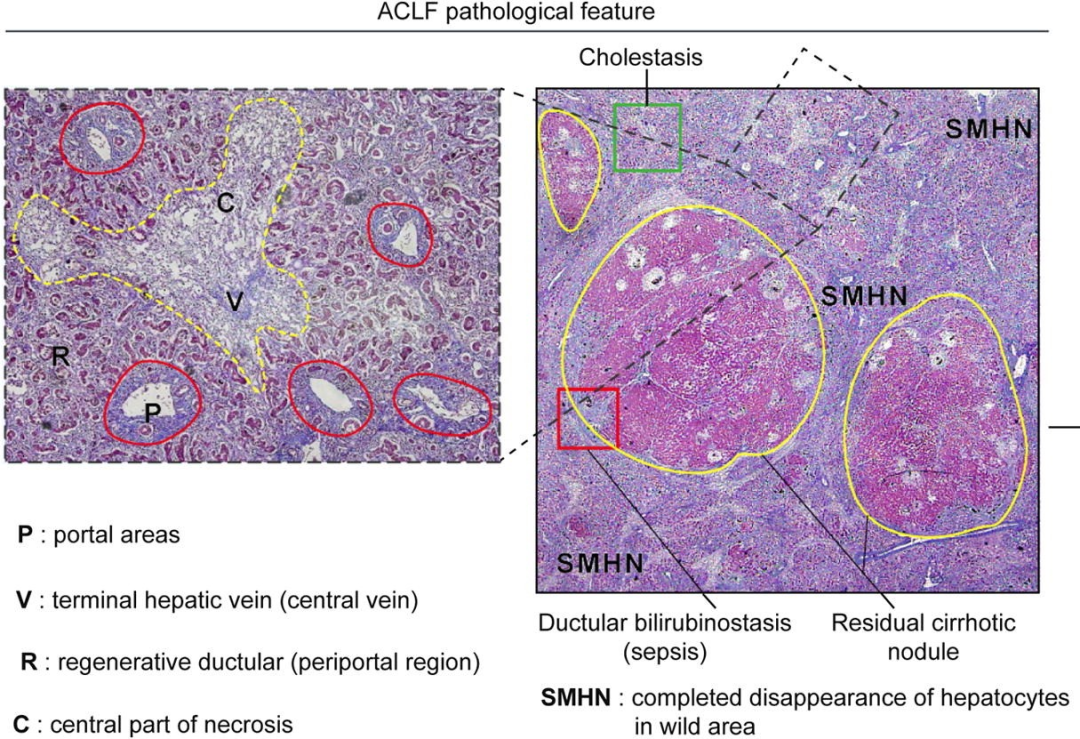
图1 ACLF病理特征
需要注意的是,由于ACLF患者的肝病基础(非肝硬化/肝硬化)、病因及诱因不同,病理检查提示肝细胞坏死的比例和程度可存在一定的差异。图2左为APASL-ACLF(慢性肝炎和代偿期肝硬化基础)病理特征,在此类人群中,2/3的患者肝脏组织病理学表现为肝细胞坏死和/或肝纤维化,且超过1/3的患者表现为严重肝细胞坏死;图2右为EASL-ACLF(代偿期和失代偿期肝硬化基础)病理特征,在此类人群中,88.5%患者表现为重度肝纤维化,仅37.5%患者出现肝细胞坏死。
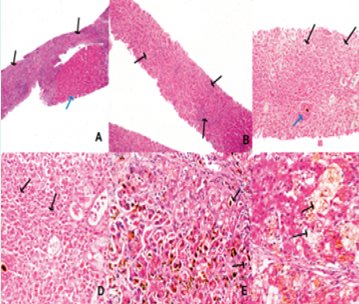
图2 APASL-ACLF与EASL-ACLF病理特征
五 ACLF诊断
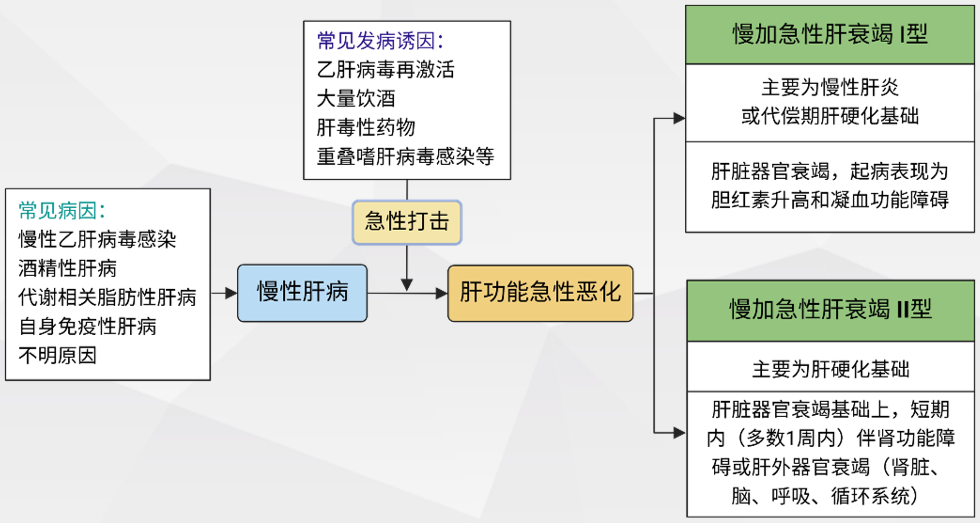
图3 ACLF诊断流程
根据起病时临床表现,可将ACLF分为2种类型:ACLF I型和ACLF II型。
ACLF I型为慢性肝病(主要为慢性肝炎或代偿期肝硬化)基础上的急性严重肝损伤,患者出现:
➤ 总胆红素升高,TBil≥12mg/dl(205.2μmol/L)或每日升高≥1mg/dl(17.1μmol/L);
➤ 凝血功能障碍(INR≥1.5或PTA≤40%)。
达到以上标准时患者可能未出现肝外脏器衰竭,但在病情进展中可出现感染、肝性脑病、腹水、消化道出血、急性肾损伤等并发症或肝外器官衰竭。
ACLF I 型在疾病演变过程中,可分为早期、中期和晚期:
➤ 早期:
(1) 可出现明显乏力、厌食、呕吐和腹胀等严重消化道症状;
(2) ALT和/或AST升高,黄疸进行性加深,TBil≥12mg/dl(205.2μmol/L)或每日上升≥1mg/dl(17.1μmol/L);
(3) 凝血功能障碍,30%<PTA≤40%(1.5≤ INR<1.9)。
➤ 中期:在肝衰竭早期表现基础上,病情进一步发展,T Bil持续上升;凝血功能障碍,20%<PTA≤30%(1.9≤INR<2.5)。
➤ 晚期:在肝衰竭中期表现基础上,PTA≤20%(INR≥2.5);或病情进一步加重,出现严重出血倾向、3~4级HE、肾功能衰竭等严重并发症。
另外,对于未达到ACLF I 型诊断标准,但出现以下肝衰竭倾向表现者,可诊断为ACLF前期(Pre-ACLF),须引起高度重视,并进行积极处理:
(1)出现明显乏力、厌食、呕吐和腹胀等严重消化道症状;
(2)ALT和/或AST大幅升高,黄疸进行性加深,5mg/dl(85.5μmol/L)≤ TBil<12mg/dl(205.2μmol/L);
(3)凝血功能障碍,PTA进行性下降但>40%(INR<1.5)。
ACLF II 型大多数在肝硬化基础上(代偿期或失代偿期)出现急性肝功能失代偿,患者出现:胆红素明显升高、凝血功能障碍(INR≥1.5或PTA≤40%),短期内(多数在1周内)出现肾功能障碍,1.5mg/dl(132.6μmol/L)≤肌酐<2.0 mg/dL(176.8μmol/L),或肝外器官功能衰竭(包括肾脏、脑、呼吸和循环系统),器官衰竭诊断标准参考EASL-CLIF。
根据肾功能障碍或肝外器官衰竭情况,ACLF II 型可分为早期、中期、晚期:
➤ 早期:肝硬化急性肝功能失代偿出现TBil明显升高和凝血功能障碍(INR≥1.5或PTA≤40%),合并肾功能障碍,1.5mg/dl(132.6μmol/L)≤肌酐<2.0 mg/dl(176.8μmol/L)。
➤ 中期:肝硬化急性肝功能失代偿,合并1个肝外器官衰竭(肾脏、脑、呼吸和循环系统)。
➤ 晚期:肝硬化急性肝功能失代偿,合并2个及以上肝外器官衰竭(肾脏、脑、呼吸和循环系统)。
六 ACLF预后评估
陈煜教授指出,基于器官衰竭特征的临床分型,不但对弥合东西方ACLF分歧具有积极的意义,同时对临床实际诊疗管理ACLF也具有非常重要的价值。
ACLF I型以肝脏器官衰竭表现起病,诊断初期可采用MELD评分、MELD-Na评分、APASL-AARC评分,病程进展过程中出现肝外器官衰竭,可联合使用COSSH-ACLF II评分、CLIF-C ACLF评分、NACSELD器官衰竭评分。
ACLF II型在起病时即表现为肝脏衰竭合并肝外器官功能障碍或衰竭,应联合应用MELD评分、MELD-Na评分、COSSH-ACLF II评分、CLIF-C ACLF 评分和NACSELD器官衰竭评分等多种预后评分。临床诊疗过程中,应对ACLF病情进行动态评估(每3-7天),以指导治疗决策。
另外,传统临床指标构建的预后模型大多基于单一时间点的结局(存活、死亡或肝移植),新的动态预后分型对ACLF病程进行了分阶段(4周、12周)评估,并精准细化了多种结局(存活、死亡或肝移植、肝衰竭状态),为构建更精准的预后预测模型提供了新思路,可作为一种新的预后评估参考依据。
七 ACLF治疗
目前ACLF的治疗措施主要包括3个方面:内科综合治疗、人工肝治疗、肝移植治疗。
1. 内科综合治疗
• 一般支持治疗:包括卧床休息、病情监护、纠正低蛋白血症、监测实验室指标、消毒隔离等;
• 营养评定、支持治疗及随访管理:①营养评定;②营养支持治疗;③营养随访管理;
• 对症治疗:①抗炎护肝药物的应用;②微生态调节治疗应用;③免疫调节剂的应用;
• 病因治疗:明确肝衰竭病因对指导治疗及判断预后具有重要价值,包括查明发病原因及诱因两类;
• 并发症的内科综合治疗:感染、腹水、脑水肿、肝性脑病、急性肾损伤等并发症可参考相关指南或共识。
2. 非生物型人工肝支持治疗
• 适应证:①各种原因引起的ACLF前、早、中期患者,部分晚期患者;②肝移植术前等待肝源、肝移植术后出现排异反应、移植肝无功能期的患者。
• 相对禁忌证:①严重活动性出血或弥散性血管内凝血者;②对治疗过程中所用血制品或药品如血浆、肝素和鱼精蛋白等严重过敏者;③血流动力学不稳定者;④心脑梗死非稳定期者。
• 治疗时机选择:对于ACLF前、早及中期患者,建议在针对病因及发病诱因等治疗的基础上,尽早开始人工肝治疗;对于晚期患者,因其并发症多、总体预后差、人工肝治疗风险大,应详细评估风险,治疗前应做好充分准备(包括各种应急预案),同时积极寻求肝移植的机会。
• 治疗模式选择:①胆红素水平显著升高时,可将不同作用机制的血液净化模式进行组合;②凝血功能严重障碍时,治疗模式应含有使用外源性血浆的治疗模式,如PE、PDF;③存在比较明显的HE时,建议治疗模式包含DPMAS、PDF或HDF,尽量避免单独PE;④存在肾功能不全、电解质/酸碱失衡时,建议治疗模式包含HDF或PDF;需要脱水时,建议治疗模式包含HF、HDF。
• 常用组合模式:DPMAS+PE、PE+HDF、HDF+DPMAS、PDF+PP、PE+PP+HDF等。在临床实际应用时,综合考虑选择最合适的人工肝组合模式,联合增效或扬长避短,以期取得更好的治疗效果,减少不良反应和并发症的发生。
治疗频率:建议根据ACLF的分型(分期)、病情进展速度等确定。
3. 肝移植治疗
对于ACLF I 型患者,可采用MELD评分评估肝移植人群;若病情进展,伴发肝外器官衰竭或ACLF II型患者,建议联合应用CLIF-C ACLF评分。对于经3-7天内科治疗,病情未控制或进一步恶化,但不超过3个器官衰竭或CLIF-C ACLF<64分的患者应优先移植;3个及以上器官衰竭或CLIF-C ACLF≥64分患者,应每天监测,当器官衰竭情况改善或评分下降时(器官衰竭数量≤3或CLIF-C ACLF< 64分),可再次行肝移植评估。
对于合并急性呼吸窘迫综合征、不可重建血运的严重冠心病的患者,应谨慎选择肝移植。
另外,随着医疗技术的发展,肝移植的适应证逐渐扩大,部分以往被视为禁忌的情况如今已不再绝对禁忌。多学科综合诊治可更精准地筛选肝移植适宜患者,更合理利用医疗资源。
八 ACLF未满足的临床需求及展望
ACLF未满足的临床需求及未来的研究重点包括:
1. 深入探索发病机制:需深入探索系统性炎症、免疫反应及肝细胞再生等相关机制。
2. 研究新型治疗技术:干细胞治疗、生物型人工肝、细胞或肝脏类器官移植及3D打印技术等新型治疗技术。
3. 开发靶向治疗药物:如白细胞介素-22、粒细胞集落刺激因子(G-CSF)、Toll样受体-4 (TLR4)拮抗剂等均有相关初步研究,但需进一步探索。
4. 优化综合管理模式:将基础与临床融合,临床多学科联合、医工交叉创新的合作,多维度协同临床研究和政策支持,优化肝移植供体分配机制等。
5. 借助大数据及人工智能等技术:精准的早期预警和预后判断对于疾病的发展、转归及结局至关重要,需进一步基于我国多中心的前瞻性大样本队列,利用疾病发展不同阶段的多组学、多模态数据资料,借助大数据及人工智能等技术的发展,构建临床简便实用的预警预测体系;制订国内外广泛认可的统一的ACLF诊断标准等。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)