首页 > 医疗资讯/ 正文
缺血性心肌病(ICM)是冠状动脉粥样硬化导致长期心肌缺血的晚期病理转归,其特征为心肌弥漫性纤维化及收缩功能障碍。随着冠心病发病率持续攀升,ICM已成为威胁人类健康的重大临床难题。近年研究表明,心脏巨噬细胞异常活化与扩增在心肌损伤及心室负性重构中发挥关键作用,其来源主要包括外周循环CCR2+单核细胞的募集分化与胚胎来源驻留巨噬细胞(CD206+/CD163+表型)的局部增殖。研究证实,心脏CCR2+巨噬细胞的数量与心衰患者左室负性重构呈显著正相关性,靶向抑制CCR2+单核细胞向心脏组织的趋化迁移,可有效改善心梗(MI)小鼠的心室重构,提示CCR2信号通路作为慢性心衰治疗靶标的潜在价值。然而,对于驻留巨噬细胞亚群的活化增殖机制及其在慢性缺血性心衰心室重构中的调控作用尚未阐明。
2025年5月1日,武汉大学中南医院王琼昕研究员团队与圣路易斯华盛顿大学Sumanth D. Prabhu教授团队合作在Circulation杂志发表了题为“CD206+IL-4Rα+ Macrophages Are Drivers of Adverse Cardiac Remodeling in Ischemic Cardiomyopathy"的研究论文,证实在慢性缺血性心衰进程中,心脏CD206+IL-4Rα+巨噬细胞亚群的病理扩增及其分泌的FIZZ1分子,通过激活促纤维化信号通路,显著加剧左室重构与心肌纤维化进程。该研究团队进一步通过靶向干预实验证明,阻断IL-4Rα信号通路可有效抑制该巨噬细胞亚群的活化增殖,从而改善心室重构并延缓心功能恶化。该发现不仅深化了对ICM病理机制的理解,更为开发靶向巨噬细胞亚群的精准治疗提供了重要理论依据,具有显著的临床转化价值。

研究团队首先通过流式细胞术对MI后2天、1周、2周、4周及8周小鼠心脏巨噬细胞的数量及亚群进行分析,发现巨噬细胞数量呈现双相性动态变化:损伤后2天达到峰值,在随后的2周内下降,继而持续再扩增至8周(慢性心衰左室重构期),此时巨噬细胞占心脏白细胞总数约63% (140,000个细胞/心脏),较假手术组增加约9倍。对巨噬细胞亚群观测发现心脏CD206+巨噬细胞在MI后持续扩增,约占MI 8周后巨噬细胞总数的85%。CD206+巨噬细胞具有增殖活性,主要表现为CCR2-、MHC IIhi,并与左室功能障碍及心肌纤维化相关。近半数CD206+巨噬细胞表达IL-4Rα,且CD206+IL-4Rα+巨噬细胞通过DLL-4/Jagged1-Notch1信号通路的激活高表达促纤维化因子FIZZ1。
为阐明CD206+IL-4Rα+巨噬细胞在心脏病理性重构中的调控机制,研究人员对正常小鼠进行不同亚群巨噬细胞的心肌原位移植(图1),实验结果显示:IL-4诱导型巨噬细胞(M[IL-4], CD206+IL-4Rα+)能特异性引发进行性心功能减低,其特征性病理改变包括心肌细胞肥大与凋亡以及间质纤维化形成。进一步追踪实验证实:①供体来源巨噬细胞在受体心脏中可持续驻留长达4周,其中M[IL-4]组细胞存留量显著高于M0 (未极化)及IL-10诱导型巨噬细胞(M[IL-10], CD206+IL-10Rα+)组(p<0.01);②仅M[IL-4]组可触发宿主原位CD206+巨噬细胞的扩增,且该细胞群主要富集于心肌纤维化病灶区。上述结果为CD206+IL-4Rα+巨噬细胞亚群在驱动心脏损伤和纤维化进程中的核心作用提供了直接证据。
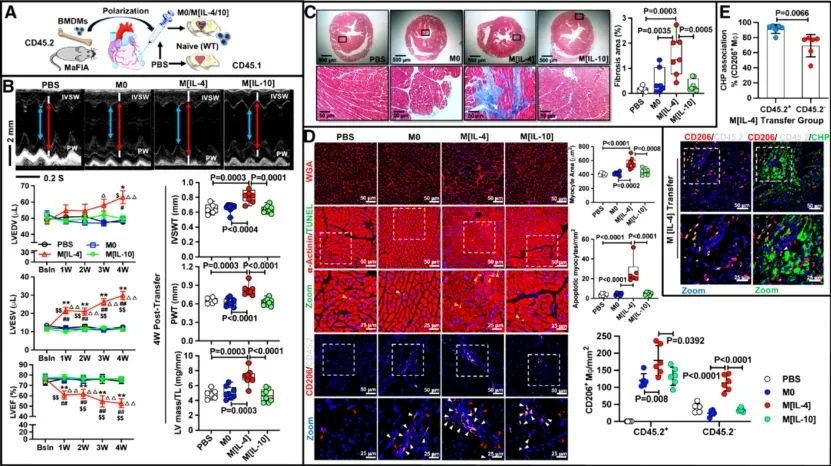
图1. 心肌原位移植IL-4诱导型巨噬细胞(CD206+IL-4Rα+)诱发心功能减退及心肌纤维化
为进一步明确CD206+IL-4Rα+巨噬细胞对慢性心衰心室负性重构的促进作用,研究人员于MI后4周,对IL-4Rαf/fLysM-CreERT2进行髓系特异性IL-4Rα敲除(图2)。结果显示:①持续6周的诱导性敲除可显著抑制心衰心脏CD206+巨噬细胞的增殖(p<0.01),并有效清除CD206+IL-4Rα+巨噬细胞亚群。②慢性心衰髓系IL-4Rα敲除可抑制左室重构、改善心功能、减少心肌纤维化,同时促进新生血管形成(微血管密度增加)。这一研究证实CD206+IL4Rα+巨噬细胞作为心衰心脏中异常扩增的关键髓系细胞亚群,可驱动心脏炎症反应进展以及病理性重构、纤维化及心功能恶化,且IL-4Rα的表达对该巨噬细胞亚群高增殖性特征起决定性作用。
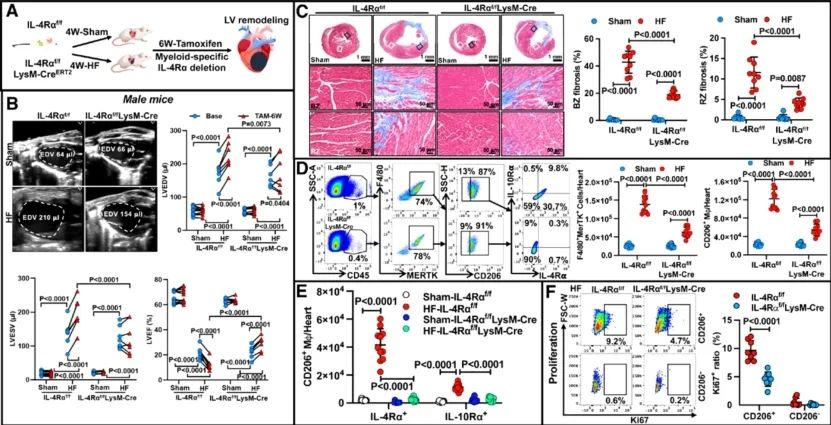
图2. 髓系特异性IL-4Rα基因敲除抑制慢性心衰心脏CD206+巨噬细胞扩增及左室重构
为验证巨噬细胞IL-4Rα信号轴作为心力衰竭治疗靶点的可行性,本研究采用靶向IL-4Rα mRNA的优化型反义寡核苷酸(ASO)实现体内特异性基因沉默(图3)。在MI后4周的心衰小鼠中,IL-4Rα基因抑制可特异性清除心脏CD206+IL-4Rα+巨噬细胞亚群,多维度地改善心衰病理进程:①左心室重构显著逆转;②心肌肥厚及纤维化降低(p<0.01)伴新生微血管密度增加;③左室射血分数显著提升;④心脏局部炎症因子水平下调伴随全身系统性炎症减低。
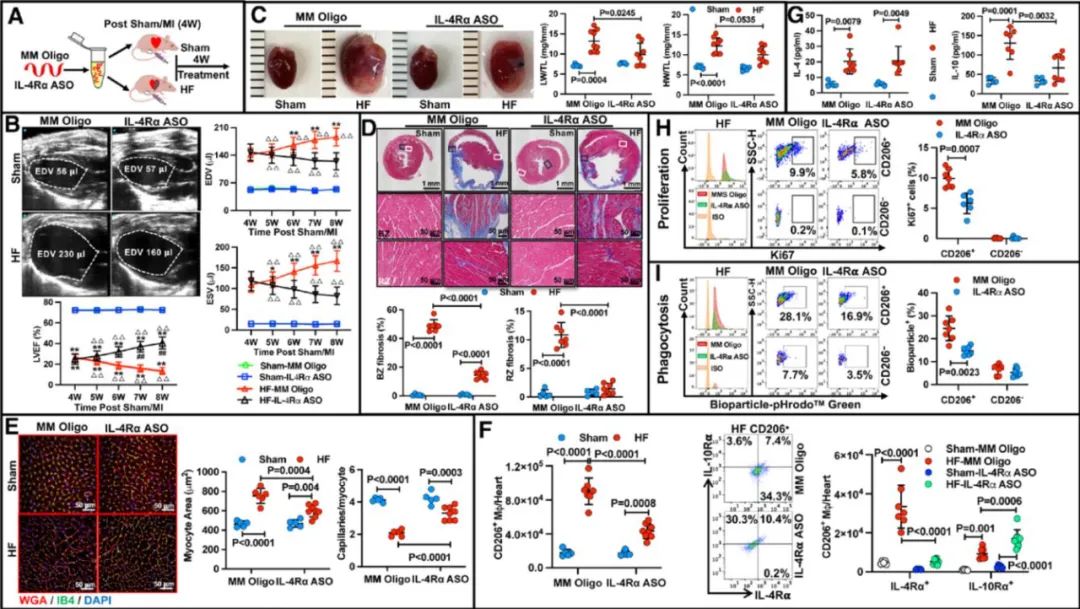
图3. 在体IL-4Rα表达抑制可清除心衰心脏CD206+巨噬细胞亚群及逆转左室重构
为进一步评估靶向CD206+巨噬细胞IL-4Rα信号通路在慢性心衰治疗中的转化价值,本研究取得以下关键发现(图4):①心衰患者心脏组织中CD206+/CD163+驻留巨噬细胞亚群显著扩增,且其扩增程度与心肌纤维化进展呈正相关;②该亚群中超过60%的CD163+巨噬细胞持续性高表达IL-4Rα及其下游效应分子FIZZ3 (FIZZ1的人类同源蛋白)。
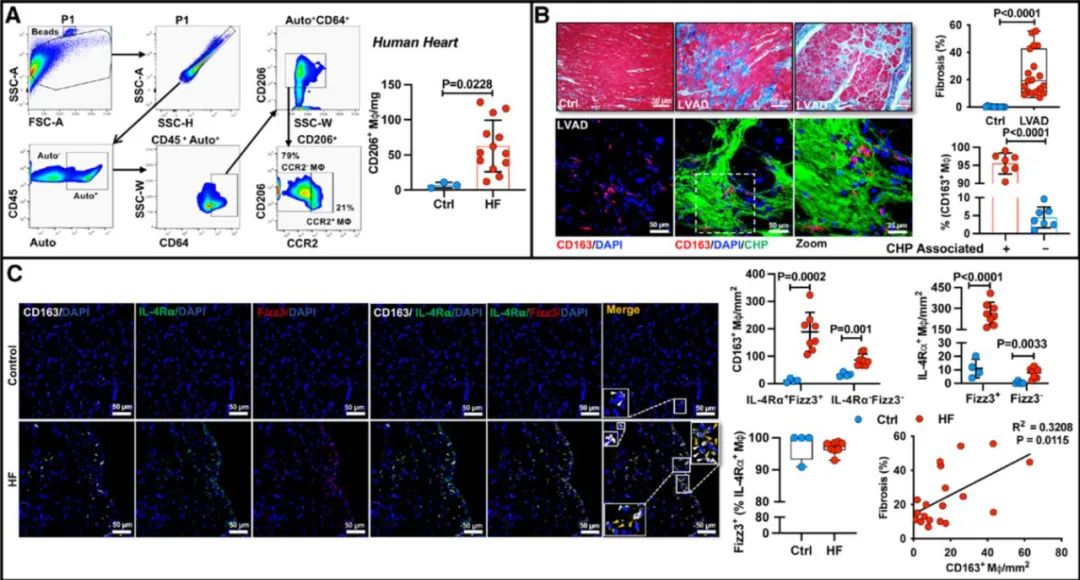
图4. CD206+/CD163+巨噬细胞在心衰患者心脏显著扩增,并高表达IL-4Rα和FIZZ3,且与心机纤维化正相关
综上所述,本研究首次阐明了CD206+IL-4Rα+巨噬细胞通过FIZZ1分泌驱动慢性缺血性心衰心室重构的病理机制,而特异性阻断IL-4Rα-FIZZ1信号轴可显著逆转心肌纤维化进程,为缺血性心肌病提供了具有临床转化潜力的治疗靶点。该发现不仅解析了巨噬细胞亚群在ICM中的异质性调控作用,更为开发基于免疫微环境调控的精准治疗策略奠定了分子理论基础。
该研究由圣路易斯华盛顿大学Sumanth D. Prabhu教授(通讯作者)与武汉大学中南医院王琼昕研究员(第一作者)共同主导完成。研究团队依托中美两国高水平科研平台,获得美国国家卫生研究院(NIH) 3项R01项目及中国国家自然科学基金1项(面上项目)的联合资助。
原文链接:
https://www.ahajournals.org/doi/full/10.1161/CIRCULATIONAHA.124.072411
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)