首页 > 医疗资讯/ 正文
【论著】
本研究对芬太尼蛛网膜下腔麻醉后大鼠脊髓背根神经节(DRG)中微RNA(miRNA)表达进行测序,探讨其可能的麻醉机制。
1 材料与方法
选择5~6周龄雄性SD大鼠6只,采用随机数字表法分为生理盐水组(N组)和芬太尼组(F组),每组3只。N组和F组分别于蛛网膜下腔注射生理盐水20 μl或等体积芬太尼。两组大鼠于给药前后用60 g和100 g的von Fray纤维丝测定机械缩足频率(PWF),0 ℃铝板测定冷缩足潜伏期(PWL);提取大鼠脊髓DRG进行miRNA测序(miRNA‑seq),筛选差异表达基因;根据测序结果进行miRNA筛选、聚类分析,在此基础上通过韦恩图筛选出芬太尼蛛网膜下腔注射对DRG作用的关键miRNA,并对关键miRNA进行基因本体(GO)分析、京都基因和基因组百科全书(KEGG)通路分析等,完成靶基因预测。
2 结果
2.1 两组大鼠PWF和PWL比较
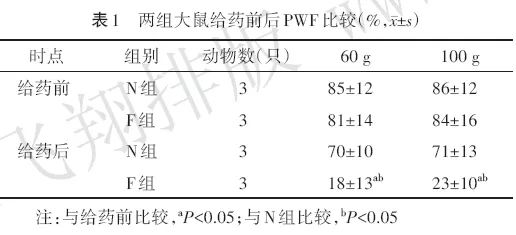
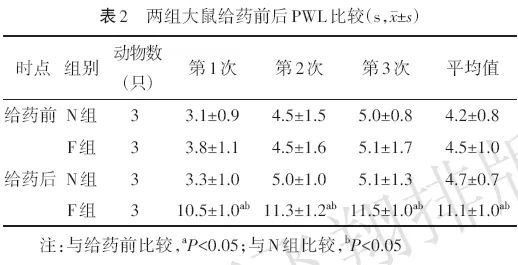
与给药前比较,给药后F组大鼠60 g和100 g纤维丝PWF均较低(均P<0.05),3次PWL及平均值均较长(均P<0.05);N组大鼠PWF和PWL给药前后差异无统计学意义(均P>0.05)。见表1、表2。
两组大鼠给药前60 g和100 g纤维丝PWF,3次PWL及平均值差异均无统计学意义(均P>0.05);给药后F组大鼠60 g和100 g纤维丝PWF低于N组(均P<0.05),3次PWL及平均值长于N组(均P<0.05)。见表1、表2。

2.2 miRNA‑seq结果
测序得到的原始序列含有接头序列或低质量序列,为了保证信息分析的准确性,需要对原始数据进行质量控制,得到高质量序列: ① 去除接头; ② 去除短于18个或长于30个核苷酸的序列; ③ 对于每个样本,将质量值低的序列去掉; ④ 去除未知碱基N(N为无法识别的碱基)含量≥10%的Reads。测序数据产出统计见表3。
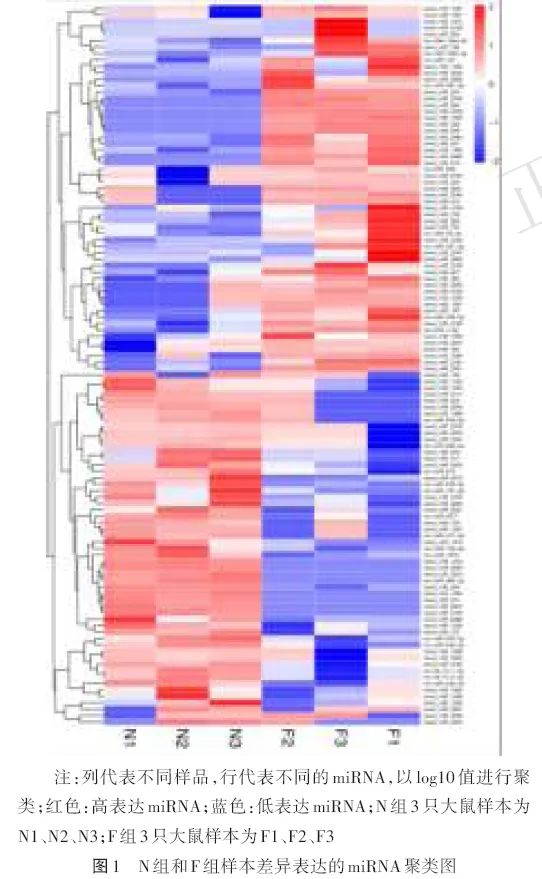
2.3 差异表达基因
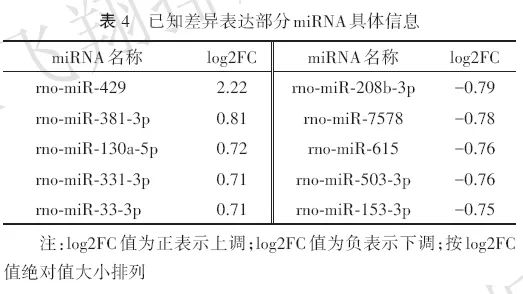
在确认测序结果质量可靠性的基础上,对筛选出的差异表达miRNA做层次聚类分析,将具有相同或相似表达行为的miRNA进行聚类,差异表达miRNA聚类结果见图1。使用“edgeR”R语言包对各组样本间差异miRNA进行筛选,显著差异表达筛选标准|logFC|>1.5且P<0.05。据此识别出在芬太尼蛛网膜下腔麻醉后大鼠DRG中显著上调基因58种,显著下调基因54种(图2)。其中上调中新预测miRNA为49个,已知miRNA为9个;下调中新预测miRNA为39个,已知miRNA为15个(表4)。

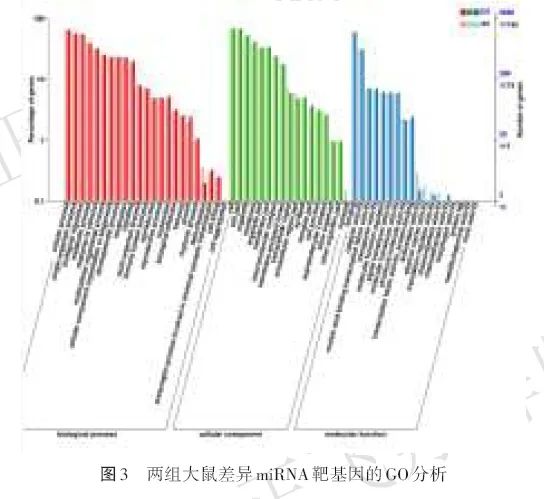
2.4 差异表达miRNA靶基因的GO功能分析
靶基因GO富集分析显示,差异表达的miRNA与离子跨膜转运的调节、钙释放通道活性、神经元投射发育、泛素蛋白转移酶活性的负调节、T细胞受体信号通路、磷酸核糖代谢过程、对皮质酮的反应、蛋白质同源寡聚化、轴突延伸、细胞凋亡过程的调节等显著相关(图3)。
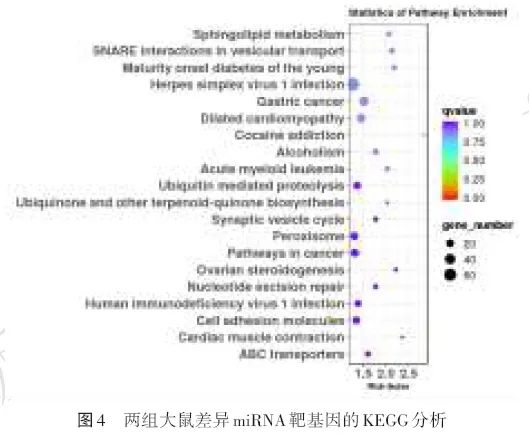
2.5 差异表达miRNA靶基因KEGG通路功能分析及富集分析
芬太尼蛛网膜下腔麻醉miRNA靶基因的KEGG主要通路涉及胃癌、囊泡运输中的可溶性N‑乙基马来酰亚胺敏感因子附着蛋白受体(SNARE)[与降钙素基因相关肽(CGRP)分泌相关]相互作用、青少年成熟期糖尿病、单纯疱疹病毒1型感染、扩张型心肌病、急性粒细胞白血病、可卡因成瘾、酗酒、鞘脂代谢等(图4)。
2.6 差异蛋白中的候选蛋白筛选
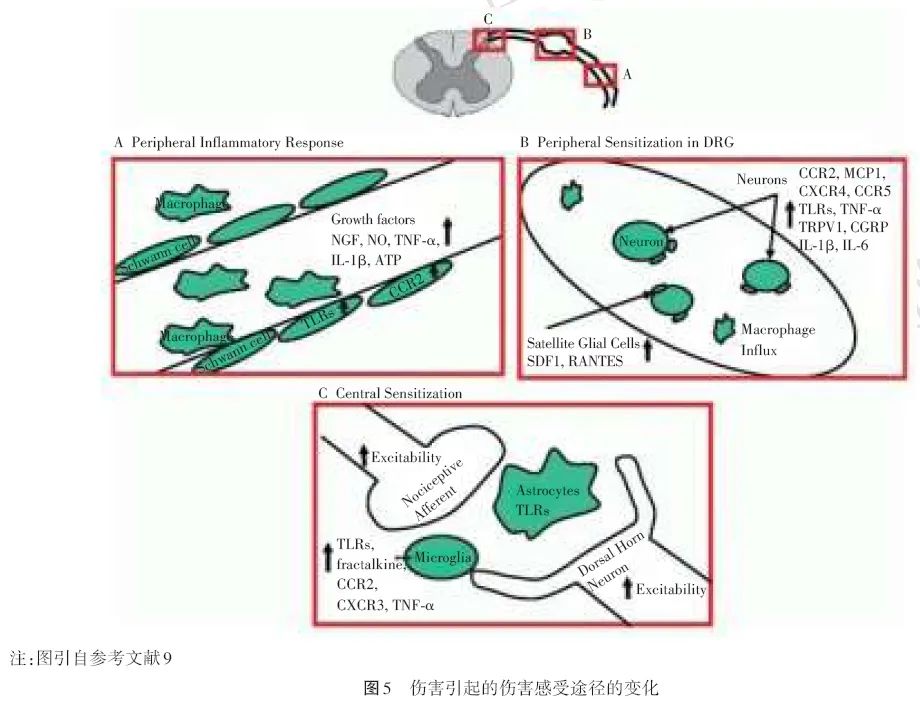
从上述差异蛋白中筛选出可能参加芬太尼蛛网膜下腔镇痛的分子作为进一步研究的目的蛋白,通过KEGG通路功能分析发现,多数蛋白通路参与生物功能调节。通过查阅文献,从差异蛋白通路中选取了CGRP进行文献学习(图5),结果发现,许多镇痛药物可通过抑制DRG中CGRP的合成而发挥镇痛作用。
3 讨论
本研究通过高通量测序法检测芬太尼蛛网膜下腔麻醉组大鼠DRG中miRNA表达谱,发现差异显著。通过DRG转录测序发现,芬太尼蛛网膜下腔麻醉后大鼠DRG中显著上调基因58种,显著下调基因54种。
本研究发现,芬太尼蛛网膜下腔麻醉miRNA靶基因的KEGG主要通路涉及囊泡运输中的SNARE(与CGRP分泌相关)相互作用,而CGRP广泛分布于中枢和外周神经系统,主要由感觉神经元,特别是无髓鞘的C纤维和薄髓鞘的Aδ纤维(两种纤维统称为CGRP能神经纤维)释放。
本研究发现,芬太尼蛛网膜下腔麻醉差异表达的miRNA与离子跨膜转运的调节有关。在DRG神经元胞体和纤维上存在多种离子通道和递质通道,包括电压门控钠通道、瞬时受体电位通道、P2X受体通道等,参与急性和慢性疼痛的传导,发挥DRG介导的镇痛作用。此外,本研究还发现,芬太尼蛛网膜下腔麻醉差异表达的miRNA与钙释放通道活性有关,而Ca2+的升高被认为与疼痛和痛觉过敏一致,钙紊乱与疼痛相关。
综上所述,本研究鉴定了芬太尼蛛网膜下腔麻醉后大鼠DRG中差异表达miRNA,并通过生物信息学分析对差异表达的miRNA及其靶基因的潜在功能进行预测分析。我们认为大鼠DRG中与离子跨膜转运的调节,钙释放通道活性以及囊泡运输中的SNARE(与CGRP分泌相关)相互作用等相关的miRNA可能参与了芬太尼蛛网膜下腔的麻醉过程,但差异表达miRNA在蛛网膜下腔麻醉作用的具体调控机制仍需进一步研究。
国际麻醉学与复苏杂志,2025,46(04):344-350 .
DOI:10.3760/cma.j.cn321761-20240615‑01239
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)