首页 > 医疗资讯/ 正文
摘要:目的分析脑梗死患者住院期间发生消化道出血的危险因素。方法回顾性连续纳入青岛西海岸新区人民医院神经内科2022年1月至2024年12月因脑梗死入院的患者。收集所有患者的基线资料及治疗情况,基线资料包括年龄、性别、入院时收缩压、入院时舒张压、入院时美国国立卫生研究院卒中量表(NIHSS)评分、既往史[高血压病、糖尿病、冠心病、心房颤动、脑梗死病史、血脂异常、消化道疾病(胃炎、胃溃疡)]、脑梗死部位(前循环、后循环、多发性)、急性卒中Org10172治疗试验(TOAST)分型、入院时实验室检查指标(血红蛋白、血小板计数、凝血酶原时间、活化部分凝血活酶时间),治疗情况包括抗血小板聚集治疗、抗凝治疗、静脉溶栓治疗、降脂治疗、预防性质子泵抑制剂使用。根据住院期间是否发生消化道出血,将患者分为出血组和非出血组,消化道出血的诊断依据《急性上消化道出血急诊诊治流程专家共识(2020版)》中的诊断标准。比较两组患者的住院时间及住院期间全因死亡患者比例。将单因素分析中差异有统计学意义的变量纳入多因素Logistic回归分析,评估脑梗死患者住院期间发生消化道出血的影响因素。结果共纳入344例脑梗死患者,男201例,女143例,年龄32~91岁,平均(68±12)岁,其中22例(6.4%)发生消化道出血,322例(93.6%)未发生消化道出血。(1)出血组患者年龄[(74±12)岁比(67±12)岁]、入院时NIHSS评分[8(4,20)分比2(2,4)分]、入院时凝血酶原时间[(13.1±1.5)s比(12.4±1.1)s]及冠心病[50.0%(11/22)比20.8%(67/322)]、心房颤动[50.0%(11/22)比15.5%(50/322)]、消化道疾病[27.3%(6/22)比14.3%(46/322)]、静脉溶栓治疗[22.7%(5/22)比2.2%(7/322)]患者比例均高于非出血组,入院时血红蛋白水平[(118±21)g/L比(135±16)g/L]、抗血小板聚集治疗患者比例[59.1%(13/22)比79.5%(256/322)]均低于非出血组,住院期间全因死亡患者比例[40.9%(9/22)比1.6%(5/322)]、住院时间[(11.24±2.90)d比(6.96±1.42)d]均高于非出血组,差异均有统计学意义(均P<0.05)。两组患者脑梗死部位分布、TOAST分型分布差异均有统计学意义(均P<0.01)。余单因素分析结果差异均无统计学意义(均P>0.05)。(2)多因素Logistic回归分析结果显示,高入院时NIHSS评分(OR=1.183,95%CI:1.112 ~ 1.259,P<0.01)、心源性栓塞型(OR= 2.858,95%CI:1.302~7.917, P=0.043)、抗血小板聚集治疗(OR= 2.142,95%CI:1.238~3.705, P=0.006)和静脉溶栓治疗(OR= 7.242,95%CI:1.802~29.110,P=0.005)是脑梗死患者住院期间发生消化道出血的危险因素。结论高入院时NIHSS评分、心源性栓塞型、抗血小板聚集治疗和静脉溶栓治疗是脑梗死患者住院期间发生消化道出血的危险因素。
脑梗死是我国成人致死、致残的首要病因,其治疗与并发症管理一直备受关注。消化道出血在脑梗死并发症中尤为突出,其止血与抗凝治疗之间的矛盾不仅增加了原发病的治疗难度,延长了住院时间,还增加了患者的死亡风险。消化道出血的病因复杂,涉及多种因素,包括胃肠道黏膜屏障功能障碍、应激反应引发的胃溃疡以及抗血小板聚集或抗凝治疗导致的药物相关性出血等。既往研究表明,急性脑梗死后消化道出血的发生率为1.24%~8.60%,对于高龄或存在多种慢性疾病的患者,其消化道出血的发生率高达19%(40/216)。因此,明确脑梗死患者发生消化道出血的危险因素,结合临床实际情况制定有效的干预措施,是改善脑梗死患者预后、降低并发症发生率的关键。本研究旨在探讨脑梗死患者住院期间发生消化道出血的相关危险因素,为早期干预和个体化治疗提供依据。
1 对象与方法
1.1 对象
回顾性连续纳入青岛西海岸新区人民医院神经内科2022年1月至2024年12月收治的344例因脑梗死入院的患者,所有患者在入院后均接受了详细的临床评估与治疗。纳入标准:(1)年龄≥18岁;(2)脑梗死诊断符合《中国急性缺血性脑卒中诊治指南2018》中的诊断标准,经头部CT或MRI检查确诊;(3)病历资料完整。研究方案经青岛西海岸新区人民医院医学伦理委员会审核批准(伦理号:LL-LW-2025001)。患者或其家属签署了诊疗知情同意书。
1.2 资料收集
收集患者的基线资料,包括年龄、性别、入院时收缩压、入院时舒张压、入院时美国国立卫生研究院卒中量表(NIHSS)评分、既往史[高血压病、糖尿病、冠心病、心房颤动、脑梗死病史、血脂异常、消化道疾病(胃炎、胃溃疡)]、脑梗死部位(前循环、后循环、多发性)、急性卒中Org10172治疗试验(trial of Org 10172 in acute stroke treatment,TOAST)分型、入院时实验室检查指标(血红蛋白、血小板计数、凝血酶原时间、活化部分凝血活酶时间)。高血压病依据《中国高血压防治指南(2018年修订版)》中高血压病的诊断标准,包括非同日3次测量收缩压≥140mmHg和(或)舒张压≥90mmHg,或既往明确诊断并接受治疗者。糖尿病符合《中国2型糖尿病防治指南(2020年版)》中的诊断标准,需满足典型症状(多尿、多饮、多食、体质量下降)+空腹血糖≥7.0mmol/L、口服葡萄糖耐量试验2h血糖水平≥11.1mmol/L或糖化血红蛋白≥6.5%。冠心病依据《稳定性冠心病基层诊疗指南(2020年)》诊断标准,需具备典型心绞痛症状、心电图ST-T改变,或冠状动脉造影显示狭窄率≥50%。心房颤动遵循《心房颤动:目前的认识和治疗建议(2021)》诊断标准,符合单导联心电图(≥30s)或十二导联心电图(≥10s)显示P波消失,代之以大小、形态及时限均不规则的颤动波(f波)、RR间期绝对不规则即可诊断为心房颤动。脑梗死诊断符合《中国急性缺血性脑卒中诊治指南2018》中的诊断标准,包括急性神经功能缺损持续≥24h、CT或MRI证实为缺血性卒中,并按照TOAST分型(大动脉粥样硬化型、小动脉闭塞型、心源性栓塞型等)分类。血脂异常依据《血脂异常基层诊疗指南(2019年)》中的标准,其中总胆固醇水平≥6.2mmol/L或低密度脂蛋白胆固醇(LDL-C)水平≥4.1mmol/L即符合诊断。消化道疾病(胃炎、胃溃疡)的诊断标准参照《2020年中国胃食管反流病专家共识》、《消化性溃疡诊断与治疗规范(2016年,西安)》,其中胃炎需经胃镜检查证实胃黏膜炎症或萎缩,胃溃疡则表现为胃镜下局限性溃疡,直径>5mm,边界清晰。
收集患者治疗情况,包括抗血小板聚集治疗(阿司匹林、氯吡格雷或阿司匹林联合氯吡格雷)、抗凝治疗(低分子肝素或华法林)、静脉溶栓治疗(阿替普酶或尿激酶)、降脂治疗(阿托伐他汀或瑞舒伐他汀)、预防性质子泵抑制剂(proton pump inhibitor,PPI)使用(奥美拉唑或泮托拉唑)。
1.3 分组
根据住院期间是否发生消化道出血,将344例脑梗死患者分为出血组和非出血组。消化道出血的诊断依据《急性上消化道出血急诊诊治流程专家共识(2020版)》,需满足以下几项中的至少一项:(1)临床症状,包括呕血、黑便或血便;(2)实验室检测,连续2次便潜血试验阳性(≥++);(3)胃镜或肠镜检查明确出血病灶。
1.4 临床路径管理
依据《中国急性缺血性脑卒中诊治指南2018》及《急性上消化道出血急诊诊治流程专家共识(2020版)》,制定并实施标准化临床管理路径,旨在规范脑梗死患者入院后的全程管理,降低并发症发生风险并改善预后,具体路径包括以下关键环节:
急性期管理(入院0~72h):对于发病4.5h内且符合静脉溶栓适应证的患者,优先启动静脉溶栓治疗,使用阿替普酶(0.9mg/kg),并严格监测出血风险。溶栓治疗后,持续动态评估患者NIHSS评分、凝血功能及便潜血,确保及时发现和处理出血倾向。在血压管理方面,静脉溶栓患者维持收缩压<180mmHg、舒张压<105mmHg,避免血压过高引发出血并发症;非静脉溶栓患者则根据基线血压进行分层管理,目标收缩压为140~160mmHg,以确保足够的灌注压力,同时避免血压过低导致的灌注不足。在抗栓治疗方面,静脉溶栓患者在溶栓24h后复查头部CT,如无出血则启动抗血小板聚集或抗凝治疗。非心源性卒中患者在发病24h内应启动抗血小板聚集治疗(单抗或双抗),而心源性栓塞患者则在排除出血风险后开始抗凝治疗。在胃黏膜保护方面,针对高危患者(如NIHSS评分≥8分、年龄≥75岁、接受静脉溶栓或双抗治疗者),需预防性使用质子泵抑制剂(如奥美拉唑或泮托拉唑)。
并发症监测与干预(入院72h至7d):对于接受静脉溶栓或抗栓治疗的高危患者,应每日进行便潜血检测,并在便潜血阳性结果出现48h内进行胃镜检查。如确诊为消化道出血,立即暂停抗栓药物,并启动标准止血方案,包括使用PPI、生长抑素及内镜下治疗。在感染防控方面,对于吞咽筛查异常的患者,尽早采取鼻饲措施,以防止误吸性肺炎的发生;留置导尿管患者严格遵循无菌操作,防止泌尿系感染。对于卧床患者,使用间歇充气加压装置,出血风险较低的患者可联合使用低分子肝素皮下注射(4000IU/d),预防深静脉血栓形成。
康复与二级预防(入院7d至出院):在患者NIHSS评分稳定后48h内启动个体化康复计划,结合物理治疗和言语训练,每周定期评估患者神经功能恢复情况。对于脑梗死的危险因素控制,首先进行血脂管理,将LDL-C控制在<1.8mmol/L,采用高强度他汀联合依折麦布治疗;血糖控制方面,目标为空腹血糖4.4~7.8mmol/L,随机血糖7.8~10.0mmol/L,采用干预生活方式联合口服降糖药物治疗(如二甲双胍、吡格列酮、阿卡波糖、达格列净、沙格列汀等),当血糖>11.1mmol/L时,给予胰岛素治疗;同时,进行戒烟干预,联合药物(如伐尼克兰)与行为疗法协助患者戒烟。出院前,评估患者的改良Rankin量表(mRS)评分,若mRS评分≤2分,可制定家庭康复计划;对于高风险出血患者(如心源性栓塞型),延长PPI的使用时间至4周,以降低并发症的发生风险。
多学科协作与质量控制:由神经内科、急诊科、心血管科、消化科、康复科医护人员共同参与患者的诊疗过程,从急性期的溶栓治疗至康复期的个体化管理与护理。
1.5 消化道出血监测及干预
根据《急性上消化道出血急诊诊治流程专家共识(2020版)》,对所有脑梗死患者进行消化道出血动态监测,包括常规监测、症状触发监测和干预措施。(1)常规监测:对于无症状患者,入院后每日行便潜血检测(免疫化学法),连续3d,若结果为阴性且入院时NIHSS评分<5分,则改为隔日检测;对于出血高危(入院时NIHSS评分≥5分、接受静脉溶栓或抗凝治疗、既往有消化道疾病史)患者,每日行便潜血检测直至出院。(2)症状触发监测:出现呕血、黑便、血便或血红蛋白水平下降≥20g/L时,立即行胃肠镜检查、便常规检测以明确出血部位及程度。(3)干预措施:便潜血阳性(≥++)或胃肠镜检查证实出血者,启动标准化止血方案,包括PPI静脉滴注(用法及剂量:0.9%氯化钠注射液+奥美拉唑40mg静脉滴注,1次/12h,或0.9%氯化钠注射液+泮托拉唑40mg,静脉滴注,1次/12h)、输血支持治疗、内镜下止血或介入栓塞治疗。对比两组患者住院时间、住院期间全因死亡患者比例。
1.6 统计学分析
采用SPSS26.0软件对数据进行统计学分析。采用Shapiro-Wilk检验评估计量资料是否符合正态分布,符合正态分布的计量资料以x-±s表示,组间比较采用两独立样本t检验;不符合正态分布的计量资料以中位数和四分位数[M(P25,P75)]表示,组间比较采用Mann-Whitney U检验。计数资料以例(%)表示,组间比较采用χ2检验。缺失值采用多重插补法处理。将单因素分析中P<0.05的变量纳入多因素Logistic回归模型,探索脑梗死患者住院期间发生消化道出血的影响因素。本研究统计学检验采用双尾检验,以P<0.05为差异有统计学意义。
2 结果
共纳入344例脑梗死患者,其中男201例,女143例,年龄32~91岁,平均(68±12)岁,其中22例(6.4%)发生消化道出血,322例(93.6%)未发生消化道出血。
2.1 单因素分析结果
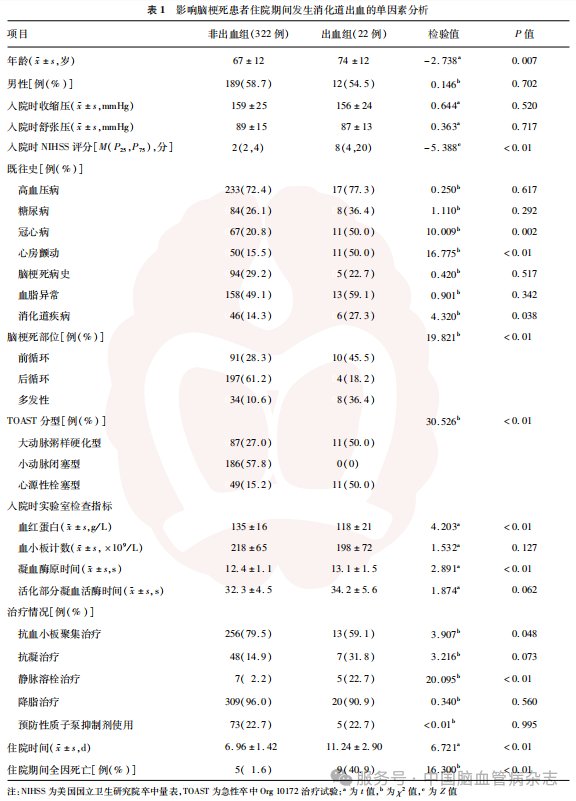
出血组患者年龄、入院时NIHSS评分、入院时凝血酶原时间及冠心病、心房颤动、消化道疾病、静脉溶栓治疗患者比例均高于非出血组,入院时血红蛋白水平、抗血小板聚集治疗患者比例均低于非出血组,差异均有统计学意义(均P<0.05)。两组患者脑梗死部位分布、TOAST分型分布差异均有统计学意义(均P<0.01)。余单因素分析结果差异均无统计学意义(均P>0.05)。见表1。
2.2 多因素Logistic回归分析结果
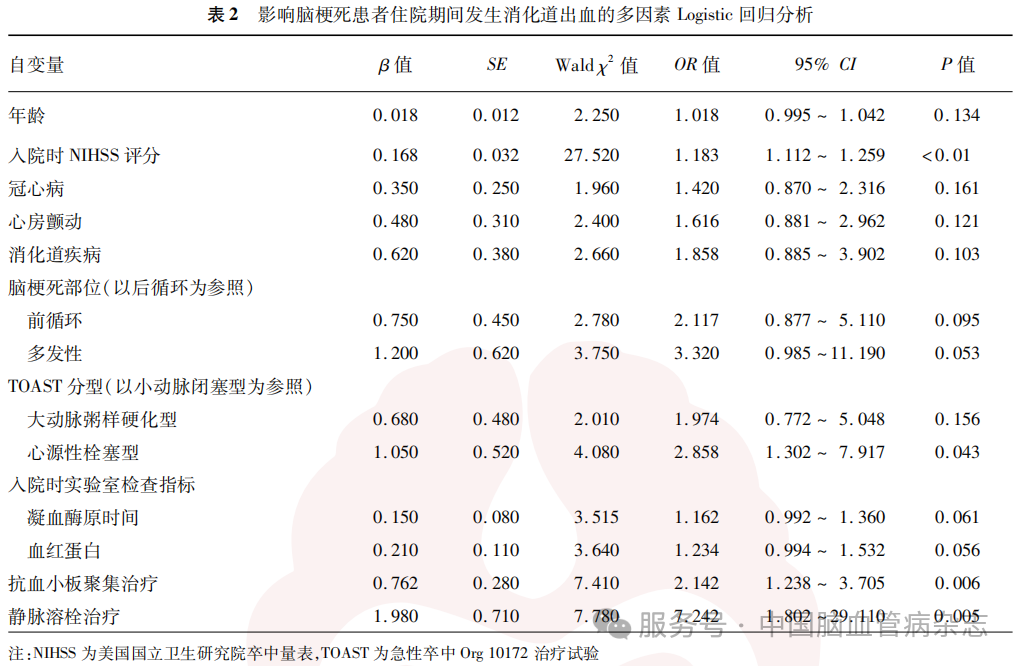
多因素Logistic回归分析结果显示,高入院时NIHSS评分(OR=1.183, 95%CI:1.112~1.259,P<0.01)、心源性栓塞型(OR=2.858,95% CI:1.302~7.917, P=0.043)、抗血小板聚集治疗(OR= 2.142,95% CI:1.238~3.705,P=0.006)和静脉溶栓治疗(OR=7.242,95% CI:1.802~29.110,P=0.005)是脑梗死患者住院期间发生消化道出血的危险因素。见表2。
2.3 两组患者的临床结局比较
出血组住院时间[(11.24±2.90)d比(6.96±1.42)d]、住院期间全因死亡患者比例[40.9%(9/22)比1.6%(5/322)]均高于非出血组,差异均有统计学意义(均P<0.05)。14例死亡患者中9例合并肾功能不全、心力衰竭或呼吸衰竭。
3 讨论
3.1 脑梗死患者消化道出血的发生率及其临床管理的重要性
既往研究显示,脑梗死后消化道出血的发生率为1.24%~8.60%,本研究结果显示,脑梗死后消化道出血的发生率为6.4%(22/344),与既往研究结果一致。脑梗死患者常由于丘脑、脑干或边缘系统受累,产生严重的应激反应及自主神经功能紊乱,进而导致应激性溃疡、上消化道出血等并发症。脑梗死治疗过程中抗血小板聚集和抗凝治疗药物的应用,使患者发生消化道出血的风险进一步增加。消化道出血不仅会加重脑梗死患者原有病情,还可能导致不可逆的多器官功能衰竭,其发生提示患者的全身状况进一步恶化。因此,临床医师应重点关注这一并发症,特别是对于高龄和神经功能损伤严重的脑梗死患者,明确消化道出血的危险因素对于制定个体化治疗方案、提高患者生存率至关重要。
3.2 入院时NIHSS评分是脑梗死患者发生消化道出血的独立危险因素
本研究显示,脑梗死后发生消化道出血患者的入院时NIHSS评分中位数为8(4,20)分,提示该类患者多存在中度至重度神经功能损伤(NIHSS评分≥5分)。多因素Logistic回归分析结果显示,入院时NIHSS评分是脑梗死患者住院期间发生消化道出血的独立危险因素(OR= 1.183,95% CI:1.112~1.259,P<0.01),提示入院时NIHSS评分越高,患者的神经功能受损越严重,可能与脑梗死发生后,自主神经系统功能调节能力变差,导致胃肠道的血供减少或功能紊乱,进而增加应激性溃疡和消化道出血的风险。此外,神经功能严重受损的患者通常需要抗血小板聚集或抗凝治疗,可能进一步增加消化道出血的发生风险。本研究结果提示,入院时NIHSS评分除可用于评估脑梗死患者神经功能损伤程度外,其作为消化道出血的风险预测指标同样具有重要临床意义。
3.3 TOAST分型与消化道出血:从病因预测脑梗死后消化道出血的风险
TOAST分型侧重于从病因学对脑梗死进行研究,可以为脑梗死的预后预测提供依据,其包括大动脉粥样硬化型、心源性栓塞型、小动脉闭塞型、其他病因型和不明原因型。本研究结果显示,TOAST分型为心源性栓塞型是脑梗死患者住院期间发生消化道出血的危险因素(OR= 2.858,95% CI:1.302~7.917,P=0.043),可能与其应用抗凝药物时间更长有关,增加了消化道出血的发生风险。因此,对于TOAST分型是心源性栓塞型的脑梗死患者,需要特别关注其抗凝药物使用情况,包括药物类型及剂量,并及时检测是否存在胃肠道出血。
3.4 抗血小板聚集治疗与消化道出血:获益与风险评估
抗血小板聚集治疗是脑梗死患者常用的标准治疗方法,对于预防复发性卒中具有重要作用。本研究显示,抗血小板聚集治疗是脑梗死患者住院期间发生消化道出血的独立危险因素(OR=2.142,95% CI:1.238~3.705,P=0.006)。这可能与抗血小板药物对胃肠黏膜的直接损伤作用有关。抗血小板聚集药物可以抑制血小板的聚集功能,从而增加胃肠道的微小出血风险,尤其是对于存在潜在胃溃疡或糜烂的患者。Malloy等的一项Meta分析(共纳入88675例患者)表明,在脑梗死二级预防中,与单一氯吡格雷相比,阿司匹林与氯吡格雷联合应用与更高的胃肠道出血率相关(RR=2.81,95% CI:1.96~4.10)。对于常规服用抗血小板聚集药物的患者,尤其是服用双联抗血小板聚集药物时,应提前评估患者胃肠道出血风险,必要时加用PPI来降低消化道出血发生的风险。临床医师应根据患者的个体化危险因素,动态调整抗血小板聚集治疗方案,从而在有效预防血栓的同时最大限度地降低消化道出血的发生率。
3.5 静脉溶栓治疗与消化道出血:风险与获益的平衡
本研究结果显示,静脉溶栓治疗是脑梗死患者住院期间发生消化道出血的独立危险因素(OR=7.242,95%CI:1.802 ~ 29.110, P=0.005),提示静脉溶栓治疗作为急性脑梗死的重要治疗手段,其潜在的消化道出血风险需引起高度警惕。但其95%CI较宽提示可能受样本异质性或静脉溶栓药物剂量差异的影响。在病理生理机制方面,静脉溶栓治疗可通过激活纤溶系统降解纤维蛋白原,削弱凝血功能,增加黏膜微血管渗血风险;同时,急性脑损伤引发的交感神经过度激活可导致胃黏膜血管痉挛及缺血-再灌注损伤,进一步诱发应激性溃疡。尽管静脉溶栓增加了脑梗死患者消化道出血风险,但其降低致残率的临床获益仍不可替代,临床决策需个体化平衡血管再通获益与消化道出血风险。对于入院时NIHSS评分≥4分、发病时间在4.5h以内且无静脉溶栓禁忌证的脑梗死患者,静脉溶栓治疗仍是首选治疗方式,但需严格筛查消化道出血高危因素(如高龄、既往消化道出血史和凝血功能异常),并在静脉溶栓后24h内加强生命体征与便潜血监测。未来研究可探索新型靶向静脉溶栓药物或联合神经保护剂的应用,以优化治疗时间窗内的风险获益比。
本研究中出血组与非出血组预防性使用PPI的患者比例差异无统计学意义,但《应激性溃疡防治专家建议(2018版)》推荐对于应激性溃疡危重症患者,存在脑血管意外一项高危因素即可预防性使用PPI。Conrad等的一项前瞻性双盲研究对重症监护病房应激性溃疡危重患者(包括至少一个上消化道出血危险因素),随机接受奥美拉唑混悬液或西咪替丁注射液预防上消化道出血,共治疗14d,结果显示,奥美拉唑组出血率低于西咪替丁组[4.5%(7/157)比6.8%(10/146),P< 0.05],提示预防性应用奥美拉唑可以更有效地预防应激性溃疡危重症患者上消化道出血。PPI在代谢过程中对细胞色素P4502C19有亲和作用,可削弱氯吡格雷的抗血小板聚集作用,尤其是奥美拉唑,泮托拉唑影响相对较小。随着双联抗血小板聚集药物的广泛应用,需要更多更全面的临床研究评估抗血小板聚集药物与PPI联合应用治疗脑梗死患者的安全性及协同作用。
3.6 消化道出血患者的预后:住院时间延长与住院期间全因死亡患者比例增加
本研究结果显示,出血组患者的住院时间延长[(11.24±2.90)d比(6.96±1.42)d, P<0.05],住院期间全因死亡患者比例升高[40.9%(9/22)比1.6%(5/322),P< 0.05]。住院时间延长的原因可能包括:(1)消化道出血后需暂停抗栓治疗,增加了脑梗死复发风险,延长了神经功能康复周期;(2)出血相关干预措施(如内镜止血、输血支持)及并发症管理(如感染控制)增加了住院时间;(3)出血导致的贫血、低蛋白血症等全身代谢紊乱延缓了患者整体恢复进程。全因死亡患者比例的升高则与多器官功能衰竭密切相关,本研究14例死亡患者中9例合并肾功能不全、心力衰竭或呼吸衰竭,提示消化道出血可能通过全身炎症反应及血流动力学紊乱加剧多系统损伤[36]。尽管本研究观察到两组全因死亡患者比例存在差异,但受限于回顾性设计及较少样本量,未能进一步区分直接死亡原因(如脑疝、感染性休克等),且未完全控制潜在混杂因素(如患者基线脏器功能状态)。未来需通过前瞻性研究结合尸检或详细死亡原因分类,明确消化道出血对死亡风险的独立贡献。
本研究的局限性:本研究为单中心、回顾性设计,样本的代表性不足;纳入变量不全面,病历中既往数据记录不完整,导致研究结果可能存在偏倚,今后有待收集更多的变量并开展多中心和前瞻性研究加以验证和优化。
综上所述,本研究系统分析了脑梗死患者住院期间发生消化道出血的危险因素,结果表明,高入院时NIHSS评分、心源性栓塞型、抗血小板聚集治疗和静脉溶栓治疗是消化道出血的独立危险因素。随着神经功能损伤的加重,脑梗死患者发生消化道出血的风险增加,TOAST分型为心源性栓塞型也提示脑梗死患者消化道出血风险增加,抗血小板聚集和静脉溶栓治疗作为急性脑梗死有效的治疗手段,但其潜在的消化道出血风险不容忽视。本研究分析了脑梗死后神经功能损伤对胃肠道功能调节方面的影响,提示临床医师不仅要关注脑梗死患者的神经功能恢复,还应积极干预消化道出血等并发症,特别是应在权衡利弊后在消化道出血高风险人群中预防性使用胃黏膜保护药物。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)