首页 > 医疗资讯/ 正文
卵巢肿瘤细胞在腹水中的锚定非依赖性存活是腹膜转移的初始和关键步骤。卵巢肿瘤细胞如何实现锚定独立性仍不清楚。
2025年4月3日,中山大学潘超云、李洁及刘军秀共同通讯在Nature Communications 上在线发表题为“A noncanonical role of SAT1 enables anchorage independence and peritoneal metastasis in ovarian cancer”的研究论文。研究表明亚精胺/精胺N1-乙酰转移酶1(SAT1)的非经典作用决定了不依赖锚定的细胞存活并增强卵巢癌中的转移播散。
SAT1高癌细胞在腹水中普遍存在,原发性肿瘤中SAT1的高表达与卵巢癌患者腹膜转移率增加有关。从机制上讲,SAT1对多个有丝分裂调节基因的H3K27结构域进行非标准乙酰化,从而提高其转录水平,并保护播散细胞免受异常有丝分裂和有丝分裂细胞死亡的影响。值得注意的是,SAT1对H3K27的乙酰化依赖于谷氨酰胺的还原羧化来供应细胞核中的乙酰辅酶a。在小鼠模型中,使用小分子抑制剂银杏内酯B抑制SAT1可减轻转移性肿瘤负荷。研究得出结论,SAT1抑制是转移性卵巢癌有前景的治疗策。

卵巢癌是女性第八大常见癌症,近年来全球每年有超过20万人死于卵巢癌。上皮性卵巢癌(EOC)是最常见的卵巢癌类型,通常扩散到腹膜,在诊断时导致广泛的腹膜沉积和恶性腹水。目前EOC的标准疗法是减瘤手术联合铂类辅助化疗。一部分同源重组缺陷症(HRD)患者或对一线铂类化疗有反应的患者可能受益于聚(ADP\核糖)聚合酶(PARP)抑制剂的维持治疗。然而,化疗耐药和对PARP抑制剂的耐药性常见于EOC。EOC患者的有效疗法代表了紧迫的未满足的临床需求,需要深入了解发病机制以确定潜在的治疗机会。
恶性腹水伴肿瘤细胞播散通常与卵巢癌的转移和复发有关。当被剥夺与细胞外基质(ECM)的附着时,细胞通常会经历一种称为失巢凋亡的程序性细胞死亡。然而,腹水中的卵巢癌细胞在ECM脱离后存活下来,并在腹膜腔中广泛播散,与锚定无关。不依赖锚定的细胞存活对于腹膜转移可能特别重要。先前的研究表明,细胞存活的锚定独立性与代谢重编程有关。值得注意的是,癌细胞在增殖与播散方面的代谢支持可能截然不同。然而,实现锚定独立性和腹膜转移的代谢重编程的上游信号和下游靶标在很大程度上是未知的。
在这项工作中,鉴于上述发现,研究最初试图研究代谢重编程的作用,这在卵巢癌的锚定非依赖性细胞存活和腹膜转移中起关键作用。值得注意的是,我们发现了SAT1(多胺分解代谢中的限速酶)在调节对有丝分裂控制和染色体分离至关重要的基因中的H3K27ac表观遗传标记方面的非经典作用。这一机制促进了非锚着依赖性生存,并驱动卵巢癌细胞的腹膜播。
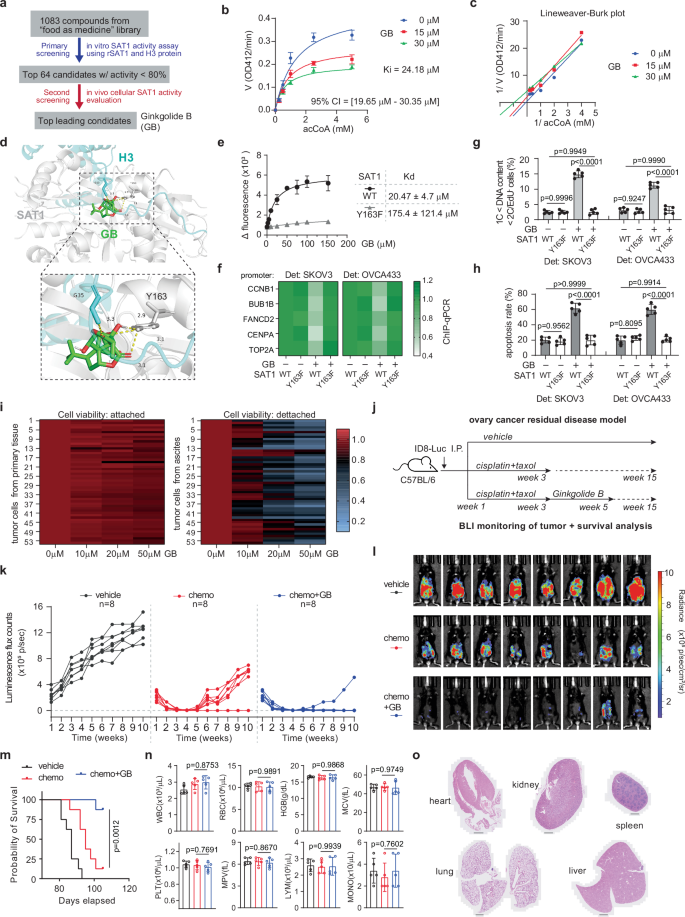
图1 银杏内酯B被鉴定为SAT1抑制剂,减少腹膜转移作为维持治疗(摘自Nature Communications)
参考消息:
https://doi.org/10.1038/s41467-025-58525-8
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)