首页 > 医疗资讯/ 正文
儿童癌症是儿童1-14岁年龄段第二大死因,15-19岁年龄段的第四大死因。尽管过去40年来生存率有显著提高,但复发和晚期肿瘤患者的预后仍然很差,总体生存率低于20%。这其中,复发性中枢神经系统肿瘤、神经母细胞瘤、肉瘤和其他罕见实体瘤面临最大的治疗挑战。从分子角度,肿瘤发展中涉及的分子网络变化非常复杂,这种复杂性会加剧癌细胞基因组的不稳定性,进而导致更多亚克隆和异质性。肿瘤在进展中的高变异性以及许多分子通路的可塑性,也正是药物治疗出现耐药的基础。因此,如果通过基因组测序可以识别基因组改变,并与针对特定通路的抑制药物相匹配,便可实现有效的靶向治疗并减少药物毒性,为进一步个体化精准医疗建立基础。
近日,美国“战胜儿童癌症研究联盟”(Beat Childhood Cancer Research Consortium)的19所医院和科研中心团队,在 Genome Medicine 发表题为 Molecular-guided therapy for the treatment of patients with relapsed and refractory childhood cancers: a Beat Childhood Cancer Research Consortium trial 的文章。通过一项前瞻性、多中心临床试验,评估将肿瘤基因组和转录组分析与分子肿瘤委员会(MTB)相结合的个体化疗法,即分子导向治疗(Molecular-guided Therapy,MGT),证明了该疗法在为复发/难治性实体瘤儿童做出实时治疗决策时的可行性、安全性和疗效。

本研究于2014年7月至2018年6月共纳入186名受试者,144名接受了分子导向治疗(MGT)。接受MGT的受试者平均年龄11.04岁,其中69.44%至少接受过一种复发治疗。受试者被分为3组:复发/难治性神经母细胞瘤(31例,21.53%)、复发/难治性中枢神经系统肿瘤(41例,28.47%)和复发/罕见实体瘤(72例,50%)。
分子导向疗法(MGT)的主要流程为:
(1)样本收集:收集受试者接受手术切除或活检获得的新鲜肿瘤样本,并采集外周血样本;
(2)分子分析:将肿瘤样本和外周血样本送至CLIA(美国“临床检验改进修正计划”)认证的实验室,进行肿瘤-正常全外显子组测序、肿瘤全转录组测序;
(3)数据分析:利用生物信息学分析方法,对测序数据进行变异检测、拷贝数变异分析、表达谱分析等;
(4)分子肿瘤委员会(MTB):由多学科专家组成的委员会根据患者的分子特征和文献证据,制定个体化的多药联合治疗方案(可推荐最多4种药物的组合);
(5)治疗和随访:患者启动分子引导治疗后,每2个疗程进行一次疗效评估(通过RECIST标准),并记录不良事件发生情况;
(6)细胞株和PDX(患者源移植瘤)模型建立:部分肿瘤样本将用于进一步研究;
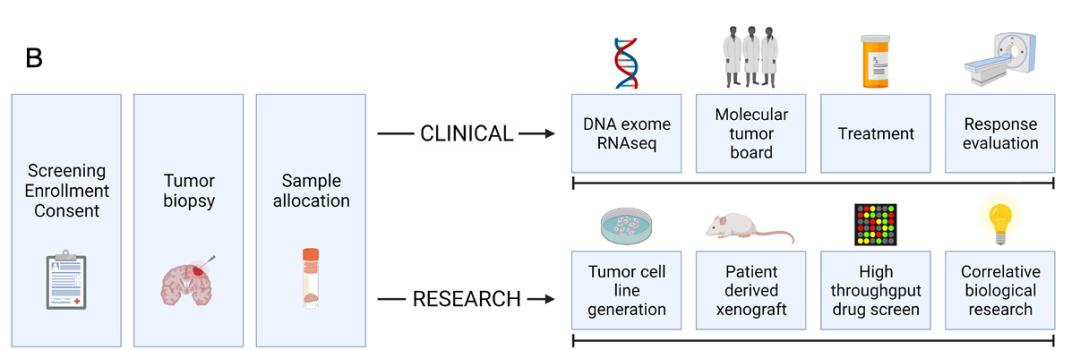
含数据流与样本流的研究流程图
在同意并参与研究后,受试者接受活组织检查,以非显著方式获取肿瘤样本。然后将肿瘤样本分为临床组和研究组,并送往Ashion(CLIA)和POTRL(非CLIA)进一步评估。Ashion进行了肿瘤正常全外显子组测序(WES)和肿瘤RNA测序。然后对数据进行分析,结果提供分子肿瘤委员会用于指导治疗决策。受试者根据分子肿瘤委员会意见接受治疗,并按方案评估疗效。送往POTRL的肿瘤样本用于细胞系和PDX模型生成、高通量药物筛选以及进一步的生物学研究和分析。
本研究证明了MGT的可行性、安全性和有效性。
-
可行性:从活检到开始治疗的平均时间为38天,84%的受试者在第1个疗程内启动全部推荐的治疗,95%的患者最终启动了推荐的全部治疗;
-
安全性:使用MGT药物的相关毒性很低,仅有少数3-4级不良事件发生,未见明显意外毒性;
-
疗效:整体上65%的受试者获得了临床获益。神经母细胞瘤组为67%,中枢神经系统肿瘤组为73%,罕见实体瘤组为60%。表明该个体化治疗方法具有较好的疗效;
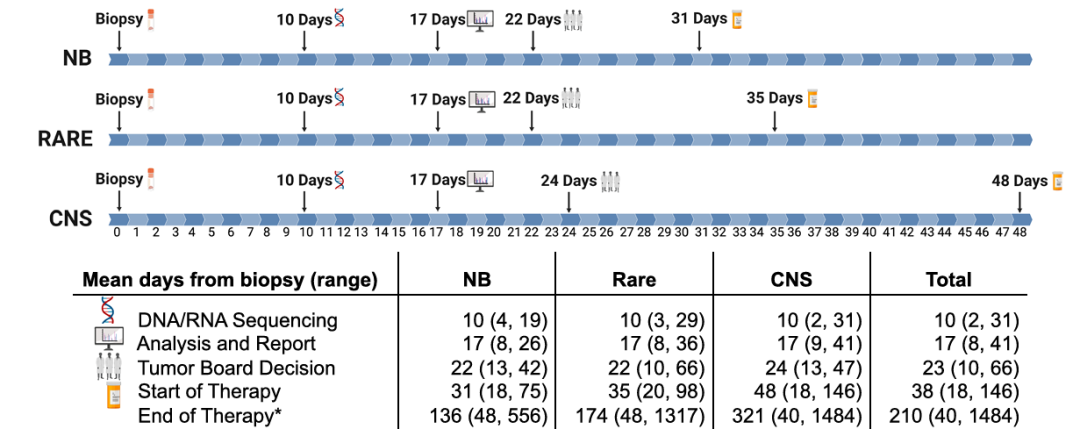
通过从活检到DNA/RNA测序、分析报告、肿瘤委员会决定和MGT启动的时间来评估可行性
时间线中记录了三种肿瘤类型(NB-神经母细胞瘤,Rare-罕见实体瘤,CNS-中枢神经系统肿瘤)从活检到系列时间点的平均天数。平均值的范围在相应的表格中注明。计算所有符合安全标准的受试者的值(n=144)。对于提交时仍在接受治疗的受试者,将2019年11月1日作为治疗结束日期,以免将这些受试者排除在评估之外。 *治疗结束是指从活检到最后一剂研究药物给药的天数。
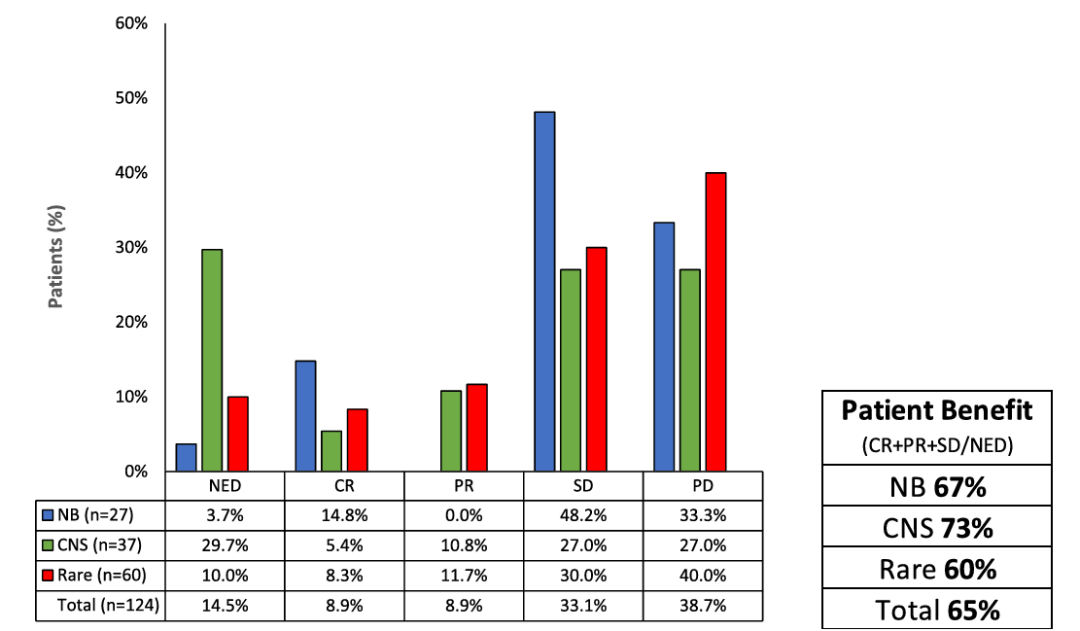
对所有符合疗效标准受试者(n=124),使用其最佳扫描结果计算的最佳治疗应答率。
总体上,14.52%(18/124)的受试者在手术切除后仍处于无疾病迹象状态(NED),8.87%(11/124)达到完全缓解(CR),8.87%的受试者达到部分缓解(PR),33.06%(41/124)保持疾病稳定(SD),而39.71%(48/124)的受试者有进展性疾病(PD)。
本研究从分子层面进行探索,揭示了儿童癌症的复杂基因组学特征。
通过全外显子组和全转录组测序,对不同肿瘤类型的突变谱、拷贝数变异和基因表达特征进行了深入分析,发现儿童肿瘤具有独特的分子特征;通过肿瘤样本的异质性分析,对受试者的多次活检样本进行了纵向分析,发现肿瘤存在明显的基因组演化和异质性,这为进一步理解耐药机制提供了线索;成功建立了96株细胞株和47株PDX模型,为进一步深入研究提供了重要的工具。
总之,该研究证明了将综合测序(全外显子组测序和全转录组测序)与分子肿瘤委员会相结合的个体化治疗方法在复发/难治性儿童实体瘤患者治疗中的可行性、安全性和疗效。强调了在儿童癌症中,单纯依靠DNA测序的局限性。通过分子测序结果与多学科的MTB的综合建议相结合,做出实时的个体化治疗决策,这种"N of one"的研究设计不仅是创新性的,更克服了单一靶向药物治疗的局限性,采用多药联合治疗克服肿瘤的异质性和耐药性,提高了治疗效果。另一方面,该研究未对不同治疗决策方法(仅DNA、DNA+RNA、仅RNA)的疗效进行深入比较分析,未对受试者的生存结局进行评估,也未对治疗方案的成本-效果进行分析,仍需要进一步的大样本、长期随访、对照研究来验证其疗效和安全性。
猜你喜欢
- ATVB 解放军中部战区总医院向光大教授团队发现炎症细胞源性MYDGF抑制内皮细胞LDL穿胞及抗动脉粥样硬化
- 国家卫健委:11月4日新增新冠肺炎确诊病例78例本土病例68例
- 饮食减肥期间晚餐怎么吃才能瘦得快?
- 男子误喝假酒中毒 医生处方:喝60度真酒解毒
- 手术后多久拆线对身体最好
- 31省区市新增确诊14例 新冠病毒会根据鼻腔进到身体吗
- 用热毛巾搓这个部位竟能排毒
- 江苏省药品监督管理局关于发布实施第十批20个品种《江苏省中药...
- 弧心距(arc center distance):评估掌侧Barton骨折移位的影像参数
- JAMA Oncology:复旦大学蔡国响/上海交通大学王争发现ctDNA甲基化可用于临床监测结直肠癌复发,指导分级和治疗
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)