首页 > 医疗资讯/ 正文
随着近年来我国冠心病的发病率逐年上升,其已严重影响到健康中国策略的实施。急性心肌梗死(acute myocardial infarction, AMI)是冠心病的危急重症类型,其死亡率和致残率均较高,远期预后也较差。近年来,以胸痛中心及冠心病介入治疗为主的AMI治疗方式,起到了挽救患者的生命、改善患者远期预后作用,AMI患者死亡率已明显下降。随着AMI后心室重构机制、心功能不全研究的深入,近年来有诸多治疗心功能不全的新药问世。但上述手术和药物治疗手段并不能逆转或者完全阻断AMI后心肌细胞死亡、心室重构的发生发展,同时AMI发生后心肌损伤机制复杂,尚未完全明了。因此,如何进一步减少心肌细胞的死亡,保留更多有用的心肌细胞,是避免AMI继发心力衰竭的重要手段。
越来越多的研究证实,环境因素在疾病的进展中发挥重要作用。吸烟、饮酒、高脂饮食、高糖饮食等环境因素在不改变基因序列的情况下,调控一系列基因的表达,同时也参与了心血管疾病的发展,即所谓的表观遗传学。大量研究发现,通过调控表观遗传学修饰可以改善AMI的预后,并有望成为治疗AMI的新策略。因此,进一步深入阐述、明确AMI的心肌损伤、心室重构、心功能不全发展机制,探索特异性的保护手段,促进缺血缺氧条件下心肌细胞的存活、阻断心肌细胞死亡是AMI研究领域的主要方向之一。RNA结合蛋白(RBPs)在多种生物过程中发挥着多种功效。RBM15作为一种重要的RBP,近期研究证实其在mRNA的m6A修饰过程中发挥重要调节作用,但在MI中的调控功能仍不清楚。
2024年4月18日,复旦大学附属中山医院葛均波院士团队在JACC Basic to Translational Science上发表了题为“RBM15 protects from myocardial infarction by stabilizing NAE1”的研究论文,揭示了RBM15通过m6A修饰功能稳定其在细胞凋亡功能上的靶点NAE1从而发挥MI后心功能保护作用。

首先,研究者通过RNA甲基化测序(MeRIP-seq)发现心肌梗死样本中m6A水平升高,其在心梗组织和对照组织的转录本中皆高表达,心梗组织中更显著。通过筛选一系列RNA修饰蛋白,结果显示RBM15是心肌梗死后的重要调节因子。通过对比STEMI患者及对照组外周血中RBM15表达情况,证实其在STEMI患者外周血中显著高表达。

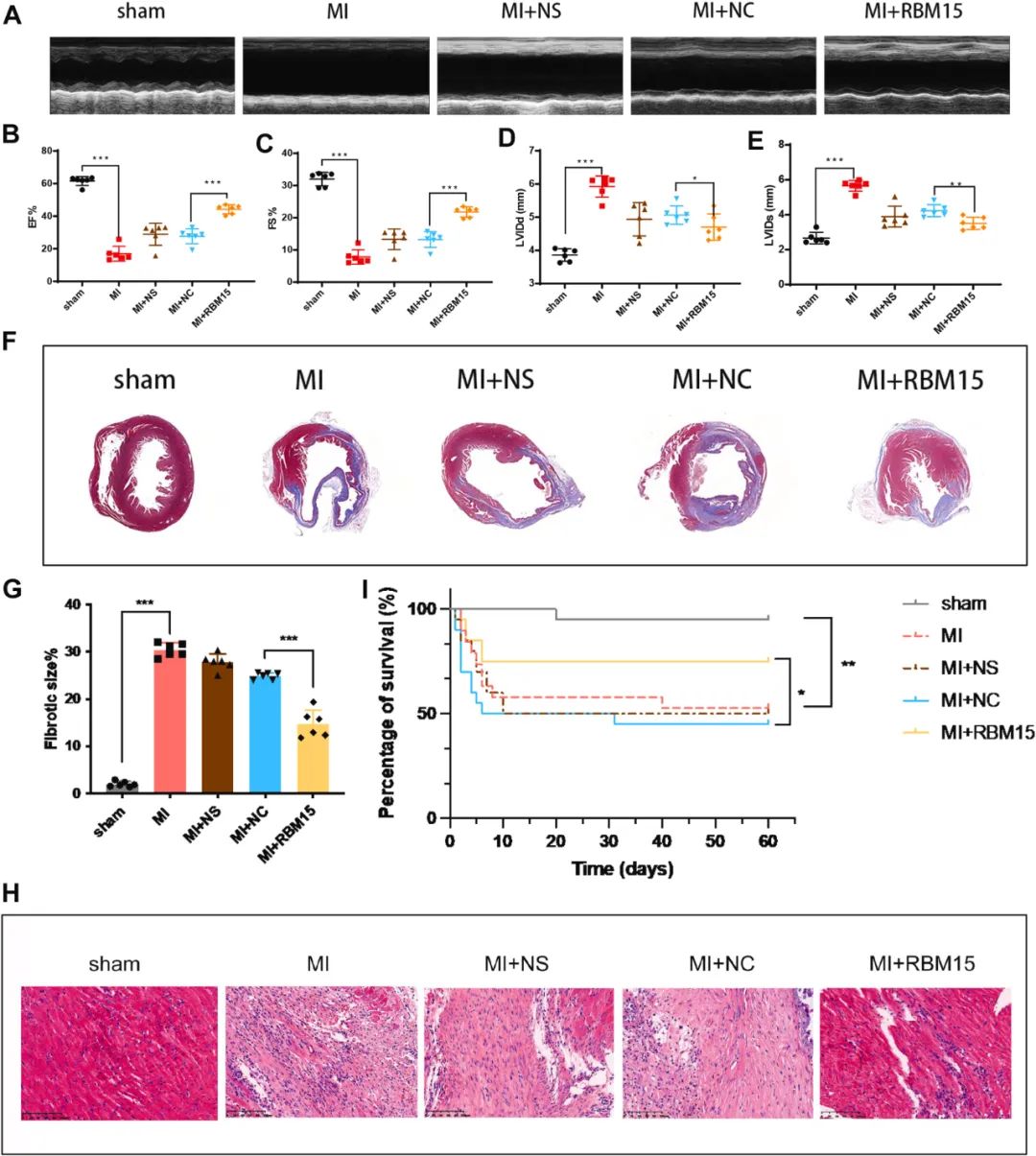
随后,研究者通过免疫印迹、免疫荧光等实验证实,RBM15过表达减轻了心肌细胞缺氧后的凋亡,进一步研究发现,RBM15过表达可以显著改善小鼠心梗后的心功能。这两项结果提示,RBM15有助于延缓小鼠MI后心功能的恶化。
在机制上,研究者通过测序分析,结果表明NAE1可作为RBM15发挥心梗后心脏保护作用的重要靶点。采用NAE1抑制剂(MLN4924)进一步证实,在RBM15过表达的情况下,m6A甲基化的增强导致NAE1 mRNA的稳定性增加,最终促进NAE1的高表达。

综上所述,本研究探讨表观修饰因子RBM15在MI中的生物学功能及其机制,RBM15可通过稳定其在细胞凋亡功能上的关键靶点来影响MI的进展,揭示了表观修饰机制可能是MI的治疗干预的潜在靶点。

复旦大学附属中山医院心血管内科程灏博士、吴剑副研究员为该文的共同第一作者,葛均波院士、马剑英教授为该文的共同通讯作者。复旦大学附属中山医院邹云增教授、李琳楠博士等合作者亦给予重要指导和贡献。该工作得到了多项国家自然科学基金及科技部重点研发计划的支持。
原文链接:
https://www.jacc.org/doi/10.1016/j.jacbts.2024.01.017- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)