首页 > 医疗资讯/ 正文
胶质母细胞瘤是最致命的恶性肿瘤之一,表现出明显的肿瘤内异质性,其中胶质母细胞瘤干细胞(GSCs)对肿瘤发生和治疗抵抗起着重要作用。泛素连接酶和去泛素化酶的药物调节剂正在开发用于癌症和其他疾病。
2024年3月19日,西湖大学谢琦,深圳湾实验室李磊和匹兹堡大学Jeremy N. Rich共同通讯在Cell Discovery 发表题为“RBBP6 maintains glioblastoma stem cells through CPSF3-dependent alternative polyadenylation”的研究论文。该研究进行了并行的体外和体内CRISPR/Cas9敲除筛选,针对人类泛素E3连接酶和去泛素化酶,揭示了E3连接酶RBBP6作为GSC维持的一个必需因子,靶向RBBP6抑制了GSC的增殖和肿瘤起始。
在机制上,RBBP6介导CPSF3的K63-链接泛素化,稳定了CPSF3来调节选择性多腺苷酸化事件。RBBP6敲除导致MYC竞争性内源性RNA的3'UTR缩短,从而释放了miR-590-3p从缩短的UTRs中,从而降低了MYC的表达。用小分子抑制剂(JTE-607)靶向CPSF3可以减少GSC的存活率并抑制体内肿瘤生长。总的来说,RBBP6通过调节CPSF3依赖的选择性多腺苷酸化在GSC中维持高MYC表达,为胶质母细胞瘤提供了一个潜在的治疗范例。

胶质母细胞瘤是最常见和致命的原发性脑肿瘤,中位生存时间不到两年。目前胶质母细胞瘤的标准治疗包括最大程度的手术切除,联合放疗和化疗,随后进行辅助化疗,只能提供姑息治疗。胶质母细胞瘤表现出肿瘤内异质性,其中自我更新的胶质母细胞处于层级顶端。胶质母细胞以其自我更新和肿瘤起始能力而功能特异化,此外还对肿瘤血管生成、放射抵抗力和化疗抵抗力有额外的贡献。
胶质母细胞瘤是最早进行全面遗传分析的肿瘤之一,揭示了导致信号传导失调的频繁变异,包括涉及表观遗传学变化、转录调节因子和转录后调节的变异。然而,基于遗传突变的精准医学对胶质母细胞瘤患者的临床管理影响有限,表明替代的分子靶点可能提供治疗益处。泛素化是调节底物蛋白命运和/或功能的最常见的翻译后修饰之一。泛素-蛋白酶体通路维持大多数蛋白质的稳态。泛素分子通过涉及E1(泛素激活)、E2(泛素连接)和E3(泛素连接酶)酶的催化级联添加到靶标蛋白中,可以通过去泛素化酶(DUBs)逆转。
先前的研究已将泛素途径与胶质母细胞瘤的生长总体和GSC的维持特异性联系起来。例如,胶质母细胞瘤可能过表达USP15,该酶结合SMAD7-SMAD特异性E3泛素蛋白连接酶2(SMURF2)复合物去泛素化并稳定型I转化生长因子-β受体(TβR-I),增强TGF-β信号传导。在GSCs中,USP9x取消乙醛脱氢酶1A3(ALDH1A3)的多泛素化以稳定ALDH1A3并维持GSCs。用USP9x抑制剂WP1130处理GSCs可诱导ALDH1A3降解并抑制GSC的生长。此外,USP13和FBXL14相互调节GSCs中MYC的多泛素化。因此,去泛素化酶和泛素连接酶可能是胶质母细胞瘤的潜在治疗靶点。
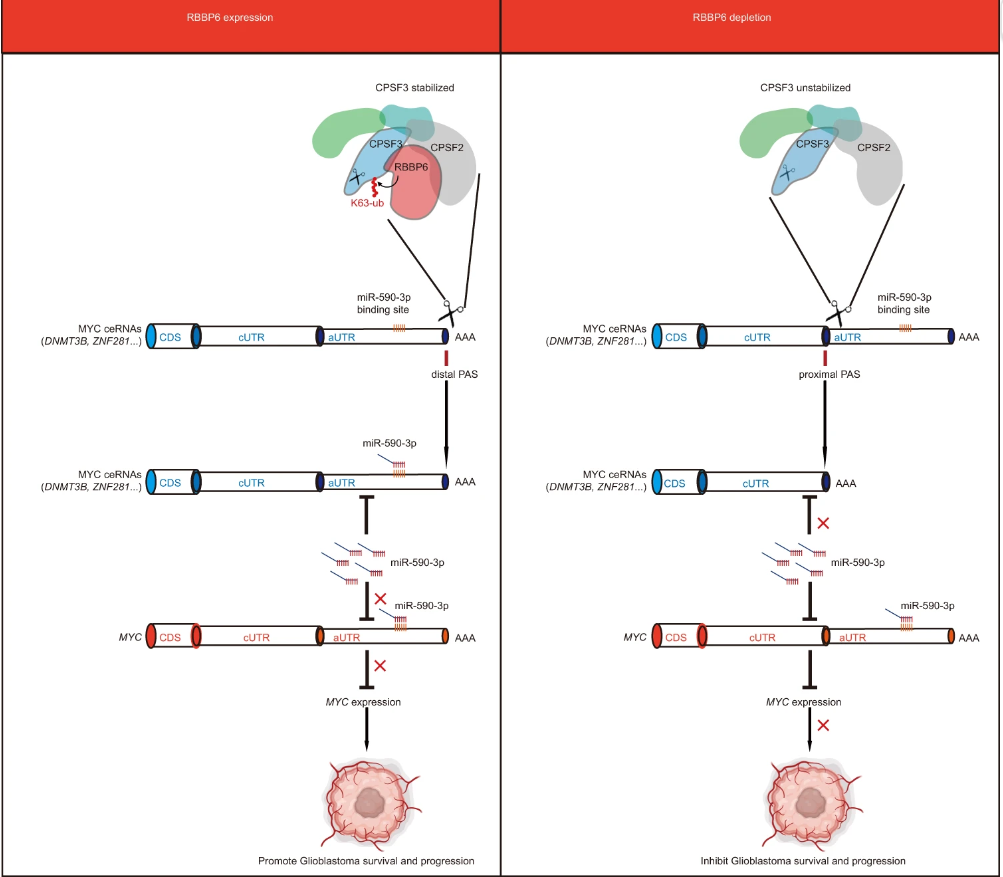
文章模式图(图源自Cell Discovery )
CRISPR/Cas9基因敲除(KO)高通量筛选已被证明是癌症治疗中目标基因发现的有效平台。先前的CRISPR筛选研究主要集中在体外培养的细胞模型上,这些模型无法充分代表肿瘤微环境的复杂效应,这种方法可能限制了药物开发的成功。在这里,作者改进了一种更具生理学相关性的体内CRISPR筛选方法,以识别对GSC维持和肿瘤形成至关重要的泛素连接酶和去泛素化酶。
参考消息:
https://doi.org/10.1038/s41421-024-00654-3
猜你喜欢
- 高烧不退抗生素无效孩子得了什么怪病?
- 骨质疏松的病因和诊断以及它的治疗
- 《柳叶刀子刊》:精神病性抑郁症治疗最新研究进展
- 山西省新增海外输入确诊1例 新冠肺炎为什么有轻重症
- Cancer Cell:乳腺癌中精氨酸-多胺-TDG通路如何“驯化”巨噬细胞,抑制T细胞抗癌能力
- 张宁谈多囊卵巢综合征诊治误区有哪些
- Int Orthop:锁骨完全移位粉碎性中段骨折保守治疗与手术治疗的综合比较
- 2018年11月16日健康简报,星期五!健康是一种生活态度!
- Clin Rheumatol:托法替布与TNF抑制剂治疗类风湿性关节炎的疗效比较
- JAMA Surg:长期遵循观察等待策略的直肠癌患者的生活质量和功能结局
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)