首页 > 医疗资讯/ 正文
肿瘤微环境中的病理血管生成会阻止免疫细胞有效浸润肿瘤,增加对免疫检查点阻断的抵抗性,抗血管生成药物如VEGF抑制剂能够重新编程肿瘤微环境,增强免疫检查点抑制剂的效果,高TMB (≥10 mutations/megabase)与免疫检查点抑制剂的客观反应率、无进展生存期等临床指标相关,目前,尚无关于TMB与阿替利珠单抗联合贝伐珠单抗一线治疗高TMB晚期非鳞状NSCLC的生存获益相关性的前瞻性研究,通过II期非随机对照试验评估阿替利珠单抗联合贝伐珠单抗在高TMB晚期非鳞状NSCLC患者中的临床疗效和安全性。

方法
该研究为一项多中心、单臂、开放标签的II期非随机对照试验,纳入患者治疗初治的年龄≥18岁、病理证实的IIIB-IV期非鳞状NSCLC、ECOG评分0-1分、无已知EGFR/ALK/STK11/MDM2/ROS1基因变异、TMB≥10 mutations/megabase或≥16 mutations/megabase (血液样本),患者接受阿替利珠单抗1200mg + 贝伐珠单抗15mg/kg,每21天为一个周期,直至疾病进展或不可耐受毒性,主要终点:12个月无进展生存率,次要终点:总体生存率、客观反应率、反应持续时间等,探索性分析:TMB与疗效的相关性、预测生物标志物等。数据截止时间:2022年2月28日。
纳入人群
该研究纳入了38名患者,全部为IIIB-IV期非鳞状非小细胞肺癌,平均年龄为63.7岁,73.7%为男性,94.7%有吸烟史,中位吸烟量为45包年,ECOG评分:42.1%为0分,57.9%为1分,92.1%为腺癌,50.0%有高血压,44.7%有血脂异常,31.6%有慢性阻塞性肺病,28.9%有糖尿病,所有患者TMB均≥10 mutations/megabase或≥16 mutations/megabase (血液样本),无已知EGFR/ALK/STK11/MDM2/ROS1基因变异。

研究结果
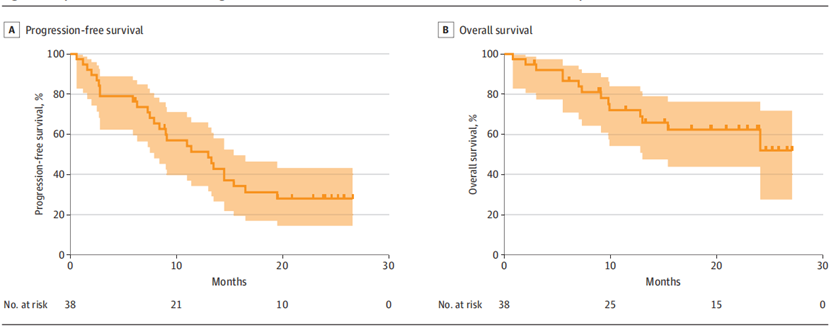
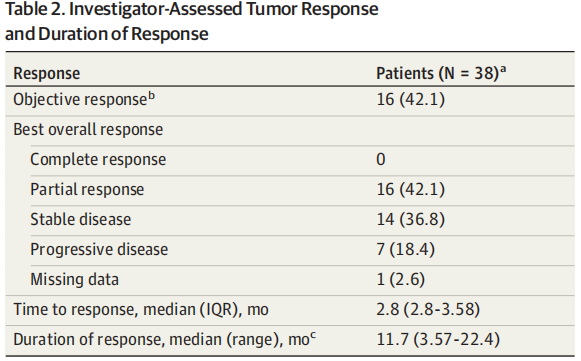
主要终点:12个月的无进展生存率为51.3%,达到研究的主要终点,表明该联合方案在控制肿瘤生长方面取得了显著的效果。次要终点:6个月和12个月的总体生存率分别达到86.6%和72.0%,显示出该方案在延长患者生存方面也有明显优势,42.1%的客观反应率显示,该联合方案对部分患者肿瘤的缩小和控制效果明显,11.7个月的中位反应持续时间表明,联合方案所引起的反应是持久的,未发现TMB水平与无进展生存率、总体生存率、客观反应率等疗效指标存在明显相关性,未发现与疗效相关的预测性生物标志物。
安全性
所有级别的不良反应中,阿替利珠单抗组最常见的是疲劳、瘙痒、乏食和腹泻,而贝伐珠单抗组最常见的是高血压和蛋白尿,3-4级不良反应中,阿替利珠单抗组包括肝功能异常、关节痛、关节炎、腹泻和胰酶升高,而贝伐珠单抗组包括高血压、肝功能异常、肛瘘、心肌梗死和血管病变,治疗中断和剂量调整主要出现在3-4级不良反应中,研究认为阿替利珠单抗联合贝伐珠单抗在该人群中的安全性良好,未发现新的安全信号。
结论
阿替利珠单抗联合贝伐珠单抗在高TMB晚期非鳞状NSCLC患者中显示了有希望的临床疗效和持久的反应,同时安全性良好,12个月无进展生存率为51.3%,符合研究的主要终点,6个月和12个月的总体生存率分别达到86.6%和72.0%,客观反应率为42.1%,反应持续时间为11.7个月,阿替利珠单抗联合贝伐珠单抗可能成为高TMB晚期非鳞状NSCLC患者的标准一线治疗方案,TMB水平与疗效无关,未发现与疗效相关的预测性生物标志物,研究存在局限性,需要进一步研究来验证这一联合方案的优越性。
原始出处
Provencio M, Ortega AL, Coves-Sarto J, et al. Atezolizumab Plus Bevacizumab as First-line Treatment for Patients With Metastatic Nonsquamous Non–Small Cell Lung Cancer With High Tumor Mutation Burden: A Nonrandomized Controlled Trial. JAMA Oncol. 2023;9(3):344–353. doi:10.1001/jamaoncol.2022.5959.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)