首页 > 医疗资讯/ 正文
前 言
2022年5月,第75界世界卫生大会通过了《2022-2030年全球卫生部门关于艾滋病、病毒性肝炎和性传播疾病行动计划》决议[1],《计划》提出,到2030年消除病毒性肝炎的公共卫生威胁。为了达到这一目标,美国肝炎防治基金会发布了《逐步简化慢性乙肝治疗标准》[2]:只要血清中可以检测到HBV DNA,不管ALT是否升高都干预治疗,这样才能实现WHO提出的80%治疗目标。由此,HBV DNA的检测的灵敏度被成功推上了“风口浪尖”上。
当前,HBV DNA定量检测的方法大多是荧光定量聚合酶链反应(polymerase chain reaction,PCR)技术,PCR具有敏感度高,特异度好,定量范围广,可以重复利用等优点[3]。但在临床实践中,影响PCR灵敏度的因素有很多,除了反应体系外,特殊标本的内源性成分也是重要的PCR抑制因素。本研究针对一例高脂血、溶血标本对HBV DNA结果的影响进行处理和分析,从而为本实验室制定可靠的解决方案,现报道如下。
案例经过
患者男性,45岁,既往“慢性乙型肝炎病毒感染病史”,艾米替诺福韦片及恩替卡韦胶囊口服抗病毒治疗,今于我院定期复诊。在为患者进行HBV DNA定量检测时,发现标本严重脂血合并溶血(图1),于是我们对标本进行高速离心(2500r/min,15min)处理,处理前后的血清均参与HBV DNA的提取扩增,并检测甘油三酯(TG)、血红蛋白(Hb)和总胆红素(TBil)水平。


图1 上图为普通离心,下图为高速离心
处理前后患者的HBV DNA定量扩增曲线如图2。
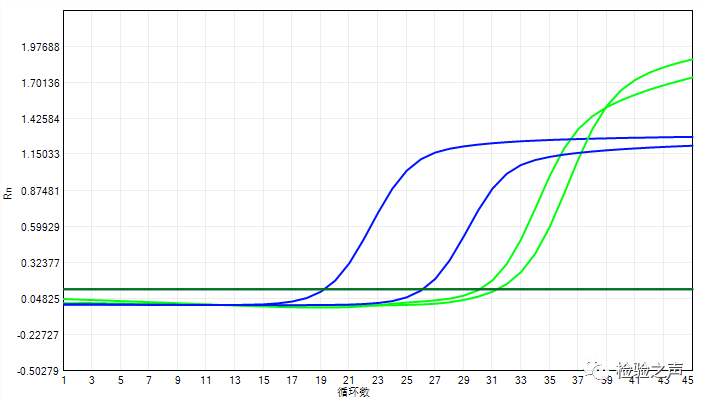
图2 HBV DNA扩增曲线(蓝色)从左到右为:处理后标本,处理前标本;绿色曲线为内标
处理前后患者的HBV DNA定量结果及偏倚如表1。
表1 处理前后患者的HBV DNA定量检测结果

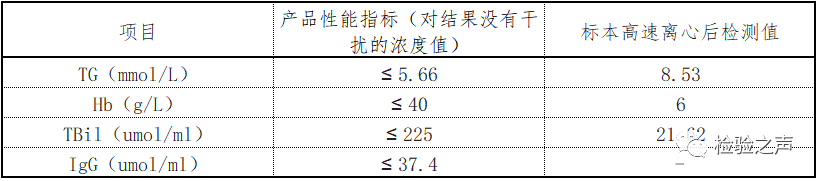
HBV DNA试剂盒说明书中产品性能指标内源性干扰物质的描述,和处理后患者的TG、Hb和TBil水平如表2。
表2 HBV DNA定量检测内源性干扰物质资料
案例分析
HBV DNA检测结果的准确性将影响临床治疗及预后判断,所以HBV DNA定量检测具有重要的临床意义[6]。检测 HBV-DNA 的方式主要依靠PCR,检测过程包括核酸模板的提取和扩增,很多干扰因素的都会导致结果发生变化,所以HBV DNA定量结果的准确性容易受到样本中抑制物的影响。临床上PCR抑制物主要有: TBil、Hb、IgG、TG和肝素等,这些物质来源于样本的中组分或处理样本过程中所产生,它们会降低模板的扩增效率,甚至造成低水平样本检测为假阴性结果,这将会延误治疗,造成病情反复。
研究[6]表明,血红蛋白是存在于RBC内PCR抑制物,它们抑制PCR反应可能与释放铁离子有关,从而干扰DNA合成,而胆红素是血红蛋白的衍生物,也会抑制PCR反应。TG抑制PCR反应原因为: ①高血脂会导致荧光猝灭,使得荧光信号强度降低; ②高血脂会抑制Taq酶的活性,从而使扩增效率降低。IgG对PCR反应抑制机制是与单链DNA相互作用,使得靶DNA不能与DNA聚合酶结合,而且当样本加热循环时,这种抑制作用会增强。另有研究表明[7],高脂血与溶血均会对PCR 检测 HBV-DNA 结果造成影响,建议在实验室检测时,注意做好相关措施,对于高脂血患者先接受降血脂治疗后再进行检测,对于溶血标本则建议再次抽取新鲜血液进行二次检测。蔡桂君[8]等报道利用淋巴细胞分离液分离全血中淋巴细胞提取人类疱疹病毒4型核酸,处理过程为取1ml全血标本加入等量无菌生理盐水稀释,加入2ml淋巴细胞分离液,2500r/min离心15min,小心吸取全部红细胞表面的白色细胞层,将白细胞层直接用于核酸提取。全血标本前处理方法均与全血血浆定量PCR检测结果对比,发现处理后明显高于未处理标本结果,且两种前处理过程中均能有效消除胆红素与血红素对定量PCR的影响。
本案例中,样本同时存在脂血和溶血,而且TG的浓度为8.53mmol/L,超出了产品性能指标的浓度值5.668.53mmol/L;Hb和TBil在产品性能指标范围内。标本处理前后的检测结果偏倚为27.61%,远远超出了±0.24的范围。因此我们认为,该样本的脂血状态,抑制了PCR反应,导致检测结果的减低,通过高速离心,可以在一定程度上减轻抑制物的干扰。
总 结
目前,大多数试剂盒对抑制物的干扰都有一定的处理能力,所以在遇到状态异常的黄疸、脂血和溶血样本时不能一律拒收,实验室应该按照 CNAS-CL02-A009:
2018《医学实验室质量和能力认可准则在分子诊断领域的应用说明》文件中的判断标准,对 HBV DNA定量检测试剂干扰进行评价,制订出适合本实验室的标准检测程序。对于重度的溶血样本,可以根据内标有无扩增曲线决定是否重抽样本;对于脂血的样本,可以通过高速离心进行检测;而对于重度的黄疸、脂血和高IgG样本,若内标无扩增曲线,或者目的基因扩增曲线出现异常,可以使用特征指标正常阴性血清稀释待测样本,从而降低抑制物对检测结果的影响,但同时一定要注意避免因过度稀释导致假阴性结果的发生。
参考文献:
[1]https://cdn.who.int/media/docs/default-source/hq-hiv-hepatitis-and-stis-library/full-final-who-ghss-hiv-vh-sti_1-june2022.pdf?sfvrsn=7c074b36_9.
[2]Wong RJ, Kaufman HW , Niles JK, et al. Simplifying treatment criteria in chronic hepatitis B: Reducing barriers to elimination[J]. Clin Infect Dis, 2022 May 20:ciac495.
[3]李育敏,徐怡,阚丽娟,等. 质控工具在荧光定量 PCR 测定HBV DNA 室内质控中的应用[J]. 检验医学与临床,2019,16(14):1993-1996.
[4] 王玮,鲁清月,李振红,等.实时荧光定量 PCR 检测临床标本的前处理方法研究进展[J].国际检验医学杂志,2018,39( 3) : 333-335.
[5] 中国合格评定家认可委员会.CNAS-CL02-A009: 2018《医学实验室质量和能力认可准则在分子诊断领域的应用说明》.
[6]胥明勇,吴泳桦,朱华强.PCR抑制物干扰HBV DNA试剂检测能力评价[J].四川医,2019,40(05):522-524.
[7]王晓川,吴英超,孙良起等.高脂血 溶血标本对聚合酶链反应测定低水平乙型肝炎病毒的脱氧核糖核酸检测结果的影响[J].实用医技杂志,2021,28(05):614-615.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)