首页 > 疾病防控/ 正文
男性不育症,是一种多因素异质性疾病,大约影响了7%的男性。非阻塞性无精症(NOA)是最严重的男性生殖系统疾病之一,指睾丸组织本身没有制造精子的能力,大约有1%的育龄男性会患此疾病。
2022年1月3日,中科院动物研究所高飞研究员、上海交通大学附属第一人民医院泌尿外科中心李铮教授等在 Signal Transduction and Targeted Therapy 期刊发表了题为:Oligomer-Targeting Prevention of Neurodegenerative Dementia by Intranasal Rifampicin and Resveratrol Combination – A Preclinical Study in Model Mice 的研究论文。
该研究揭示了 MSH5 基因突变是非阻塞性无精症(NOA)潜在致病原因,并在小鼠模型上证实了CRISPR/Cas9基因编辑能够修复该基因突变,产生成熟精子。

该论文对三名非阻塞性无精症(NOA)患者(编号为P8944、P7602、P7824)进行了研究,他们三人来自三个没有生育问题史的中国家庭。首先,研究团队对他们排除了男性不育的已知病因,包括隐睾症、性腺机能减退症、癌症、饮酒和吸烟。他们的生殖系统也发育正常,睾丸大小和FSH激素水平也相对正常。进一步检查显示,他们也不存在染色体异常。
为了进一步确定这三名患者的不育症原因,研究团队对他们进行了全外显子基因测序。
P8944患者的MSH5基因出现了四碱基缺失的纯合突变,该导致导致终止密码子提前,MSH5表达的蛋白缺失了587个氨基酸。而他的父母和兄弟姐妹则携带一个突变,因此并未患病。
而P7602和P7824患者情况相同,他们二人的MSH5基因出现了复合杂合突变,也就是说他们的两个MSH5等位基因均出现了突变,但突变位点不相同。
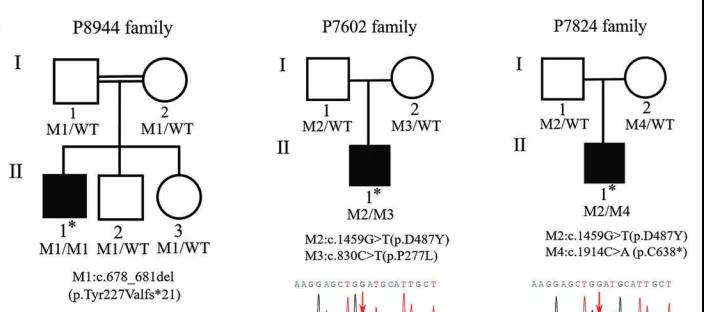
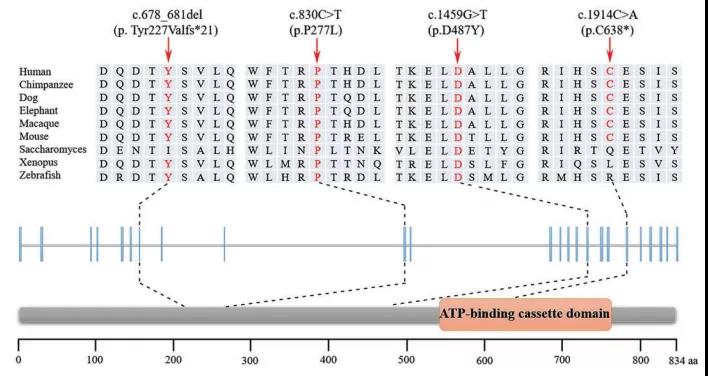
这三名患者出现的四个突变位点,在不同物种之间保守程度很高。
为了验证MSH5基因突变的功能,研究团队在小鼠上进行了研究,携带MSH5基因纯合突变的雄性小鼠的睾丸显着变小,且生精小管中出现大量凋亡细胞。这表明MSH5突变可能是非阻塞性无精症(NOA)的病因之一。不过这三名患者的睾丸大正相对正常,这可能是由于MSH5基因在人体和在小鼠中作用不完全相同所致。
CRISPR/Cas9系统是目前最强大的基因编辑技术,而且已经广泛应用于动物疾病模型和人体治疗。为了挽救上述MSH5基因突变小鼠,研究团队将CRISPR基因编辑组份(sgRNA、表达Cas9的质粒、MSH5基因的单链DNA模板)或MSH5基因质粒注射到小鼠生精小管中。注射后使用电穿孔技术提高转染效率,5周之后,在这些小鼠的生精小管中发现了少量的具有头部和尾部的成熟精子。但并未在附睾尾部发现成熟精子,这可能是由于该系统的基因编辑效率较低所致。还需要进一步研究以提高转染效率和编辑效果。
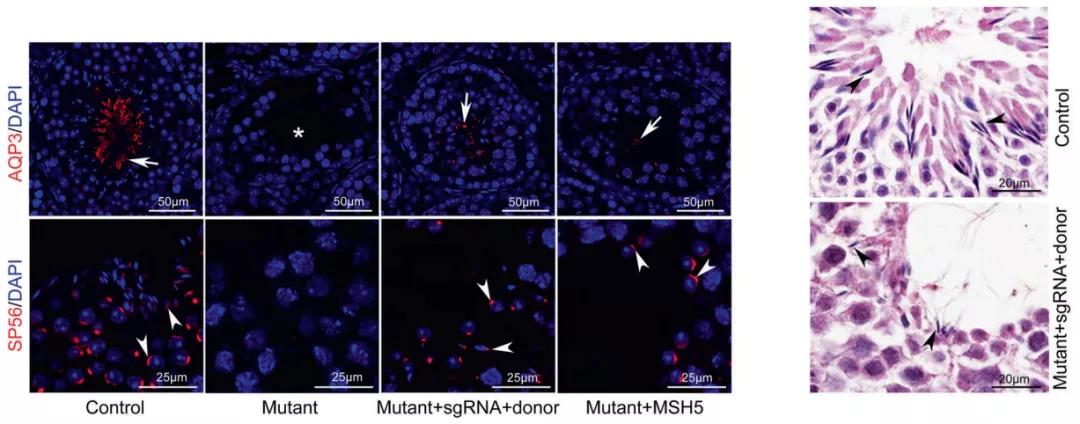
总的来说,该研究表明,MSH5基因突变是非阻塞性无精症(NOA)的潜在病因,公衡重要的是,该研究通过体内基因编辑修复了小鼠模型中的MSH5基因突变,这提示了该方法具有治疗男性生殖系统疾病的潜力。
原始出处:
Chen, M., Yao, C., Qin, Y. et al. Mutations of MSH5 in nonobstructive azoospermia (NOA) and rescued via in vivo gene editing. Sig Transduct Target Ther 7, 1 (2022). https://doi.org/10.1038/s41392-021-00710-4
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)