首页 > 医疗资讯/ 正文
头颈部鳞癌(HNSCC)年发病超过80万例,5年生存率仅为60%,顺铂耐药是主要瓶颈。CCT复合物是真核生物II类伴侣蛋白家族成员,由8个同源亚基组成,CCT与细胞蛋白质组中5-10%的蛋白质存在相互作用,并包括多种癌蛋白。其亚基CCT2在多种癌症中高表达且与预后不良相关,但其在头颈鳞癌中的作用机制不明。c-Myc作为关键致癌因子,直接靶向成药困难,故而靶向其上游调控蛋白或可成为新策略。此外,化疗诱导的凋亡囊泡可能通过传递相关分子促进肿瘤恶性进展。本研究重点探讨:1)CCT2是否通过稳定c-Myc驱动头颈鳞癌进展及耐药;2)凋亡囊泡是否通过传递CCT2传播耐药性。
1.CCT2在头颈鳞癌中高表达且与不良预后相关
通过对多个独立数据库的分析,发现CCT2在头颈鳞癌组织中显著高表达(图1A-B),且与不良预后相关(图1C-E)。对头颈鳞癌肿瘤样本的免疫组化结果也显示相较于癌旁正常组织,肿瘤组织呈现CCT2高表达,并与肿瘤增殖活性呈正相关(图1F)。进一步分析发现,CCT2表达水平与肿瘤临床分期显著相关(图1G)。在头颈鳞癌组织和多种头颈鳞癌细胞系中,CCT2 mRNA和蛋白水平的表达均显著高于正常细胞(图1H-J)。这些结果证实了CCT2在头颈鳞癌中的异常高表达特征,并揭示了其与肿瘤进展和不良预后的相关性。
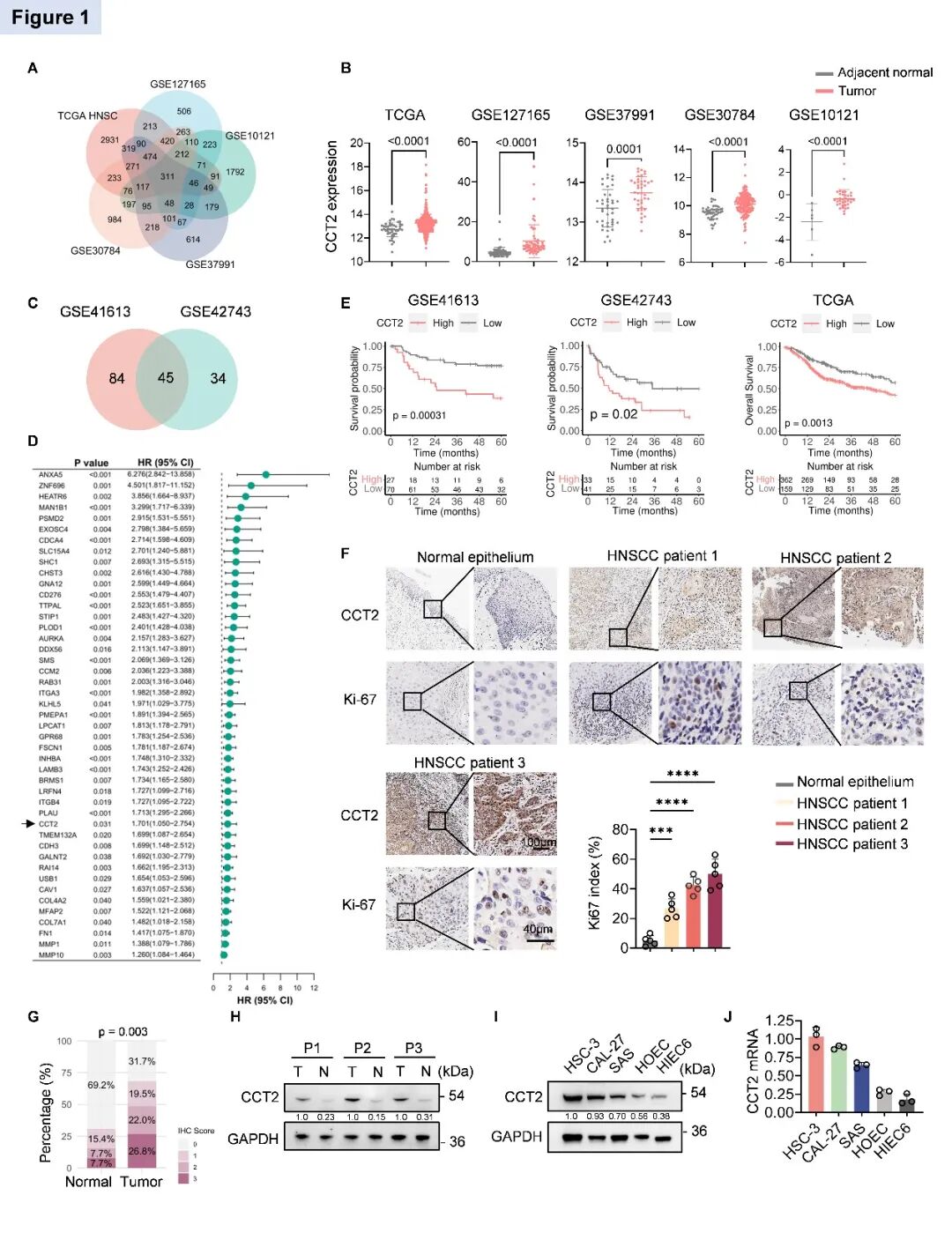
图1 CCT2在头颈鳞癌中的表达情况及其与预后的相关性(原文中Figure 1)
2.CCT2促进肿瘤增殖和细胞周期进展
在体外实验中,本研究选择不同CCT2表达水平的HSC-3和SAS细胞系,通过shRNA成功构建CCT2敲低模型(图2A&B)。功能实验表明,CCT2敲低显著抑制了肿瘤细胞的增殖能力和克隆形成潜能(图2C&D)。进一步机制研究发现,CCT2敲低导致细胞周期发生G1/S期阻滞(图2E),并调控了Cyclin D1、Cyclin E1和p21等关键周期调控蛋白的表达(图2F)。在体内实验中,CCT2敲低的移植瘤体积显著减小,生长速率明显降低(图2G-I)。免疫组化分析显示肿瘤组织中增殖标志物Ki-67表达显著下调,与体外实验结果一致(图2J)。这些发现证实了CCT2通过调控细胞周期进程促进头颈鳞癌增殖的重要作用。
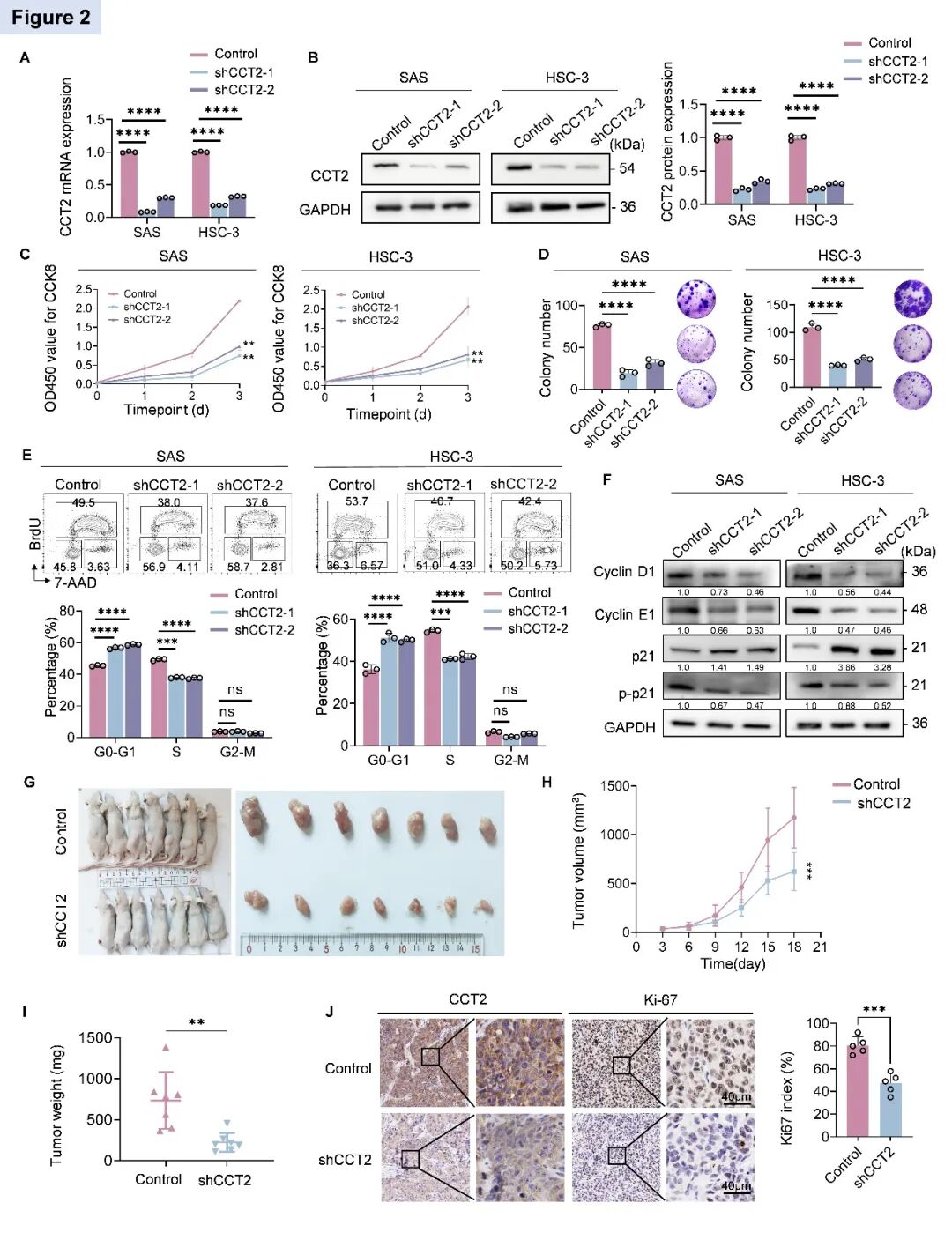
图2 CCT2对头颈鳞癌增殖能力的影响(原文中Figure 2)
3.增强迁移、侵袭及EMT过程
通过Transwell小室实验发现,敲低CCT2显著抑制了HSC-3和SAS细胞的迁移和侵袭能力(图3A)。划痕实验进一步证实,CCT2敲低延缓了伤口愈合速度,表明细胞迁移能力受损(图3B)。为更真实模拟肿瘤微环境,研究采用三维肿瘤球迁移实验,结果显示CCT2敲低组的肿瘤球迁移面积显著减小(图3C)。单细胞运动轨迹分析也观察到CCT2敲低细胞的运动速度明显降低(图3D)。机制研究表明,CCT2敲除导致上皮标志物E-cadherin表达升高,间质标志物N-cadherin、Vimentin和Slug表达降低(图3E)。这些发现证实CCT2通过促进EMT进程增强头颈鳞癌细胞的迁移和侵袭能力。
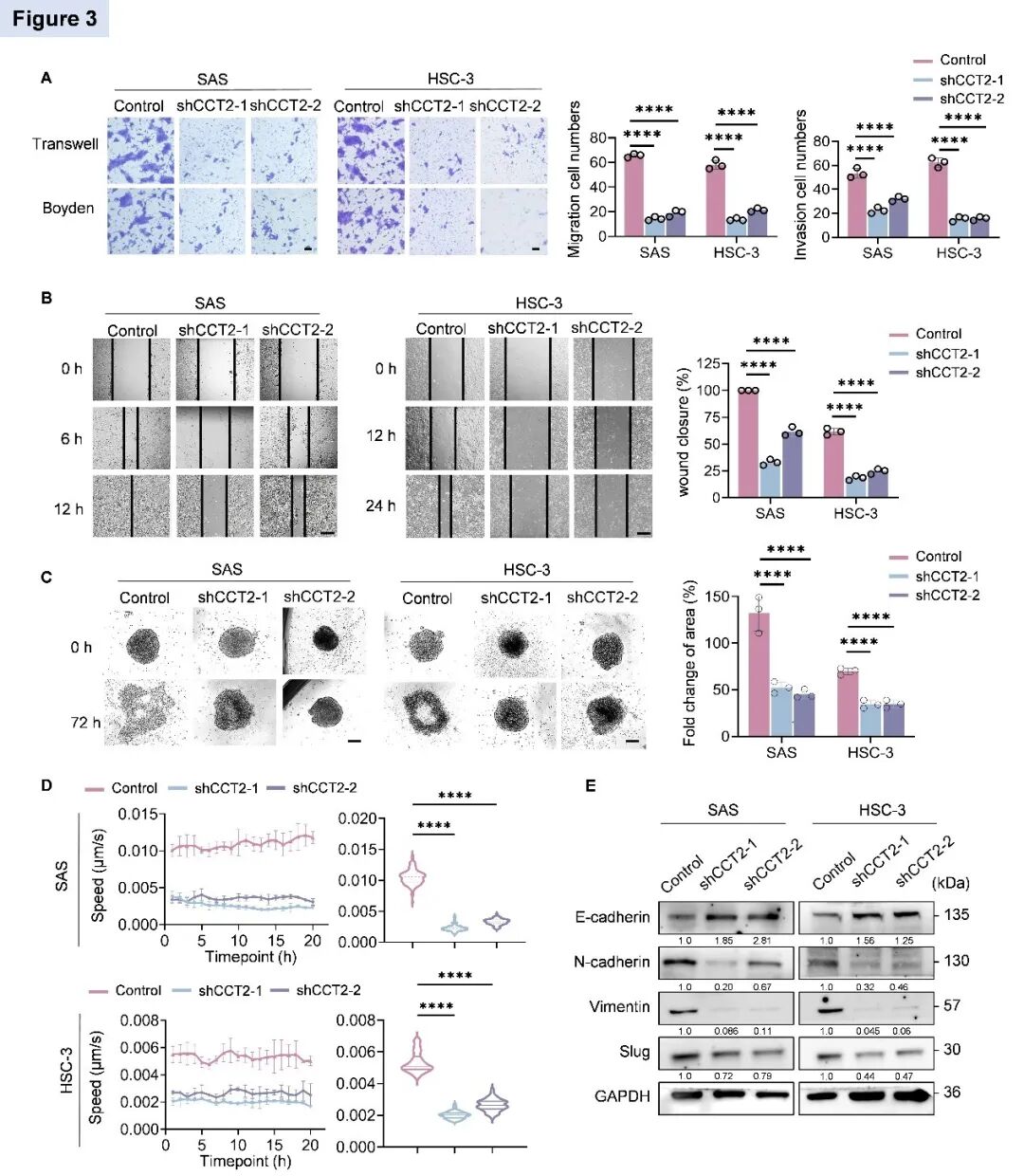
图3 CCT2敲低抑制了头颈鳞癌的侵袭和迁移(原文中Figure 3)
4.CCT2通过稳定c-Myc驱动顺铂耐药
研究发现,CCT2表达水平与头颈鳞癌细胞对顺铂的敏感性呈显著负相关:CCT2高表达的HSC-3细胞耐药性最强,而低表达的SAS细胞最敏感(图4A-C)。敲低CCT2可显著增强顺铂诱导的细胞凋亡(图4D),在动物模型中,CCT2敲低联合顺铂治疗显著抑制肿瘤生长(图4E-F)。分子机制研究表明,CCT2与c-Myc直接相互作用并延长其蛋白半衰期(图4G-K)。CCT2高表达导致c-Myc信号通路活化,并上调PCNA、CCND1等细胞周期相关蛋白的表达(图4L)。功能实验证实,c-Myc敲低亦可导致细胞周期阻滞、迁移能力下降和药物敏感性增加(图4M&N)。
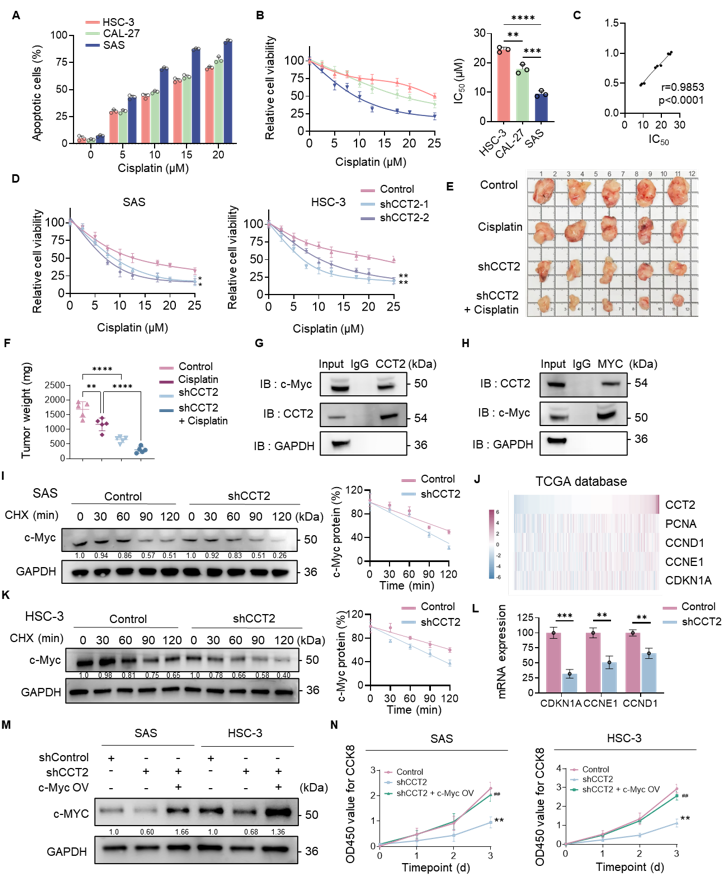
图4 CCT2介导顺铂耐药的机制(原文中Figure 5)
5.凋亡囊泡传递CCT2,介导耐药性扩散
本研究提取了顺铂诱导的HSC-3细胞来源的凋亡囊泡(图5A)。这些直径约226 nm的凋亡囊泡被顺铂敏感的受体细胞SAS摄取后,通过上调c-Myc及细胞周期蛋白的表达,加速细胞周期进程(图5I),从而增强SAS对顺铂的抵抗能力。CCT2敲低可显著削弱凋亡囊泡的耐药传递功能(图5J-L)。表明凋亡囊泡通过包裹CCT2向顺铂敏感细胞传递耐药性(图5M)。
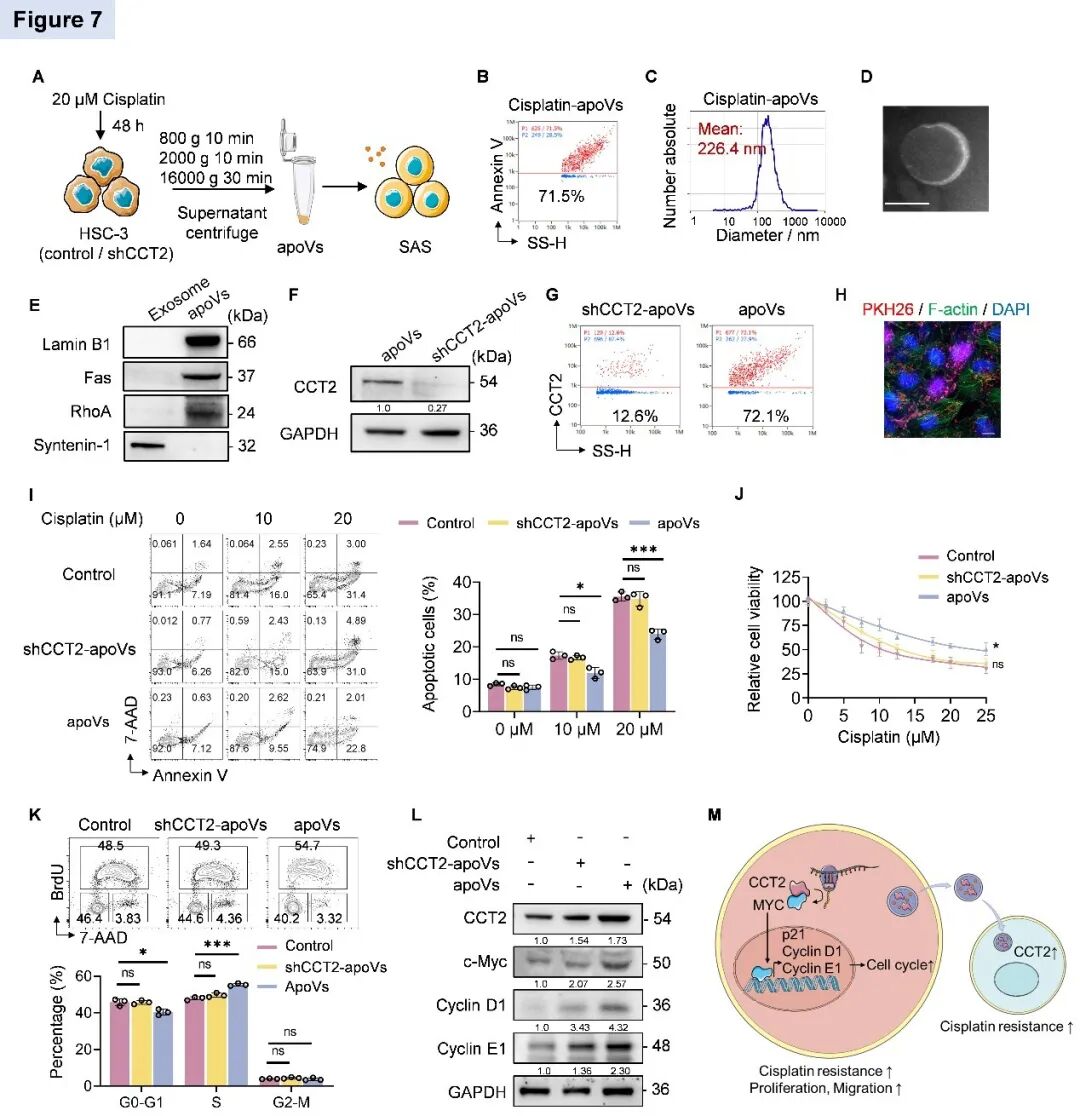
图5 凋亡囊泡传递CCT2扩散顺铂耐药性(原文中Figure 7)
总之,本研究阐明了CCT2-c-Myc轴在头颈鳞癌中的关键作用,并提出凋亡囊泡介导的非遗传性耐药新机制。结果表明,靶向CCT2或阻断凋亡囊泡的传递,可能为克服头颈鳞癌耐药提供新策略。进一步研究发现,CCT2通过稳定c-Myc促进头颈鳞癌进展及顺铂耐药,并首次揭示凋亡囊泡可介导CCT2的水平转移,从而扩大耐药细胞群体。基于上述发现,CCT2有望成为改善头颈鳞癌治疗效果的潜在新靶点。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304225002843
引用这篇文章:
Lu L, Shen Y, Li X, et al. CCT2 enhances c-Myc stabilization to drive tumor progression and chemoresistance in head and neck squamous cell carcinoma. Genes Dis. In Press.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)