首页 > 医疗资讯/ 正文
癌症相关成纤维细胞 (CAFs) 是肿瘤微环境的关键组成部分,其驱动胃癌 (GC) 进展和化疗耐药性。
2025年8月13日,复旦大学附属肿瘤医院许蜜蝶、盛伟琪,复旦大学Wang Wenfeng共同通讯在Advanced Science 在线发表题为“Exosomal CCT6A Secreted by Cancer-Associated Fibroblasts Interacts with β-Catenin to Enhance Chemoresistance and Tumorigenesis in Gastric Cancer”的研究论文。该研究发现,CCT6A 是一种 CAF 衍生因子,其高表达与 GC 进展呈正相关,并在干细胞特性、化疗耐药性和糖代谢中发挥关键调控作用。
在 CAFs 与癌细胞共培养体系中,研究发现 CCT6A 主要通过外泌体转运从 CAFs 转移到肿瘤细胞,从而增强干细胞特性、化疗耐药性和糖酵解。机制上,CCT6A 与 β-catenin 相互作用,诱导其磷酸化和核转位,进而通过激活 c-Myc 导致糖酵解抑制剂 DDIT4 和 TXNIP 的转录抑制。此外,研究还揭示了一个前馈调控环路,其中CCT6A假基因CCT6P1通过隔离miR-922充当竞争性内源RNA (ceRNA),从而稳定CCT6A的表达;而c-Myc则共激活CCT6A和CCT6P1,从而扩增致癌信号。总而言之,这些发现不仅揭示了CAF分泌的CCT6A在调控胃癌干细胞特性、化学耐药性和代谢重编程中的关键作用,还强调了其作为诊断生物标志物和治疗靶点的双重作用。

胃癌 (GC) 是全球第五大常见恶性肿瘤,也是全球癌症相关死亡的第二大原因,每年新增病例超过 100 万,死亡人数约 77 万。中国的胃癌发病率和死亡率尤其高。尽管多模态疗法已取得进展,但化疗仍然是局部晚期和转移性胃癌的主要治疗手段。然而,化疗耐药性的出现严重限制了治疗效果,这凸显了以下迫切需求:1) 揭示耐药机制;2) 识别预测性生物标志物;3) 制定克服治疗耐药性的策略。应对这些挑战有助于早期发现耐药肿瘤,指导及时干预以防止复发,并揭示新的治疗靶点以改善患者预后。
癌症相关成纤维细胞 (CAFs) 是胃癌 (GC) 肿瘤基质的主要成分,其起源于正常成纤维细胞 (NFs),后者在肿瘤信号刺激下被激活。CAFs 不仅构成了肿瘤微环境 (TME) 的重要组成部分,还参与调控驱动胃癌恶性肿瘤发生的复杂分子相互作用。越来越多的证据表明,CAFs 通过多种机制在介导胃癌耐药性方面发挥重要作用,这些机制包括细胞外基质重塑、分泌促肿瘤因子以促进血管生成和上皮-间质转化 (EMT)、代谢重编程以支持肿瘤增殖和转移,以及诱导免疫抑制微环境。例如,CAFs 激活胃癌细胞中的 YAP 信号,从而促进 5-Fu 化疗耐药性。同时,作者之前的研究表明,CAFs通过激活CXCR2/PI3K/Akt通路分泌IL-8,从而促进胃癌细胞对奥沙利铂产生耐药性;而PDPN(+) CAFs则通过激活AKT/NF-κB和CCL2-ACKR1轴诱导胃癌细胞血管生成。
含伴侣蛋白的TCP1复合物(CCT)是一个分子伴侣家族,在调节癌细胞周期进程、生长和迁移方面发挥着关键作用。CCT复合物的ζ亚基CCT6A是一种分泌蛋白,由两个相同的环堆叠而成。其表达在各种恶性肿瘤中频繁上调,包括非小细胞肺癌(NSCLC)、神经胶质瘤、黑色素瘤、结直肠癌(CRC)和睾丸癌,这主要是由于7p11.2染色体区域的扩增。功能上,CCT6A已被证实通过抑制SMAD2和激活促转移性TGF-β信号传导来促进非小细胞肺癌(NSCLC)进展,而外泌体CCT6A可作为胶质母细胞瘤的潜在预后生物标志物。此外,CCT6A在肺癌中发挥致癌基因的作用,并与结直肠癌(CRC)肿瘤微环境中的T细胞耗竭有关。先前的研究强调了CCT6A在上皮组织中的显著过表达,这与胃癌(GC)的不良预后相关。然而,CCT6A在GC中的具体作用和潜在机制仍然很大程度上未知,值得进一步研究。
该研究确定CCT6A是一种关键的CAF衍生因子,与GC的化疗耐药性、代谢重编程和不良预后密切相关。通过功能和机制分析,证明CAF衍生的外泌体CCT6A通过β-catenin/DDIT4-TXNIP/c-Myc轴促进GC细胞干性、顺铂耐药性和糖酵解。值得注意的是,该研究发现了一种新的竞争性内源性RNA (ceRNA)机制,其中CCT6A假基因CCT6P1吸附miR-922上调CCT6A。此外,c-Myc转录共激活CCT6P1和CCT6A,形成一个自我强化的致癌环路。总而言之,该研究结果揭示了胃癌细胞中CAF驱动的化学耐药和代谢适应轴,表明CCT6A有望成为治疗基质介导肿瘤进展的靶点。
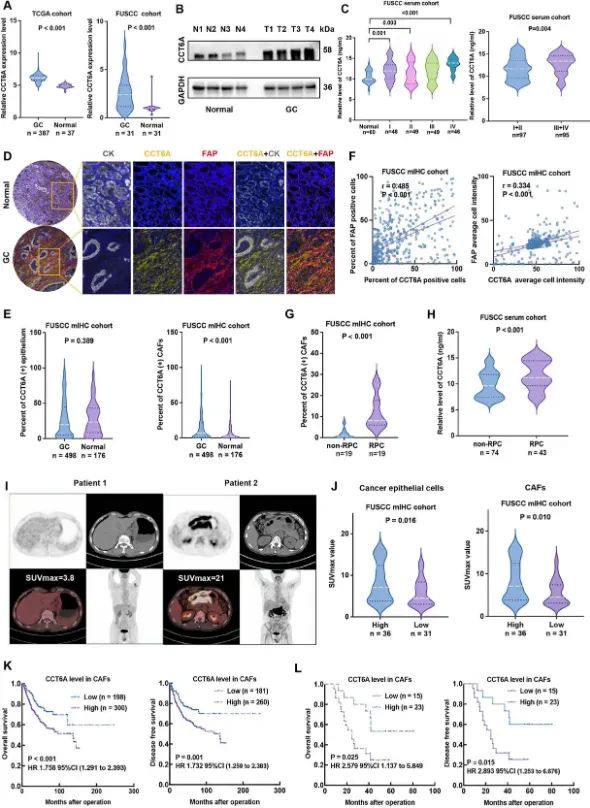
图1 CAFs 中的 CCT6A 表达与胃癌患者的化学耐药性、葡萄糖代谢和不良生存率相关(图源自Advanced Science)
参考消息:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202506674
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)