首页 > 医疗资讯/ 正文
胆汁淤积性肝病(CLD)是一类由胆汁形成、分泌和/或排泄障碍引起的肝脏疾病,其主要特征是胆汁酸和其他毒性代谢物在肝内积聚,造成胆管细胞和肝细胞损伤。原发性胆汁性胆管炎(PBC)和原发性硬化性胆管炎(PSC)是慢性CLD最常见的类型。长期、严重胆汁淤积会导致肝纤维化、肝硬化甚至肝癌,危及生命。CLD早期缺乏特异性临床症状,加之有效诊断工具缺乏,常常导致确诊延迟。当患者出现黄疸、肝衰竭或门静脉高压症状时,往往已属疾病中晚期,治疗效果受限。且当前治疗多为对症处理,缺乏针对病因的疗法,导致患者预后不佳,生存质量和预期寿命均受到严重影响。因此,探索精准诊疗和前沿治疗策略意义重大。本文拟从CLD的诊断进展、生物标志物探索、靶向药物治疗到未来个体化治疗模型构建等角度进行系统性述评,旨在为推动CLD从“经验治疗”向“精准干预”转变提供思路。
1流行病学
CLD的发病率至今尚未有精准统计数据。曹旬旬等针对上海市4 660例住院慢性肝病患者开展的调研中,胆汁淤积的总体发生率为10.26%。研究还发现,年龄与慢性肝病患者胆汁淤积的发生存在相关性,随着年龄的增长,胆汁淤积的发生率呈上升态势。Bortolini等开展的针对初次确诊慢性肝病患者的研究显示,在2 520例新诊断的慢性肝病患者中,882例(35%)存在胆汁淤积现象,且胆汁淤积在PBC和PSC患者中更为常见。
PBC的全球总体年发病率为1.76/10万,患病率为14.6/10万。PBC主要影响40~70岁的成年女性,发病率和患病率随着年龄的增长而增加,在60~79岁时达到高峰。在过去20年中,全球成年男性发病率的增加降低了女性与男性的比例,女性与男性的比例已从9∶1逐渐下降至4~6∶1。与女性相比,患有PBC的男性在诊断时肝病处于更晚期,肝细胞癌的发病率增加,预后更差。此外,男性PBC患者对熊去氧胆酸(UDCA)的生化反应率更低。
PBC的发病率和患病率因地区而异。相较于欧洲地区(1.86/10万),北美地区PBC发病率更高(2.75/10万),亚太地区最低(0.84/10万)。患病率趋势与发病率相同,北美地区为21.81/10万、欧洲地区为14.59/10万、亚太地区为9.82/10万。2000年后,全球PBC的发病率持续上升。此后,北美地区和欧洲地区的增长率趋于平稳,而亚太地区的发病率继续缓慢增加。随着时间的推移,3个地区的PBC患病率均持续上升。最新研究显示,亚洲地区的PBC患病率(11.9/10万)可能高于既往报道的水平,地区差异表明日本和中国的患病率更高(19.1/10万)。
最近研究表明,PSC的总体发病率为每年0.77/10万。大多数PSC患者的年龄在25~45岁,中位诊断年龄为41岁。尽管90%的PSC患者患有炎症性肠病,但只有2.4%~4%的溃疡性结肠炎(UC)患者和1.4%的克罗恩病患者患有PSC。在患有PSC和UC患者中,60%~70%为男性,不过在未患UC的PSC患者中,女性略占多数(女性与男性的比例为1∶0.8)。PSC与肝胆恶性肿瘤以及结直肠癌之间的关联已得到明确证实,10.9%的PSC患者患有胆管癌,患UC和PSC的患者患结直肠腺癌的风险是普通人群的5倍。遗传因素(一级亲属中有患PSC的兄弟姐妹,患病风险增加11倍)、不吸烟以及其他自身免疫性疾病是增加PSC患病率的风险因素。
2诊断进展:从经典指标到组学赋能
CLD的诊断模式正经历着显著转变,由传统指标逐步发展为多组学数据综合模式。经典的免疫标志物是自身免疫性肝病的诊断基础。在PBC患者中,抗线粒体抗体M2亚型(AMA-M2)是最常见的抗体,90%~95%的患者可检测出该抗体。其中,对于AMA-M2阴性的PBC,针对GP210(核孔糖蛋白210)和SP100(核点蛋白100)的自身抗体具有一定的诊断价值,尽管其检测的特异性高,但敏感性较低。Li等研究发现,AMA-M2阳性或阴性PBC患者血清中抗pIgR自身抗体的表达水平均显著升高,提示血清抗pIgR自身抗体水平可作为PBC潜在的诊断标志物。而对于PSC而言,尚缺乏特异性抗体标志物,血清中核周抗p-ANCA(中性粒细胞胞浆抗体)在PSC患者中检出率相对较高,但特异性低,目前仍缺乏理想的血清学标志物用于早期诊断或疾病分型。
肝穿刺活检仍是评估慢性肝病肝损伤程度的金标准。但因其属于侵入性操作,存在一定风险,肝硬化晚期患者需慎重考虑。不同病因下,肝组织学表现各异,通常包括胆管增生、纤维化和炎症,如PBC常表现为非化脓性破坏性胆管炎和小胆管破坏,PSC常见胆管丧失和“洋葱皮”样纤维化。
基因诊断的快速发展极大地促进了遗传性胆汁淤积性疾病的确诊。新一代高通量基因测序能够实现多基因同时检测,有效加快了诸如Alagille综合征、进行性家族性肝内胆汁淤积症(PFIC)等单基因病的确诊,同时也证实了ABCB4(ATP结合盒转运体亚家族B成员4)等基因变异在不明原因胆汁淤积中的致病性。由此,开发了涵盖52个基因(包括非编码变异)的Panel,为遗传性胆汁淤积性疾病的确诊提供了高效、准确的方法。
此外,基于RNA测序的转录组学解决了微阵列的局限性,已有研究得出了疾病表达谱,但尚未转化为临床诊断工具,不过作为早期的预示指标仍然值得探索。蛋白质组学能够分析胆汁蛋白谱,从而鉴别出PSC与胆管癌,但是由于难以通过外周抽血而获得胆汁,只能从体内获取,加之胆汁酸干扰等原因,目前尚未普及,人类肝脏蛋白质组计划将有望解决标准化的问题。代谢组学是检测分析反应通路最终代谢产物的重要技术,已有研究通过胆汁酸谱分析来鉴别PBC和PSC,但由于技术标准化不理想,以及人类代谢组数据库尚未建立完善,因此目前仍局限于机制研究层面。
3治疗策略:从经典药物到靶向干预
CLD的治疗模式正从传统药物向精准靶向干预转变。UDCA作为PBC一线治疗,可改善生化指标并延缓疾病进展,但30%~40%患者应答不佳,且对PSC疗效不明确;其衍生物去甲熊去氧胆酸(Nor-UDCA)通过增强肝胆分流与免疫调节,在PSC中展现出降低ALP水平的潜力。核受体靶向药物是近年研究热点,法尼醇X受体(FXR)激动剂中,奥贝胆酸(OCA)曾获批用于UDCA应答不佳的PBC患者,但因其临床获益不大于风险,2024年在欧洲宣布撤市;非甾体FXR激动剂(如Cilofexor、Tropifexor)可改善ALP水平且瘙痒副作用较轻,有望成为新一代替代药物。过氧化物酶体增殖物激活受体(PPAR)激动剂可通过调控胆汁酸合成与炎症通路发挥治疗作用,贝特类药物(苯扎贝特/非诺贝特)已获亚太肝病学会指南推荐用于UDCA应答不佳者;新型选择性激动剂如Seladelpar(PPARδ)、Elafibranor(PPARα/δ)及Saroglitazar(PPARα/γ)在Ⅱ期试验中显著降低ALP水平,且耐受性良好。
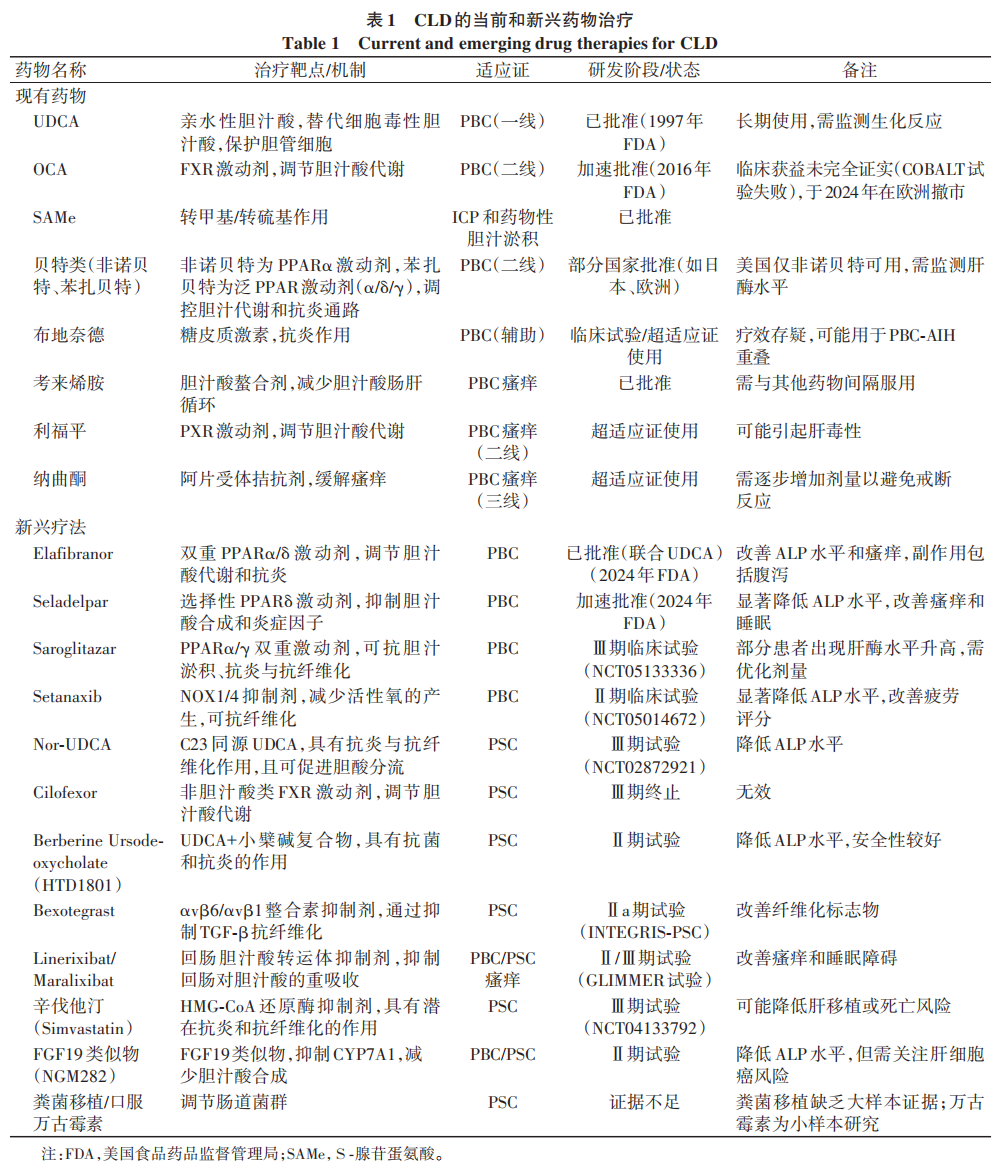
其他前沿策略包括以下几种。(1)微生物组干预:抗生素可降低PSC患者ALP水平(33.2%)及梅奥风险评分(36.1%);粪菌移植使30%患者ALP水平下降≥50%,其疗效与特定菌群丰度相关。(2)靶向生物制剂:FGF19(成纤维细胞生长因子19)类似物NGM282可抑制胆汁酸合成,在PBC/PSC中降低ALP水平达50%。(3)基因治疗:针对遗传性胆汁淤积(如PFIC),AAV载体介导的ABCB4基因递送在动物模型中可修复胆汁酸代谢(表1)。
4前沿探索:从机制研究迈向精准医疗
4.1 分子机制与新靶点
随着对CLD分子机制研究的不断深入,诸多潜在的新靶点逐渐浮现。一方面,深入剖析胆汁酸代谢、免疫调节和纤维化进程中的关键分子通路,如FXR、PPAR等核受体信号通路的精细调控机制,为开发更具针对性的治疗靶点提供了理论依据。另一方面,肠道菌群与肝脏之间的“肠-肝轴”相互作用机制备受关注,研究发现肠道菌群的失衡可通过影响胆汁酸代谢、免疫反应等途径参与CLD的发生发展,这使得调节肠道菌群成为潜在的治疗靶点,有望通过微生态制剂等干预手段改善疾病进程。此外,一些细胞内信号通路,如Janus激酶-信号转导和转录因子、核因子-κB等在炎症和纤维化中的关键作用被揭示,针对这些通路的关键节点开发靶向药物,可能为CLD的治疗带来新突破。
4.2 个性化治疗
由于CLD患者在疾病发展阶段、治疗效果及遗传背景等方面存在诸多差异,个性化治疗已成为重要的发展趋势。基因检测技术的快速发展,可进一步了解患者的遗传易感因素。通过对CLD相关基因,如胆汁酸转运蛋白基因等的多态性进行分析,可以预测患者对各种药物治疗的反应以及预后情况,进而实现精准用药。例如,已知某些基因变异会影响患者对UDCA的治疗反应,对于这类患者,可提前调整治疗方案。同时,将临床表现、实验室检查结果、影像学特征以及各种分子生物学资料相结合,构建多维度的疾病评估体系,才能为每个患者选择更精准的个性化治疗方案,提高治疗效果,改善患者的生活质量。
4.3 新型药物与临床试验
在寻求克服传统治疗药物局限性的过程中,新药物的研发和临床试验正积极推进。新型药物研发方面,将优化已上市的药物靶点,如新的FXR激动剂、PPAR激动剂等。此外,具有创新机制的药物也不断涌现。如Setanaxib(GKT831),这是一种靶向NOX1/4(烟酰胺腺嘌呤二核苷酸磷酸氧化酶1/4)抑制氧化应激的药物,在PBC患者的Ⅱ期试验中,展现出改善肝纤维化、降低胆汁淤积标志物水平和缓解症状等方面的治疗潜力。临床试验方面,多中心随机对照试验明显增多,不仅关注药物的治疗效果,安全性和长期预后也越来越受关注。真实世界研究方法的应用,可进一步评估新型药物在真实临床环境中的有效性和安全性,加快了新型药物从实验室走向临床应用的进程。
5小结
CLD的诊治是由多学科协作完成的,临床经验的不断积累和基础研究的不断增加,促使一批新的治疗方案及新型靶向药物取得了积极进展,但如何实现对CLD进行早期诊断及精准化治疗等问题仍存在挑战。未来还应加强对分子机制的研究,进一步阐明CLD的遗传学、免疫学和代谢学基础,为CLD精准化治疗和个性化治疗提供科学依据。FXR激动剂类、PPAR激动剂类等新型药物,极大丰富了药物治疗的范围,而CLD的药物治疗正向个体化联合治疗模式和机制靶向模式发展。此外,组学技术(包括基因组学、转录组学、蛋白组学、代谢组学及微生物组学)和人工智能算法相融合,已逐渐影响CLD研究与管理模式的发展。未来通过多组学整合、人工智能辅助决策、治疗靶点药物的更新和完善,以及来自真实世界研究数据的反馈,将共同推动CLD的早期识别、精准治疗和精准管理,提高CLD患者的生活质量,改善远期预后。
全文下载
https://www.lcgdbzz.org/cn/article/doi/10.12449/JCp50701

- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)