首页 > 医疗资讯/ 正文

急性右心室衰竭(ARVF)是最容易被忽视但却最致命的临床综合征之一。这种由右心室充盈障碍和/或射血功能受损引起的急性病变,常常伴随体循环瘀血,发病率与死亡率持续居高不下。最近发表在《欧洲心脏杂志》上的权威综述为我们提供了全面的诊疗指导,让我们重新审视这一临床挑战。
右心室的独特解剖生理基础
解剖结构的特殊性
右心室在解剖学上由三个独特部分构成:流入道(包含三尖瓣装置)、小梁化乳头肌区域以及流出道。与左心室的三层心肌结构截然不同,右心室仅含两层心肌:纵向排列的内层心肌和源自左心室的外层环状纤维。这种结构差异决定了右心室的功能特点。
更为重要的是,左心室收缩通过室间隔收缩及维持体循环和右冠状动脉灌注压,贡献约20-40%的右心室压力生成,这种贡献在病理状态下更为显著。心室间相互依赖源于共享的环状纤维、室间隔和心包腔,其中后两者分别是收缩期与舒张期相互依赖的主要介质。

血供特点与缺血耐受性
右心室游离壁血供几乎全部来自右冠状动脉的锐缘支,冠脉灌注可发生于舒张期与收缩期。由于右心室氧需求低、氧储备高、室间隔双重血供及良好的侧支循环,使其对缺血的耐受性较左心室更强。
压力-容积关系与负荷适应
右心室壁较薄(质量仅为左心室的1/6)、顺应性更高,能够在不显著增加舒张末压的情况下适应静脉回流的大幅波动,同时维持相对恒定的每搏量。后负荷包含稳定成分与脉动成分:稳定成分通常以肺血管阻力(PVR)表示,脉动成分由肺血管系统的波反射产生,其强度受肺血管顺应性、心率和左房压影响。
心室-肺动脉耦联
心室-肺动脉耦联是理解急性右心衰的关键概念。动脉弹性(Ea)与右心室收缩末期弹性(Ees)的比值定义为右心室-肺动脉耦联:
-
最优耦联:Ees/Ea = 1时,右心室向肺动脉的势能传递达最佳状态
-
生理状态:Ees/Ea = 1.5-2,实现最大效率和最低能耗
-
失耦联:Ees/Ea < 0.7-1.0时,代偿机制耗竭进入右心室衰竭

急性右心衰的病因与发病机制
主要病因分类
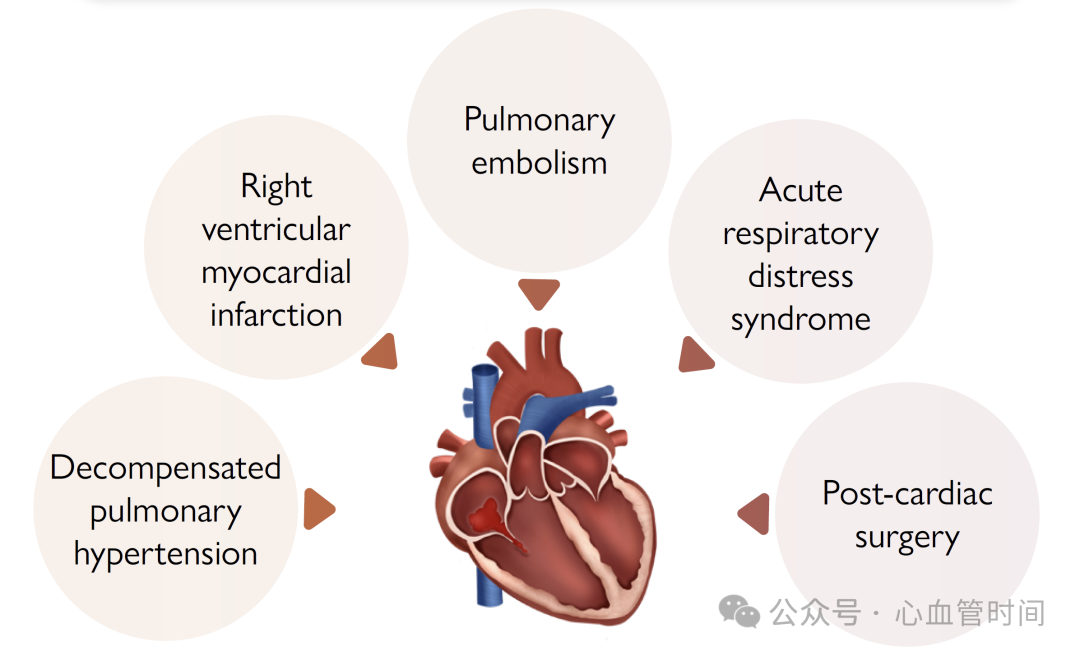
慢性右心衰的病因可大致分为压力超负荷、容量超负荷或心肌损伤三种类型。但单纯容量超负荷导致急性右心衰较为罕见,因此ARVF主要由压力超负荷、心肌损伤所致,而两者共同作用更为常见。

急性肺栓塞:右心功能障碍是影响急性肺栓塞预后的关键因素。若无慢性压力超负荷导致的右心室肥厚,右心室无法对抗50-60 mmHg的肺动脉压。初始代偿通过等长自身调节实现,后负荷进一步增加将导致右心室扩张。
右心室梗死与缺血:ARVF多由右冠状动脉近端闭塞引发,约30-50%的下壁心肌梗死患者合并此症。虽然影像学证实右心室梗死存在,但许多临床病例表现为短暂性缺血损伤,尤其是成功再灌注患者。射血分数低于40%会导致右心衰患者更大的血流动力学损害和更高的住院死亡率。
急性呼吸窘迫综合征:约20%的ARDS患者存在右心功能障碍,且与死亡率升高相关。右心室收缩力降低与PVR升高是ARDS相关右心功能障碍的核心机制,可由缺氧、高碳酸血症、酸中毒、肺微血栓、肺泡死腔增加等诱发。
心脏手术:ARVF是心脏术后严重并发症,**院内死亡率高达70-75%**。在体外循环心脏切开术后、心脏移植术后和接受左心室辅助装置植入的患者中,发生率分别为0.1%、2-3%和20-30%。
慢性肺动脉高压急性失代偿:由于肥厚的右心室才能产生更高压力,右心室压>50-60 mmHg时多提示慢性病变。院内死亡率高达15-20%,ICU患者中达40%。
病理生理恶性循环
急性右心衰的标志是右心室扩张。当失代偿后,右心室扩张试图维持每搏量,但会引发进行性收缩功能障碍、静脉充血、左心室充盈不足、心输出量降低、低血压及缺血等恶性循环,最终导致临床表现失代偿及循环崩溃。
全身低血压降低右冠状动脉灌注压,叠加右心室室壁张力增加及心肌氧耗上升,导致右心室缺血——这是右心室失代偿的重要机制。若发展至三尖瓣环扩张继发三尖瓣反流,可加速右心室扩张-功能障碍的恶性循环。
诊断评估的多维度策略
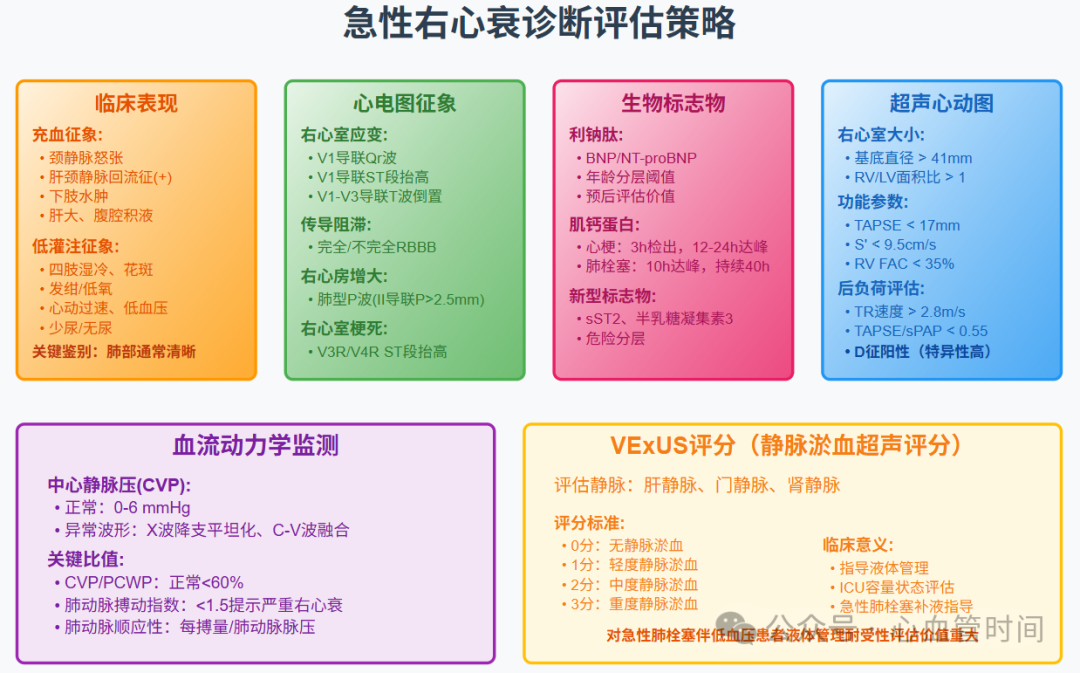
临床表现识别要点
ARVF的临床表现并非总具有高度特异性,可因基础疾病不同而存在差异。患者常表现为:
充血征象:颈静脉怒张、肝颈静脉回流征阳性、下肢和骶部水肿、肝大、腹腔积液低灌注征象:四肢湿冷、皮肤花斑、发绀/低氧、心动过速、低血压、少尿/无尿、精神状态改变心脏听诊:P2亢进(肺高血压征象)、第三心音、三尖瓣反流收缩期杂音肺部体征:肺部通常清晰(除非合并左心室收缩功能障碍和肺水肿的右心室心肌梗死病例)
心电图
心电图的敏感性较低,主要价值在于识别右心室损伤征象:
右心室应变征象:V1导联Qr波、V1导联ST段抬高、V1-V3导联T波倒置(急性肺栓塞不良预后的预测因子)传导阻滞:完全性或不完全性右束支传导阻滞心律失常:窦性心动过速或房颤/房扑(最常见发现)右心房增大:肺型P波(II导联P波>2.5 mm)右心室梗死特征:V3R/V4R导联ST段抬高和R波缺失(与近端RCA闭塞相关但不能预测右心室功能障碍严重程度)
生物标志物
肌钙蛋白作为心肌损伤标志物,在不同病因中表现模式不同:
-
心肌梗死:3小时内检出,12-24小时达峰,持续10-14天
-
肺栓塞:10小时达峰,早期检测可能假阴性,仅持续40小时,峰值低于心肌梗死
利钠肽(BNP或NT-proBNP)可作为心衰失代偿及预后不良的标志物,但特异性不足。新型生物标志物如和肽素、生长分化因子15、心型脂肪酸结合蛋白等临床应用价值尚待进一步证实。
超声心动图评估
经胸超声心动图是评估ARVF患者右心室结构和功能的主要手段,虽然因右心呈不对称新月形且位于胸骨声学屏障后方需通过多个切面评估,但通过心尖四腔切面对右心室大小和功能的直观评估仍可获取多个重要参数:
右心室大小评估:
-
舒张末期右心室基底直径:>41 mm(异常)
-
RV/LV面积比:>1(早期发现,代偿机制)
功能参数:
-
TAPSE:<17 mm(评估纵向功能,但角度依赖、负荷依赖)
-
S'速度:<9.5 cm/s(评估纵向功能)
-
右心室面积变化分数:<35%(近似右心室射血分数)
-
右心室心肌做功指数:>0.54(整体收缩和舒张功能评估)
后负荷评估:
-
三尖瓣反流速度:>2.8 m/s(用于计算右心室收缩压)
-
肺动脉加速时间:<105 ms(肺动脉压升高的可靠标志)
-
TAPSE/sPAP比值:<0.55 mm/mmHg(右心室/肺动脉耦联的替代标志)
心室相互作用:
-
D征阳性(室间隔弯曲,右心室功能障碍高度特异性标志)
-
下腔静脉直径:>21 mm且吸气塌陷<50%
静脉淤血评估:VExUS评分通过肝静脉、门静脉和肾静脉多普勒检查评估静脉淤血的存在及严重程度,为ICU中急性肺栓塞伴低血压以及急性失代偿性毛细血管前肺动脉高压患者的液体管理耐受性提供重要信息。
血流动力学评估
前负荷及中心静脉压:正常仰卧位CVP为0-6 mmHg。通过CVP波形中特征性表现可辅助识别右心室功能障碍:X波降支平坦化、C-V波融合以及V波显著增大。
后负荷评估:由于右心室后负荷由阻力性和脉动性成分共同构成,肺动脉顺应性(每搏输出量与肺动脉脉压的比值)可作为右心室后负荷的替代指标,其在肺栓塞中的预后价值优于PVR。在ARDS中,即使PVR正常,低肺动脉顺应性仍可预测死亡率。
心肌收缩力受损:肺动脉搏动指数(肺动脉压与CVP的比值)整合了后向衰竭和前向衰竭的血流动力学特征,可预测下壁心肌梗死和左心室辅助装置植入后的右心衰竭。研究显示,该指数与右心室心肌细胞功能关联更为密切。
心室间相互依赖:正常情况下,**右心房压力不应超过PAWP的60%**。严重右心衰时,心室间依赖性增强,CVP可能接近、等于甚至超过PAWP。
治疗管理的循证策略
综合治疗原则
ARVF治疗策略包括优化前后负荷、增强心肌收缩力、纠正低氧及机械循环支持。为快速有效治疗右心衰,经验丰富的多学科团队参与至关重要。

容量优化策略
容量优化过程复杂,应在初期评估时谨慎处理。对于伴有低血压的右心衰患者,若VExUS显示无静脉淤血且CVP监测提示充盈压低,可考虑给予少量补液。但需注意过度的右心室前负荷可能导致临床状况恶化。
关键监测指标:在快速补液过程中,若CVP突然升高(即较基线值增加>5 mmHg),继续补液可能无法改善每搏输出量,反而加剧右心室扩张。结合心输出量监测的被动抬腿试验是评估补液是否会引起心输出量增加的可靠且简便方法。
减容指征:若VExUS显示轻至重度静脉淤血,且CVP超过8-12 mmHg,或接近、等于甚至超过PAWP时,通过减容降低右心室前负荷可以改善左心室充盈,重建更有利的心室容量状态。
利尿剂抵抗处理:患者对高剂量袢利尿剂无反应可能由多种因素导致,包括中心静脉压升高伴肾静脉淤血、低血压、低心排及急性肾损伤。尽管确切疗效尚未明确,但越来越多的证据支持早期积极高剂量利尿策略的安全性。
血管活性药物应用
血管收缩剂:去甲肾上腺素等血管收缩剂可使动脉压高于肺动脉压,从而促进双心室收缩耦联、提高冠状动脉灌注。
正性肌力药物:为改善右心室收缩力并应对低心输出量,多巴酚丁胺、磷酸二酯酶III抑制剂及左西孟旦等药物可能具有益处:
多巴酚丁胺与米力农的直接对比研究显示两者临床结局相当,均具有相似的血流动力学效应及诱发心律失常的潜在风险。米力农经肾脏清除且半衰期较长,更易降低右心室和左心室的舒张末期压力,同时具有强效的肺循环及体循环血管扩张作用。
左西孟旦可通过增强右心室收缩力、扩张肺血管改善右心室-动脉解偶联,但其外周血管扩张效应可能加重左心室充盈不足。
药物选择策略:正性肌力药物的选择因病因不同而异。对于慢性肺动脉高压急性失代偿患者,米力农易诱发低血压及右心室缺血,此时多巴酚丁胺为优选;但若急性右心衰继发于左心衰,米力农或左西孟旦可能更具优势。
呼吸支持策略
ARVF患者常出现显著低氧血症,需进行氧疗,目标是维持动脉血氧饱和度高于90%。正压通气可能增加肺血管阻力和胸腔内压,从而减少静脉回流,导致右心室前负荷降低并显著增加右心室后负荷,使用需审慎评估。
针对ARDS的保护性通气策略:维持平台压≤27 cmpO,PaCO2<60 mmHg,根据右心室功能调整PEEP,对氧合指数<150 mmHg的患者建议俯卧位通气。
肺血管扩张治疗
对于失代偿性毛细血管前肺动脉高压患者,可通过吸入或肠外途径应用前列腺素类及一氧化氮等药物降低右心室后负荷:
吸入制剂:可最大限度减少体循环低血压,同时避免通气/血流比例失调的进一步恶化。一氧化氮常用于心脏术后患者,尤其对原位心脏移植术后发生右心衰者具有显著应用前景。
静脉前列环素类似物:可有效降低右心室后负荷,但需谨慎预防体循环低血压;左心疾病患者可能出现肺水肿等不良反应。
机械循环支持
临时机械循环支持通常用于治疗难治性ARVF患者,可作为过渡至恢复或移植的桥梁:
VA-ECMO:通过静脉-动脉体外膜肺氧合间接减轻右心室前负荷,置管可在ICU完成。对于急性肺栓塞或失代偿性毛细血管前肺动脉高压引发ARVF患者,VA-ECMO可能更有效。
右心室辅助装置(RVAD):直接卸载右心室压力,需在导管室经导管快速经皮植入。预计需长时间支持患者时,优先选择允许患者下床活动的RVAD(如Impella RP Flex或Protek Duo)。
治疗效果:近期研究表明,42-75%的ARVF患者可通过设备支持恢复足够功能以实现撤机。为减少感染、血栓栓塞或肢体低灌注等并发症,建议尽量在5-10天内逐步撤除MCS装置。
特定病因的针对性治疗
高危肺栓塞:对于高危肺栓塞,即合并梗阻性休克的PE,溶栓治疗仍是治疗基石。然而,其出血风险高(尤其是颅内出血)及临床应用禁忌症多,致使现实世界中的使用受限。
导管定向治疗(CDTs):已成为管理高危及中高危PE患者并ARVF的关键干预手段。导管定向治疗因其能快速降低血栓负荷,同时显著减少全身性溶栓相关风险,已成为当前治疗流程的核心手段。
-
导管定向溶栓术:可实现溶栓药物靶向投递至血栓部位,用药剂量较系统性溶栓治疗大幅降低
-
机械取栓术:通过专用大口径导管直接抽吸血栓,对于存在溶栓禁忌的患者优势明显
右心室梗死:成功的经皮冠状动脉介入治疗若实现右冠状动脉主干及主要右室分支的完全再灌注,可立即改善右心室功能并最终完全恢复。相反,即使RCA主干再灌注成功,若未能恢复右室分支血流,往往导致右心室恢复不良及高院内死亡率。
预后评估与临床意义
不良预后的预测因素
多项研究表明,以下因素与急性右心衰患者不良预后相关:
血流动力学指标:
-
肺动脉搏动指数<1.5:最佳右心室功能标志物
-
CVP/PCWP>0.86:提示心室间相互依赖性增强
-
持续低血压和低心排
实验室指标:
-
肌钙蛋白升高(肺栓塞的预后价值已获证实)
-
利钠肽持续升高
-
乳酸升高、酸中毒
影像学指标:
-
CT测得的RV/LV直径比值>1:对ARVF患者预后具有提示意义
-
室间隔弯曲(对右心室功能障碍高度特异)
-
下腔静脉造影剂反流
治疗反应评估
有效治疗的标志:
-
利尿剂治疗后2小时尿钠含量>50-70 mmol
-
起初6小时内尿量>100-150 ml/h
-
血流动力学参数改善
利尿剂抵抗的识别:当患者对加用二线利尿剂仍无反应时,若血肌酐水平接近基线,建议超滤治疗;若存在急性肾损伤,则需启动肾脏替代治疗。

要点总结
急性右心室衰竭在重症医学领域面临独特挑战,及时诊断与综合管理策略至关重要。关键要点包括:
早期识别:结合临床表现(颈静脉怒张、肺部清晰)、特征性心电图改变、生物标志物升高及超声心动图发现
精准容量管理:基于VExUS评分和血流动力学监测,避免过度补液导致右心室进一步扩张
个体化药物治疗:根据病因选择合适的升压药和正性肌力药,慢性肺高压患者优选多巴酚丁胺,继发于左心衰者可选择米力农
适时机械支持:42-75%的患者可成功撤机,关键在于把握启动时机
病因针对性治疗:肺栓塞患者的导管定向治疗、右心室梗死的完全血管再通
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)