首页 > 医疗资讯/ 正文
FGFR家族成员突变在转移性膀胱癌中频繁发生。泛FGFR抑制剂厄达替尼的研发为膀胱癌治疗带来了重大进展,但其疗效仍受耐药性限制。
2025年6月16日,武汉大学肖行远,华中科技大学蒋国松和张辉共同通讯在Cancer Research 在线发表题为“A Genome-Wide Synthetic Lethal Screen Identifies Spermidine Synthase as a Target to Enhance Erdafitinib Efficacy in FGFR-Mutant Bladder Cancer”的研究论文。该研究通过对厄达替尼处理的FGFR突变膀胱癌细胞系进行全基因组CRISPR-Cas9合成致死筛选,发现亚精胺合成酶(SRM)是介导厄达替尼耐药的关键因子。
机制研究表明,SRM催化生成的亚精胺可促进真核翻译起始因子5A(eIF5A)的羟丁赖氨酸修饰,进而显著提升HMGA2的翻译效率,最终导致表皮生长因子受体(EGFR)表达上调。值得注意的是,SRM的药理学抑制在体外和体内实验中均能增强厄达替尼的疗效。这些研究结果证实,靶向SRM可通过抑制HMGA2翻译进而降低EGFR转录,从而增强FGFR突变膀胱癌细胞对厄达替尼治疗的敏感性。

膀胱癌是全球范围内发病率和死亡率的重要来源。在初次确诊时,25%的患者已进展为肌层浸润性膀胱癌(MIBC)或转移性疾病。与非肌层浸润性膀胱癌相比,MIBC表现出更为多样的突变谱。此外,MIBC中FGFR家族成员的异常改变频发,且与不良预后相关。因此,采用选择性FGFR抑制剂进行靶向治疗,成为膀胱癌中致癌性FGFR激活改变的重要干预策略。
泛FGFR酪氨酸激酶抑制剂厄达替尼基于BLC2001研究结果,已获得美国食品药品监督管理局(FDA)加速批准用于FGFR2/3驱动的尿路上皮癌患者。另一项II期临床试验显示,厄达替尼在尿路上皮癌中具有40%的客观缓解率和5.5个月的中位无进展生存期。然而,获得性耐药的快速出现显著降低了厄达替尼的疗效。尽管已有研究报道脂肪前体细胞可通过NRG1/HER3轴介导膀胱癌对厄达替尼的耐药,但癌症内在的耐药机制尚未明确。近年来,CRISPR-Cas9系统为癌症脆弱性的无偏筛选提供了技术支撑,多项研究已鉴定出可增强FGFR抑制剂疗效的合成致死(SL)靶点,如肝癌中的EGFR以及肺癌中的PLK1和MTOR。但基于合成致死策略的疗效可能取决于不同肿瘤类型的遗传背景,目前尚未见全基因组水平筛选膀胱癌厄达替尼耐药相关靶点的报道。因此,仍需通过系统性筛选来确定可增强厄达替尼靶向治疗效果的SL靶点。
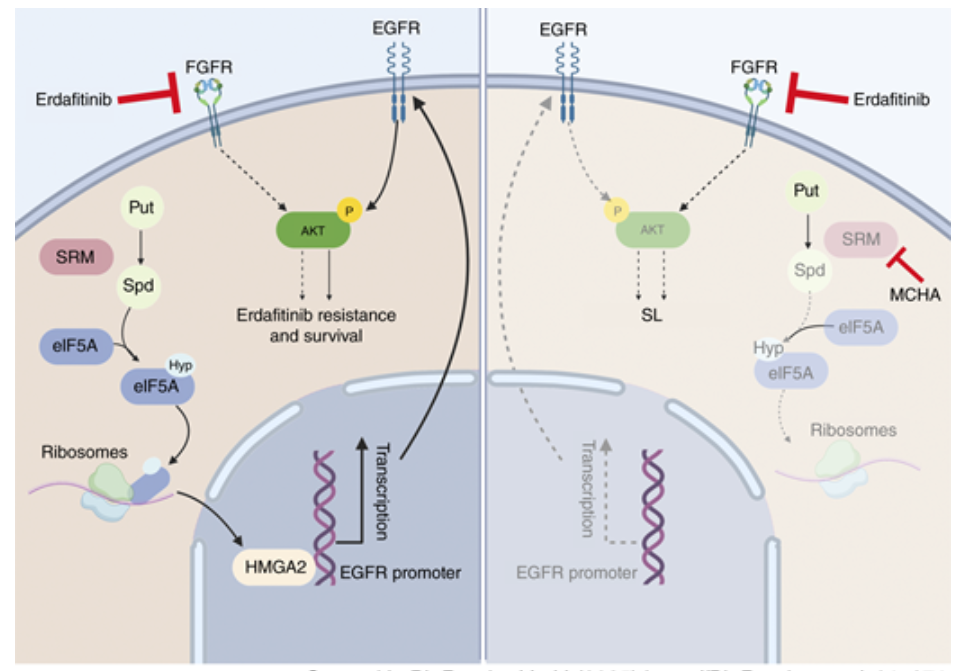
模式机理图(图片源自Cancer Research)
代谢重编程已被广泛认为是癌症的重要特征。多胺代谢紊乱与多种癌症相关,其水平升高对细胞转化和肿瘤进展至关重要。既往研究表明多胺代谢可能影响膀胱癌的生长和化学治疗敏感性,但其机制尚未阐明,且多胺代谢是否参与厄达替尼靶向治疗仍有待探索。作为多胺代谢的关键酶,亚精胺合成酶(SRM)催化腐胺转化为亚精胺,后者继而作为底物参与真核起始因子5A(eIF5A)保守赖氨酸残基的羟腐胺赖氨酸化修饰。羟腐胺赖氨酸化的eIF5A(eIF5AHyp)可特异性促进含特定基序的mRNA亚群的高效翻译。然而,SRM与eIF5A在调控膀胱癌厄达替尼耐药中的功能及分子机制仍有待揭示。
为全面探索潜在的联合治疗策略,作者通过全基因组CRISPR-Cas9合成致死筛选鉴定出SRM基因缺失可增强厄达替尼疗效。具体而言,SRM敲除(KO)与厄达替尼联用显著抑制肿瘤生长,而单独敲除SRM对膀胱癌细胞影响甚微。机制研究表明,SRM缺失通过eIF5A羟腐胺赖氨酸化途径显著减弱HMGA2的翻译。此外,HMGA2可结合EGFR启动子区域,其敲低可降低EGFR表达。重要的是,采用反式-4-甲基环己基氨基(MCHA)药物抑制SRM能显著增强厄达替尼疗效。因此,MCHA与厄达替尼的合成致死疗法可能成为提高膀胱癌靶向治疗应答率的新策略。
原文链接:
https://doi.org/10.1158/0008-5472.CAN-24-3217
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)