首页 > 医疗资讯/ 正文
食管癌流行状况与防筛及早诊
一、我国食管癌流行状况与特点
2022年我国食管癌发病率为15.87/10万,死亡率为13.28/10万,位居全部恶性肿瘤发病和死亡的第6位和第5位。我国食管癌病理类型以鳞癌为主,约占所有食管癌的86%。食管癌在我国呈现明显的城乡和地域差异,农村地区食管癌发病率和死亡率均高于城市地区,农村高发区主要集中在太行山脉附近、淮河流域以及四川、广东和福建等地。男性食管癌的发病率和死亡率均高于女性。随着经济水平的发展和医疗条件的改善,我国食管癌的发病率和死亡率每年以3%~6%的速度下降,下降趋势显著,食管癌的5年生存率已提高到33.4%,长期开展食管癌人群整合防治的地区,五年生存率已达38.3%,但食管癌的整体预后仍然较差,社会和经济负担依然沉重。
二、我国食管癌主要病因
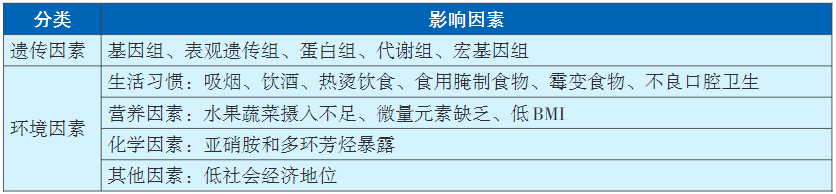
食管癌是多种环境因素与遗传因素共同作用的结果。既往流行病学研究对食管癌的病因学进行了大量探索,确定的主要危险因素包括吸烟、饮酒、热烫饮食、腌制食物、霉变食物、不良口腔卫生状况、水果蔬菜摄入不足、微量元素缺乏、低BMI、亚硝胺和多环芳烃暴露以及低社会经济地位等。归因分析显示,我国48.5%的食管癌归因于不良饮食和生活方式。基于全基因组关联分析和候选基因策略的研究已经报告了一系列食管癌的易感基因位点。此外,表观遗传组、蛋白组、代谢组宏基因组等多组学研究提示甲基化水平、microRNA、蛋白表达、代谢特征以及菌群分布等均与食管癌的发生发展有关。
三、我国食管癌主要防治措施
食管癌的一级预防主要是针对消除各种危险因素采取措施,包括戒烟、限酒、营养均衡以及改变不良生活方式。目前,我国食管癌二级预防措施主要是在高发区和高危人群中实施基于色素/电子染色内镜检查,辅以组织活检为核心的筛查及早诊早治方案,并根据内镜和病理检查出的各级别食管癌前病变进行定期随诊或微创治疗,拒绝进行内镜检查的患者,可以用食管癌甲基化检测试剂盒初筛。大规模人群队列和随机对照试验研究的结果显示,现行的筛查方案可以有效降低食管癌的发病率和死亡率。近年来,机会性筛查逐渐受到重视,提高基层医疗机构的食管癌早诊率、扩大早诊早治覆盖面成为食管癌防控工作的新转变。

未来的食管癌研究将加强病因学探索,揭示发生、复发、转移机制;开发准确性高、操作简单、费用低廉的初筛技术和生物标志物;建立高危人群识别体系和风险预测模型,优化人群筛查方案;建立共享的研究平台,实现资源整合和数据共享,持续探索防控新方法新技术,推动传统预防向个体化精准预防不断发展。
注释:
1、高风险人群定义
根据《食管癌筛查与早诊早治方案(2024年版)》,高风险人群定义为年龄≥45岁,且符合以下任意一项者:
(1)居住于食管癌高发地区(以县级行政区为单位界定,以2000年中国人口结构为标准的年龄标化发病率>15/10万)。
(2)父母、子女以及兄弟姐妹等一级亲属中有食管癌病史。
(3)热烫饮食、高盐饮食、腌制食品、吸烟及重度饮酒等不良饮食习惯和生活方式。
(4)患有慢性食管炎、巴雷特(Barrett)食管、食管憩室、贲门失弛缓症、反流性食管炎、食管良性狭窄等疾病。
(5)有食管的癌前病变诊疗史。
2、高风险人群每5年进行一次内镜筛查
《中国食管癌筛查与早诊早治指南(2022,北京)》和《食管癌筛查与早诊早治方案(2024年版)》中推荐高风险人群每5年进行一次内镜筛查。随机对照试验和大型多中心队列研究均证实内镜筛查可有效降低食管癌的发病率和死亡率。Chen等基于113340例内镜筛查组、224677例未筛查组以及299483例对照人群的比较发现,内镜筛查技术作为有效的临床干预措施,可显著降低上消化道的发病率和死亡率,与对照组相比,筛查组发生食管癌的风险降低了26%(RR=0.74,95% CI:0.69~0.79),食管癌死亡风险降低了60%(RR=0.40,95% CI:0.36~0.45)。基于河南滑县的随机对照研究显示,在9年的随访中,与对照组相比,筛查组食管癌发病率、死亡率分别降低19%与18%,若排除筛查组中未应答者和筛查后未能接受及时治疗的食管恶性病变患者,内镜筛查可使晚期食管癌发病和死亡风险均显著降低30%。
3、推荐低级别上皮内瘤变者每1~3年进行1次内镜检查
《中国食管癌筛查与早诊早治指南(2022,北京)》和《食管癌筛查与早诊早治方案(2024年版)》中推荐低级别上皮内瘤变者每1~3年进行1次内镜检查。Wei等基于多中心队列研究的结果显示,食管鳞状上皮病变等级的增加与食管鳞癌发病风险呈正相关,在8.5年的中位随访期间内,1.4%的轻度异型增生患者、4.5%的中度异型增生患者以及15.5%的重度异型增生/原位癌患者发展为食管癌。基于食管癌高发区大规模筛查队列的随访研究显示,中位随访12.15年后,低级别和高级别上皮内瘤变患者进展为食管癌的风险分别是正常人群的5.00倍(HR=5.00,95% CI:4.37-5.72)和26.41倍(HR=26.41,95% CI:22.54~30.94),发生食管癌死亡的风险分别是正常人群的3.37倍(HR=3.37,95% CI:2.77~4.10)和17.85倍(HR=17.85,95%CI:14.32~22.26)。低级别上皮内瘤变患者的食管癌发病率随着随访时间延长不断升高,死亡率在随访3年后缓慢上升,随访5年后加速上升。
4、低级别上皮内瘤变合并内镜下高危因素或病变长径>1cm者每年接受1次内镜检查,持续5年
《中国食管癌筛査与早诊早治指南(2022,北京)》和《食管癌筛查与早诊早治方案(2024年版)》中推荐低级别上皮内瘤变合并内镜下高危因素或病变长径>1cm者每年接受1次内镜检查,持续5年。一项基于四川大学华西医院的研究对201例食管黏膜低级别上皮内瘤变进行随访,结果显示58.2%的病变能达到病理逆转(原病变最大径≦1cm者占60.7%);28.9%无变化;12.9%进展为高级别上皮内瘤变或癌(原病变长径>1cm者占73.1%)。
5、Barrett食管患者伴低级别上皮内瘤变,每6~12个月进行1次内镜检查;Barrett食管患者无异型增生,每3~5年进行1次内镜检查
《中国食管癌筛查与早诊早治指南(2022,北京)》和《食管癌筛查与早诊早治方案(2024年版)》中推荐对Barrett食管患者伴低级别上皮内瘤变,每6~12个月进行1次内镜检查;对Barrett食管患者无异型增生,每3~5年进行1次内镜检查。
6、食管高级别上皮内瘤变、黏膜内癌及黏膜下癌SM1应依据相应诊断进行EMR、ESD、MBM、RFA等治疗
《中国食管癌筛查与早诊早治指南(2022,北京)》和《食管癌筛查与早诊早治方案(2024年版)》中推荐对癌前病变和早期癌症进行治疗,其中对病理学显示食管鳞状上皮高级别上皮内瘤变的患者应首选内镜下切除治疗。因病灶过长、近环周等原因难以整块切除或患者不耐受内镜切除时可进行内镜下射频消融术(radiof requency ablation,RFA)治疗或其他内镜下毁损治疗。对符合内镜下切除的绝对适应证和相对适应证的早期食管癌患者,首选内镜黏膜下剥离术(endoscopic submucosal disp,ESD);病变长径≦1cm时,如能整块切除,也可考虑内镜下黏膜切除术(endoscopic mucosal rep,EMR)治疗。对局限于黏膜固有层以内的食管鳞癌可行内镜下RFA治疗。《上消化道癌筛查及早诊早治技术方案(2020年试行)》中推荐高级别上皮内瘤变和黏膜内癌采用内镜下黏膜切除术EMR、ESD、多环套扎黏膜切除术(multi-band mucosectomy,MBM)或射频消融术(radiofrequency ablation)进行治疗。EMR、ESD或MBM后,病理报告有下列情况之一者,需追加治疗(食管癌根治术/放疗/化疗):①病变黏膜下层浸润深度≥200μm;②有淋巴管/血管侵犯或静脉侵犯;③分化较差;④水平切缘和/或垂直切缘有病变累及。详见本指南诊疗部分。
7、食管SM2癌及以上病变推荐进行手术、放化疗
根据《中国食管癌筛查与早诊早治指南(2022,北京)》和《食管癌查与早诊早治方案(2024年版)》,对病变浸润深度达黏膜下层(>200μm)的T1b期食管癌患者,有淋巴结或血管侵犯,病理分级为低分化(G3),可行食管切除术,拒绝手术或手术不耐受者可同步放化疗。《上消化道癌筛查及早诊早治技术方案(2020年试行)》中对病变黏膜下层浸润深度≥200μm,建议施行食管癌根治术或放化疗。
食管癌的诊断与鉴别诊断
一、概述
大部分食管癌患者确诊时常为进展期,确切的临床分期是影响治疗决策的重要因素。目前消化内镜和组织活检及病理学检查是确诊食管癌的金标准。影像学检查对食管癌分期起重要作用。常用的影像学检查包括食管造影、内窥镜检查/内窥镜超声(EUS)、计算机断层扫描(CT)、磁共振成像-核磁共振成像(MRI)和正电子发射断层扫描(PET/CT)等:
需与食管癌鉴别最常见的疾病为食管平滑肌瘤,通常行超声内镜检查即可鉴别;食管功能性障碍疾病主要症状为反复及间断发作的吞咽困难,通过造影典型表现结合胃镜检查即可鉴别。此外食管憩室和食管良性狭窄等疾病通过患者特征性病史、胃镜以及上消化道造影检查可以鉴别。
二、诊断常用方法和应用原则
食管癌诊断和明确分期对治疗具重要意义,特别是对接受手术的食管癌患者,术前完善的检查评估至关重要。胃镜检查作为确诊食管癌首选检查,其与CT检查相整合是诊断食管癌较为理想的方法,对食管癌的定性定位诊断和手术方案的选择有重要作用。目前建议通过内镜来早期诊断、治疗和随访食管癌。食管内镜超声是评价食管癌临床T分期重要的检查手段,准确性优于CT检查,EUS引导下细针穿刺淋巴结活检可进一步提高N分期的准确率。对存在食管重度狭窄的患者,该项技术的应用具有一定局限性。此外,对早期及癌前期病变,可用色素内镜、放大内镜辅助诊断。颈、胸、腹部增强CT检查目前已作为首诊食管癌患者的常规检查,其在评价肿瘤局部生长情况、显示肿瘤外侵范围及其与邻近结构的关系和纵隔或腹腔淋巴结转移上具有优越性,但对病变局限于黏膜的早期食管癌诊断精度不高。高分辨率CT可清晰显示食管周围及腹腔淋巴结,但判断N分期的准确性仍不高。食管造影检查能够清晰、直观地展现食管癌的位置、长度以及肿瘤部位的狭窄程度,特别是对颈段食管癌,能较准确地测量肿瘤上缘与食管入口的位置,判断手术安全切缘,同时能准确发现中晚期食管癌肿瘤破溃至周围结构形成的瘘,还能在术前帮助外科医师了解食管替代器官胃的情况。超声检查可用于发现腹部重要器官及腹腔淋巴结有无转移,也用于颈深部淋巴结的检查;对疑似锁骨上淋巴结转移者,可在超声引导下穿刺以明确病变性质。近年来,MRI开始用于食管癌的术前检查,由于MRI对脂肪信号的高度敏感性,可清楚显示食管周围脂肪层是否存在,从而判断肿瘤是否存在外侵,特别是对肿瘤是否侵犯主动脉、气管及支气管等重要结构的准确性优于其他检查。同时,MRI在判断食管癌是否存在肝转移具有明显优势。PET/CT在食管癌分期中的角色不断演变,早期浅表型食管癌临床分期不推荐使用该检查,但在评价食管癌远处转移和评估新辅助治疗后及放化疗的效果方面优于CT检查。推荐有条件的医院可开展MRI和PET/CT检查。对癌变位于隆突以上的局部晚期食管癌拟手术患者,推荐行支气管镜检查以明确气管、支气管有无受侵。
三、食管癌检查流程图
食管癌患者TNM分期检查方式各具特色,根据不同T分期,N分期淋巴结部位以及M分期,将食管癌检查制作如下流程图。
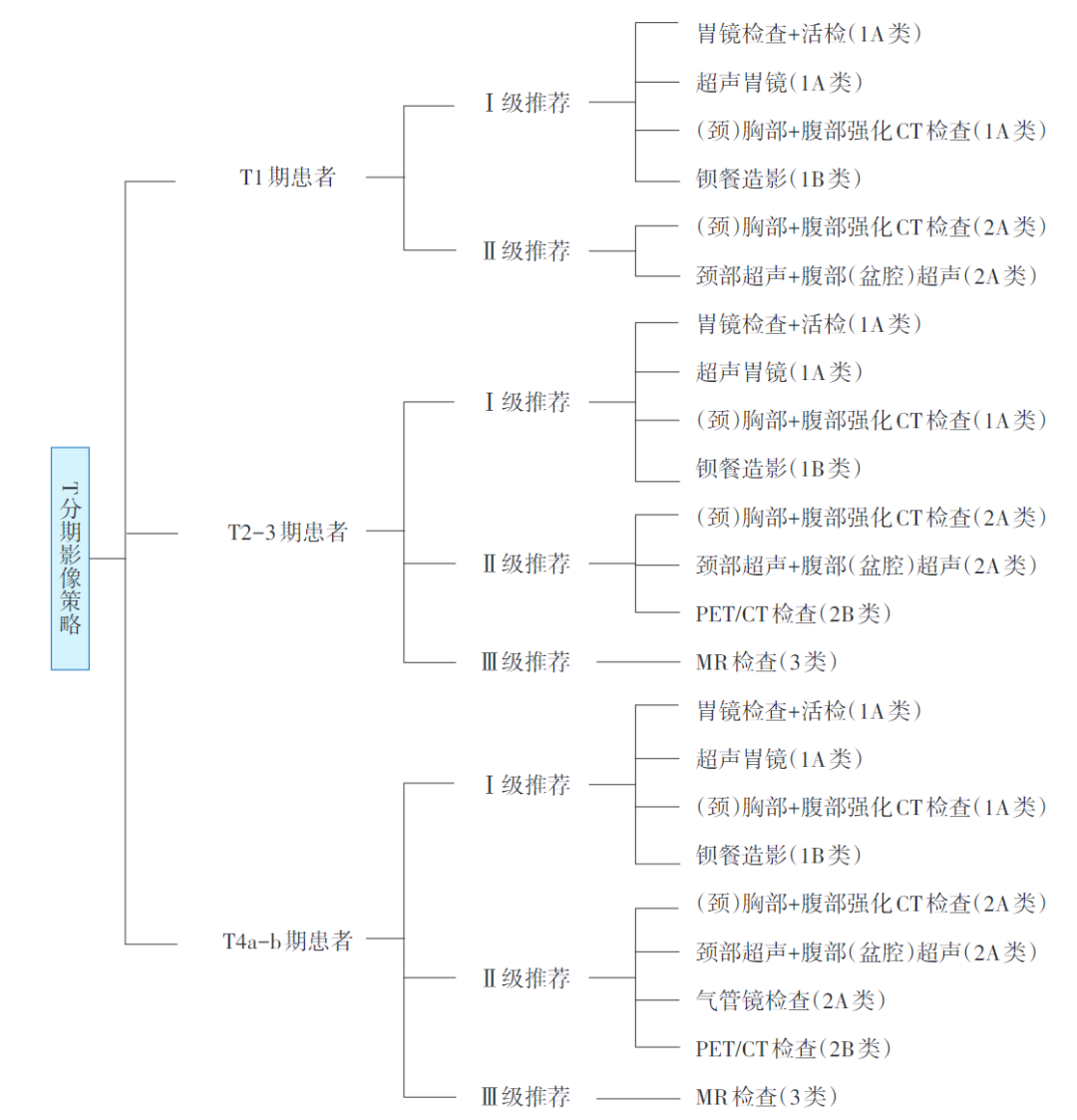
T分期影像检查策略
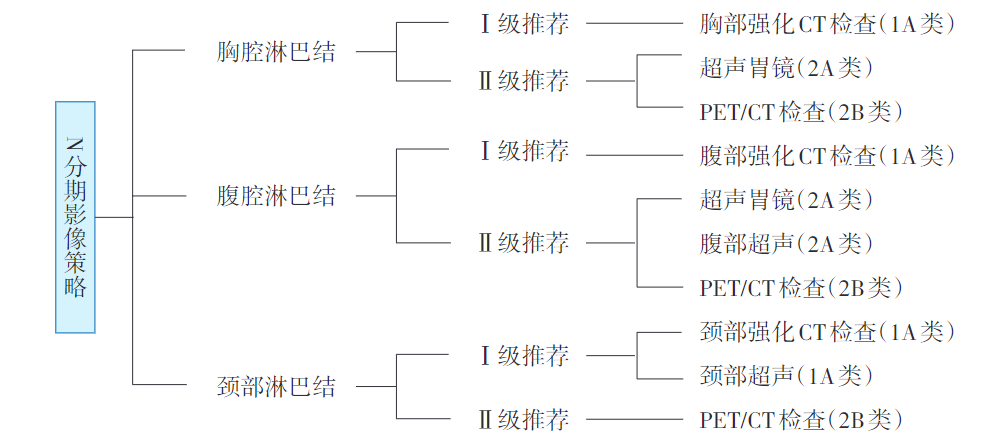
N分期影像检查策略
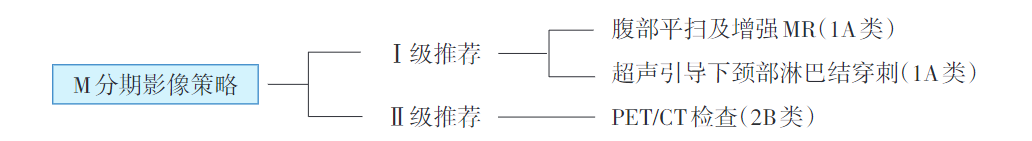
M分期影像检查策略
注释
1、T分期影像学诊断
食管癌的T分期主要由浸润深度决定。食管本无浆膜,所以无解剖屏障来阻止肿瘤局部侵犯纵隔。因此,肿瘤容易扩散到包括气管在内的颈部或胸部的相邻结构如甲状腺、喉部、支气管、主动脉、肺、心包和膈肌等。当肿瘤侵犯至纵隔内器官时,食管癌侵犯深度被定义为T4期病变,其中可切除病变被定义为T4a期,不可切除病变被定义为T4b期。首诊患者准确的临床T分期有助于明确判断局部肿瘤的纵隔侵犯程度,从而决定患者接受新辅助治疗而非直接手术。因此,术前整合影像学诊断对T分期的判断具有重要意义,通常超声内镜对T1-3期病变更有意义,而CT与MR对T4期病变的判断更具临床价值。下文将针对不同的影像学方法诊断T分期进行详细介绍。
(1)食管造影
钡餐食管造影术常作为首个检查用以评估存在吞咽困难的患者。在食管造影上,早期食管癌表现为小息肉样或片状病变或浅表扩散性病变;晚期食管癌表现为浸润性、息肉样、溃疡性或静脉曲张病变。
(2)超声胃镜(EUS)
EUS能够分辨出食管壁不同解剖层次,进而准确显示肿瘤侵袭的深度。在诊断T1期及T2期病变时具有重要意义。然而,EUS对T分期有几个局限性:一个是准确性高度依赖操作者,另一个是无法评估不可通行、狭窄肿瘤。已知的失败率为14%~25%,因为狭窄病变阻止内镜通过,应使用EUS和CT对食管癌T分期进行诊断。EUS也可用于确定区域淋巴结受累情况。同时使用细针抽吸和EUS可改善对淋巴结的评估。
(3)CT
增强CT检查目前仍是食管癌患者临床分期最佳方法,但其在局部淋巴结纵隔侵犯诊断存在局限性。EUS和PET/CT的整合使用对诊断准确性提高具有重要临床价值。对首诊食管癌患者的临床诊疗决策具有重要帮助。虽然CT无法准确区分T1至T3期病变浸润的确切深度,但对区分T3和T4期病变有重要作用,特别是在排除不可切除的(T4a)或远处转移时具有重要诊断价值。且因身体原因无法耐受强化CT的患者,仅能接受颈、胸、腹平扫CT检查。
(4)MRI与PET/CT
MRI因其具有较高的对比分辨率而在颈段食管癌的诊断中具重要意义。但其在胸段食管癌或食管胃连接部癌的诊断中因呼吸运动造成的伪影而不具备明显优势。近年来,MRI逐步开始用于食管癌的辅助诊断,特别是当局部肿物发生主动脉侵犯时,该检查有一定优势。
PET/CT常用于食管癌伴远处转移患者,但对小于5mm的肿物无明显优势。近年来一些中心将该项检查用于新辅助治疗后疗效评价的工具。同时因其高额的检查费用,应用往往受限。
(5)肿瘤周围组织侵犯诊断
1)主动脉侵犯
主动脉侵犯被定义为T4b期。通过尸检及术中探查结果显示主动脉的侵犯发生率在2%至20%不等。如果CT影像学显示肿瘤和主动脉夹角>90°或食管、主动脉和脊柱之间脂肪间隙发生闭塞均提示发生主动脉侵犯。
2)气管侵犯
气管支气管瘘和肿瘤突破气管管腔是气管支气管侵犯的明确标志。气管后壁及左主支气管压痕或牵拉亦可提示气管支气管侵犯。
2、N分期影像学诊断
精确评估N分期目前仍存在较大困难。区域淋巴结常使用EUS、CT和/或PET/CT评估转移。最常见的纵隔和腹腔干周围淋巴结转移常可通过CT和EUS评估。EUS检测转移性淋巴结优于CT。EUS只能诊断靠近食管壁的淋巴结,而对肿瘤过大EUS无法通过狭窄食管故CT诊断更具优势。
CT判断淋巴结转移与淋巴结大小具有接关系。淋巴结短轴大于1cm提示转移。CT对纵隔淋巴结转移的敏感性不高,CT的敏感性和特异性常认为在60%~80%左右和90%左右。区域淋巴结转移的确定,荟萃分析研究表明,CT的敏感性为50%,特异性为83%,PET/CT的敏感性是51%和特异性是84%。
3、M分期影像学诊断
食管癌血行转移好发部位依次为肝脏、肺、骨、肾上腺、肾脏及脑部。早期发现远处转移对食管癌治疗策略选择具有重要意义。强化CT仍是明确远处转移的首选诊断,且对肺转移的诊断具有明显优势。MRI对肝脏转移的诊断具有重要作用。PET/CT是诊断远处转移的有效工具,但因其无法分辨1cm以下的病变性质,具有一定局限性。通常拟行治疗决策重大更改时,常常推荐使用该检查。必要时推荐行全身骨扫描及脑部MRI和CT除外骨和脑转移。
食管癌病理
一、食管癌的病理分型
食管癌病理分型包括Siewert分型(适用于食管胃交界部腺癌)、大体分型和组织学分型。
1、Siewert分型
食管胃交界部腺癌是指累及解剖学上食管胃交界部的腺癌,肿瘤中心位于解剖学上食管胃交界部上、下各5cm范围内且累及食管胃交界部的腺癌适用Siewert分型。解剖学上的食管胃交界部是指管状食管变为囊状胃的部位,即食管末端和胃的起始部相交界的位置,相当于希氏角或腹膜返折水平或食管括约肌下缘,与组织学上的鳞柱交界不一定一致。Siewert分型可分为三型。
Ⅰ型:相当于远端食管腺癌,肿瘤中心位于食管胃交界部上1~5cm处。
Ⅱ型:相当于贲门腺癌,肿瘤中心位于食管胃交界部上1cm至下2cm处
Ⅲ型:相当于贲门下腺癌,肿瘤中心位于食管胃交界部下2~5cm处。
2、食管癌的大体分型
(1)早期/表浅食管癌推荐巴黎分型标准(同早期/表浅食管癌日本大体分型,即0型)
1)隆起型(0-Ⅰ)
又可分为有蒂隆起型(0-Ⅰp)和无蒂隆起型(0-Ⅰs)。
2)表浅型(0-Ⅱ)
又可分为表浅隆起型(0-Ⅱa)、表浅平坦型(0-Ⅱb)和表浅凹陷型(0-Ⅱc)。同时具有表浅隆起和表浅凹陷的病灶根据表浅隆起/表浅凹陷的比例分为表浅凹陷+表浅隆起型(0-Ⅱc+Ⅱa型)和表浅隆起+表浅凹陷型(0-Ⅱa+Ⅱc型)。
3)凹陷(溃疡)型(0-Ⅲ)
凹陷和表浅凹陷结合的病灶根据凹陷/表浅凹陷的比例分为表浅凹陷+凹陷型(0-Ⅱc+Ⅲ型)和凹陷+表浅凹陷型(0-Ⅲ+Ⅱc型)。
(2)进展期食管癌推荐国内分型
1)髓质型
以食管壁增厚为特点,边缘坡状隆起。
2)蕈伞型
肿瘤边缘隆起,唇状/蘑菇样外翻,表面可伴有浅溃疡。
3)溃疡型
少见,此类型也可见于早期/表浅癌。中央有明显溃疡,常伴边缘隆起(与Borrmann分型的2或3型对应)。
4)缩窄型
以管腔明显狭窄为特点,患者的吞咽困难症状明显。
5)腔内型
少见,此类型也可见于早期/表浅癌。病变像蘑菇样或大息肉样,有细蒂。
3、食管组织学类型(参照2019版WHO消化系统肿瘤分类)
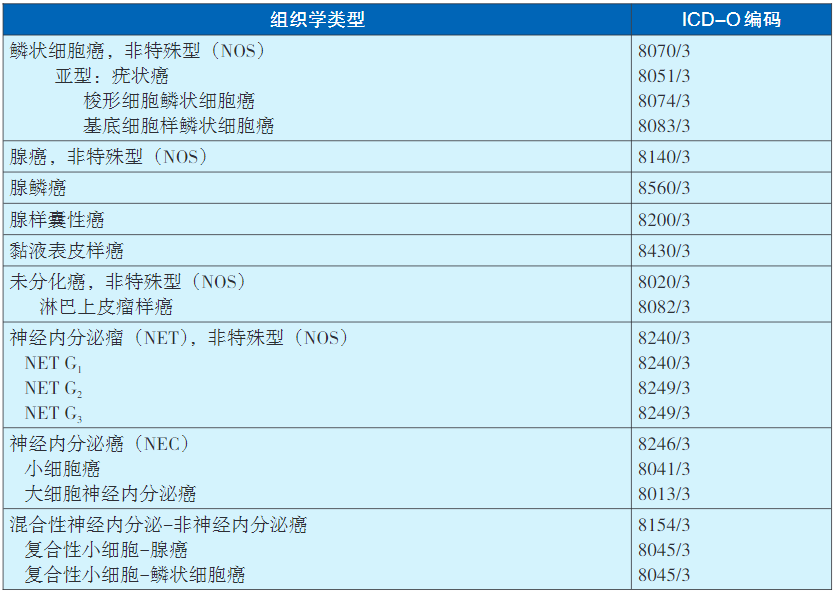
中国食管癌绝大多数是鳞状细胞癌,腺癌和腺鳞癌少见,腺样性和黏液表皮样癌罕见。鳞状细胞癌中包括三种特殊亚型,其中基底细胞样鳞状细胞癌相对多见,梭形细胞鳞状细胞癌少见,疣状癌罕见。神经内分泌瘤中,小细胞癌常见,大细胞神经内分泌癌少见,神经内分泌瘤(NET)罕见。不同组织学类型/亚型的食管癌预后不同,比如食管小细胞癌比鳞状细胞癌预后差;不同组织学类型/亚型的食管癌针对不同治疗的敏感性也不同。
除上皮性肿瘤外,食管还可发生恶性黑色素瘤、平滑肌瘤、胃肠道间质瘤、淋巴瘤等肿瘤,需注意鉴别诊断。
二、新辅助治疗后病理学评估
新辅助治疗病理反应的程度与预后密切相关。建议按照CAP(College of American Pathologists)/NCCN(The National Comprehen-sive Cancer Network)指南的新辅助治疗后病理学评估标准进行评估。
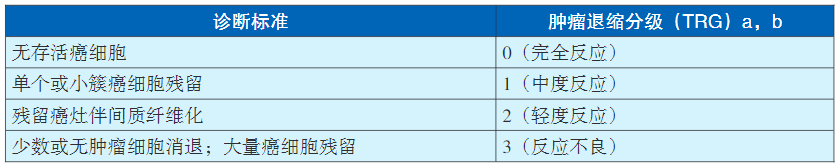
此肿瘤退缩分级只用来评估原发肿瘤。可参考Mandard、Becker、日本食管疾病学会病理学评估标准进行评估。建议同时报告残存瘤细胞比例。目前淋巴结的退缩评估尚无统一标准,建议按以下四种情况报告:
-
淋巴结有治疗反应但无残存肿瘤,淋巴结所在分组及个数;
-
淋巴结有治疗反应且有残存肿瘤,淋巴结所在分组及个数;
-
淋巴结有转移癌但无治疗反应,淋巴结所在分组及个数;
-
淋巴结无转移癌也无治疗反应
疗效评估根据存活瘤细胞决定,经过新辅助治疗后出现的无瘤细胞的角化物或黏液湖不能认为是肿瘤残留;淋巴结内出现无瘤细胞的角化物或黏液湖不能认为是肿瘤转移。
三、病理报告质控要求
合格的术后病理报告至少需要(但不限于)完整记录以下内容:肿瘤组织学类型/亚型、分化程度、肿瘤最大径、浸润深度、侵犯范围(侵犯其他组织或器官)、高危因素(如脉管瘤栓、神经侵犯等)、淋巴结清扫个数及转移个数、切缘情况(上下切缘及环周切缘)以及其他病理所见;新辅助治疗病例需报告此肿瘤退缩分级。必要时包括免疫组化和特殊染色检测内容。
参考文献及书籍:
1.《2025 中国肿瘤整合诊治指南(CACA)——食管癌》
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)