首页 > 医疗资讯/ 正文
病史
患者,男,71岁,“反复粘液血便3月,加重1月余”
肠镜检查
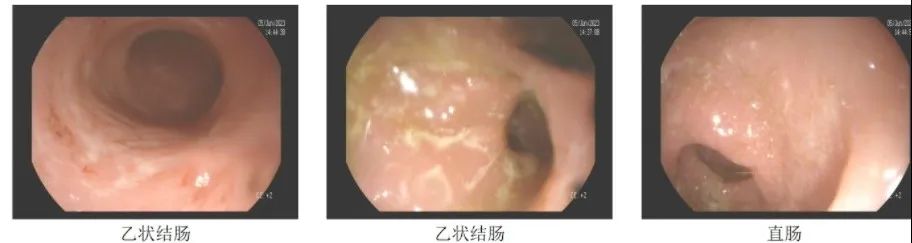
内镜所见:
进镜至乙降交界,患者无法耐受,同患者及家属商议后终止检査:距肛门30cm以下乙状结肠、直肠粘膜连续充血糜烂,血管纹理消失,接触出血明显,活检。
内镜检查诊断:
溃疡性结肠炎(mayo 2分)
镜下所见:
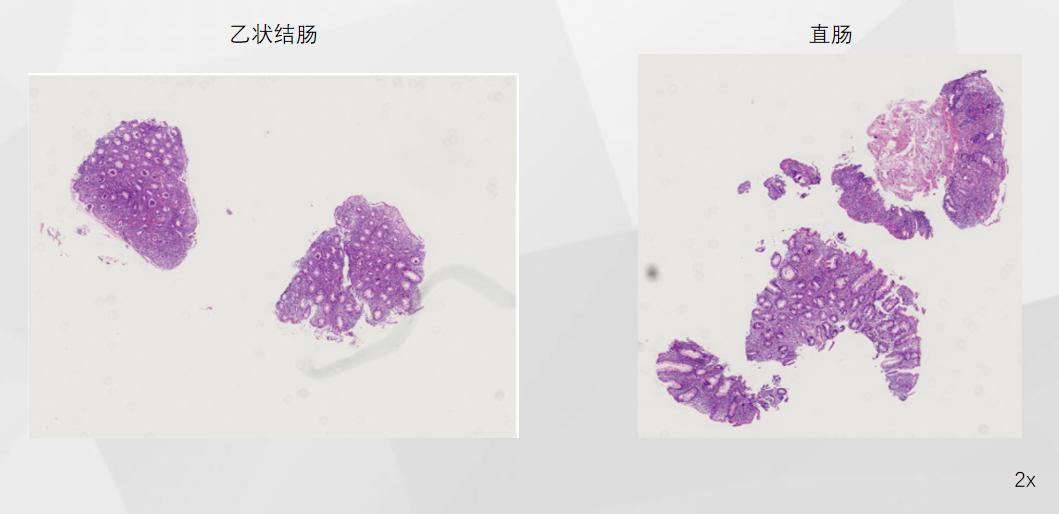
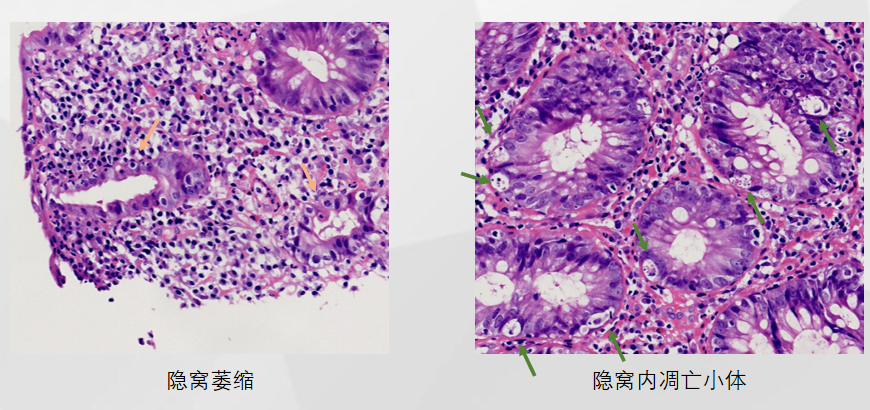
低倍镜下可见隐窝扭曲不规则,较弥漫的淋巴、浆细胞浸润。第一印象为慢性肠炎改变。
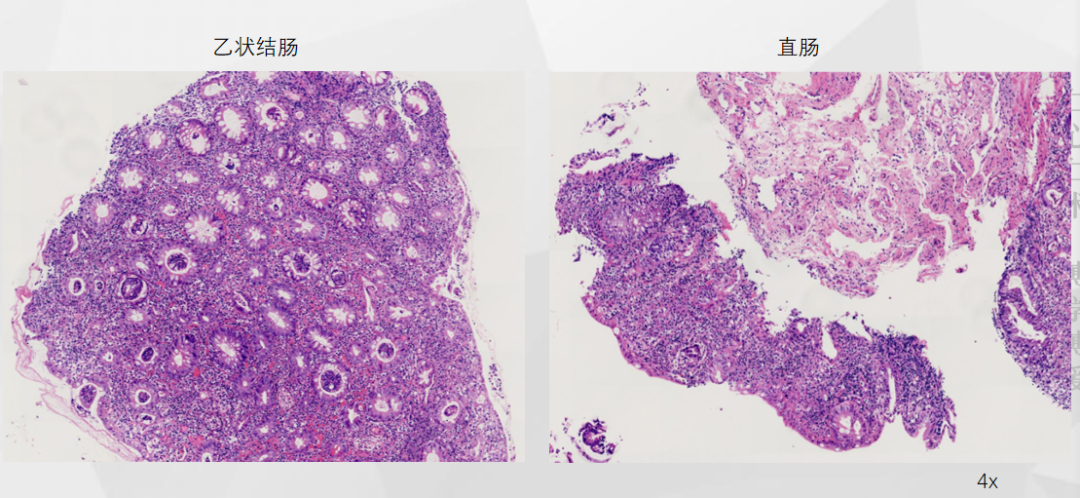
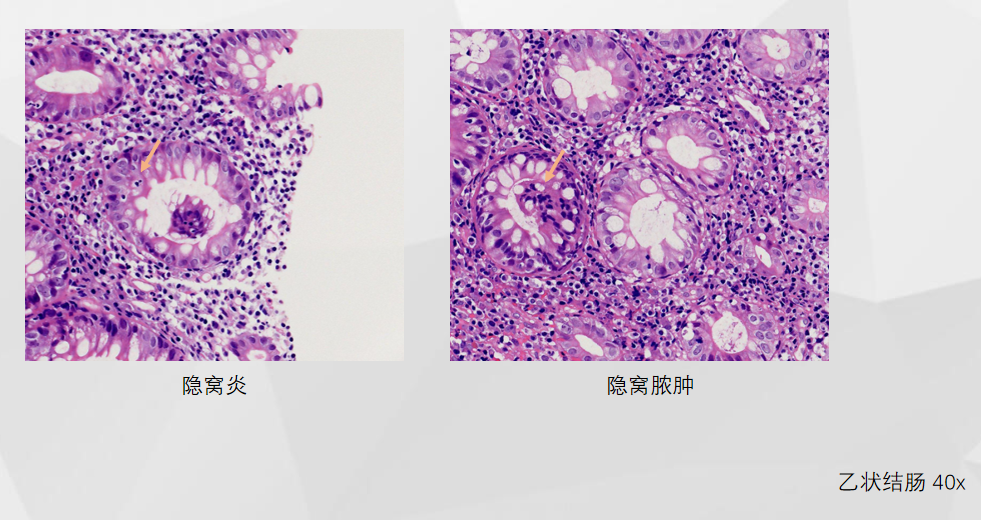
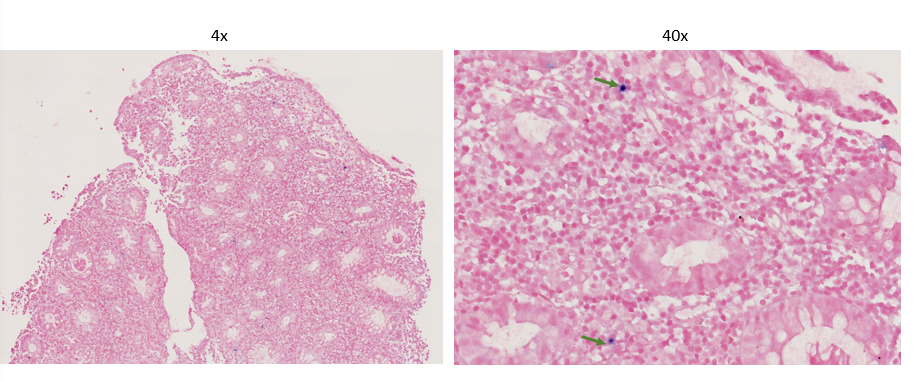
EBER-ISH 全片仅见2个阳性细胞
本例结肠活检形态学小结:
1、活动性炎明显,部分隐窝萎缩、凋零伴隐窝脓肿,考虑合并毒性/缺血性损伤;
2、慢性炎明显,基底部淋巴浆细胞增多,伴有隐窝结构改变;
3、部分隐窝上皮内凋亡小体明显增多。
病理诊断:
活检形态学需考虑感染性肠炎,炎症性肠病(溃疡性结肠炎)等,但是患者年龄偏大,而且凋亡小体明显增多如何解释?还要有哪些鉴别诊断?
幸运的是,我们有优秀的临床团队支撑。当日做内镜的消化内科医生打电话来,补充病史,患者为肺癌患者,在使用PD-1抑制剂治疗,临床考虑为免疫检查点抑制剂相关性肠炎Immune checkpoint inhibitor-associated colitis(ICIC)。结合相关病史及形态学改变,本例诊断为(ICIC);须鉴别于①感染性肠炎;②早期溃疡性结肠炎。
非肿瘤性疾病的病理诊断,需要通过多种不特异的表现排列组合,结合临床信息,最后分析最大可能性的诊断,但这也是非肿瘤性病变有魅力的一个方面。
文献复习及讨论:
过去十年间,免疫检查点抑制剂(ICIs)已发展为晚期恶性肿瘤的一线疗法,显著改善了包括延长生存期在内的多种癌症治疗结局。
目前,靶向 PD-1(程序性死亡受体1) 或其配体 PD-L1 的单克隆抗体是优先选择的免疫治疗方案。尽管检查点阻断抗体能增强肿瘤控制,但也可能引发自身免疫病理反应(常称为“免疫相关不良事件”,irAEs),最常累及皮肤、胃肠道、肝脏、内分泌器官和肺。
有文献对9例接受抗PD-1治疗并出现腹泻患者的结肠活检组织进行分析。共识别出四种主要组织学模式,其发生率大致相同:①溃疡性结肠炎(UC)样(n=2)、②移植物抗宿主病(GVHD)样(n=2)、③胶原性结肠炎样(n=3),④结合显微镜下结肠炎与UC样特征的混合型结肠炎(n=2)。无论何种亚型,均普遍存在上皮下胶原带增厚、表面上皮剥脱及隐窝上皮细胞凋亡增加等特征。
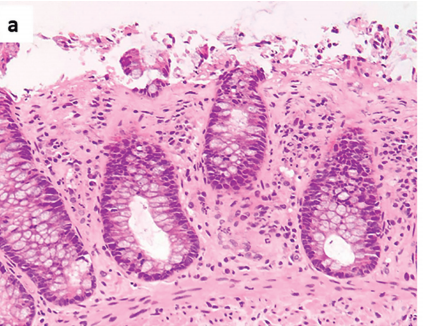
图a:胶原性结肠炎样结肠炎;
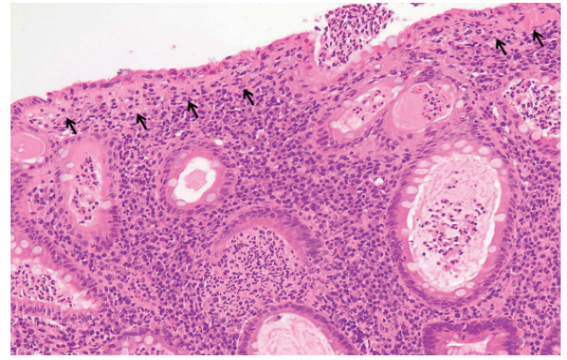
图b:溃疡性结肠炎样结肠炎表现;
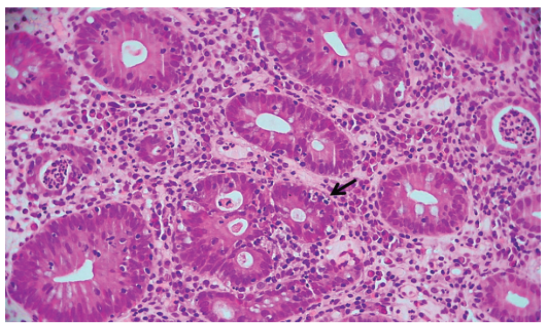
图c:混合型结肠炎模式;
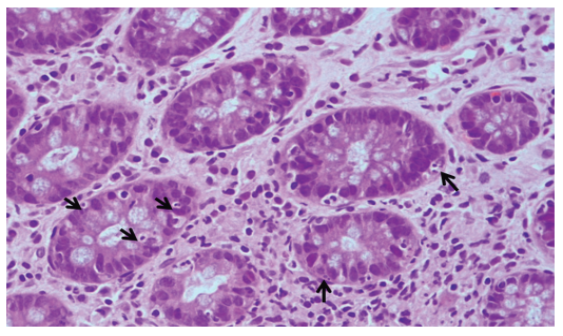
图d:移植物抗宿主病样结肠炎;
(以上图片源自参考文献1)。
另一篇文献描述了8例接受抗PD-1单药治疗期间发生结肠炎患者的组织病理学表现。最常见的损伤模式(5/8病例)表现为活动性结肠炎伴中性粒细胞性隐窝微脓肿,同时存在显著的隐窝上皮细胞凋亡及隐窝萎缩/丢失。这些特征与以凋亡为主的其他结肠炎(如急性移植物抗宿主病或特定药物性结肠炎)相似。其余病例(3/8)呈现淋巴细胞性结肠炎样模式,以上皮内淋巴细胞增多和表面上皮损伤为特征。此类病例中凋亡现象亦常见,但无隐窝萎缩/丢失。此外该文献还描述了复发性抗PD-1结肠炎。其组织学特征与初次损伤相似,但出现慢性化改变(如基底淋巴细胞浆细胞浸润、隐窝结构紊乱及1例潘氏细胞化生),此时与炎症性肠病更难区分。结合临床背景,病理学家仍可提示抗PD-1结肠炎的诊断。
心得体会:
在肿瘤性疾病领域,恶性黑色素瘤(恶黑)因其形态学模仿能力,被称为“tumor mimics”;而在非肿瘤性病变范畴中,个人认为药物性损伤恰似“非肿瘤界的恶黑”,其镜下表现具有极强的迷惑性,可模拟各类非肿瘤性病变的形态特征。这类复杂病例的鉴别诊断,既需要详细追溯用药史、病史等临床线索,更依赖多学科团队(MDT)的密切协作。具体到形态学观察,除了关注活动性炎症、慢性炎等改变外,若发现显著的隐窝凋亡或毒性缺血损伤模式,要想到药物性损伤的可能。
致谢:
在此过程中,诊断的顺利推进得益于北京大学深圳医院多学科伙伴的专业支持:特别感谢病理科陶丽丽医生在MDT讨论中提出的宝贵见解,以及在病例撰写过程中给予的悉心指导与专业建议。感谢病理诊断医生陈翠敏凭借深厚的诊断功底,在复杂形态学特征中抽丝剥茧;同时致谢消化内科医生荀安营在病史采集、内镜评估环节的高效协作,其提供的用药史与临床特征,为病理鉴别诊断搭建了重要参考。
参考文献:
1、Stratigoula Sakellariou, Evgenia Papathanasiou, Marina Perdiki, et al. Histological diversity of anti-PD1-induced colitis[J]. Histology and histopathology, 2022, 37(7): 699-708. DOI: 10.14670/HH-18-456.
2、Jonathan H Chen, Maryam K Pezhouh, Gregory Y Lauwers, et al. Histopathologic Features of Colitis Due to Immunotherapy With Anti-PD-1 Antibodies[J]. The American journal of surgical pathology, 2017, 41(5): 643-654. DOI: 10.1097/PAS.0000000000000829.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)