首页 > 医疗资讯/ 正文
2019年,法国巴黎Gustave Roussy医院的一张CT影像对比图在肿瘤学界引发轰动:一位历经化疗、免疫治疗均告失败的晚期非小细胞肺癌患者,在入组德曲妥珠单抗(T-DXd)临床试验后,全身转移病灶仅2个月便显著缩小。这张影像让临床医生看到了肺癌精准治疗的全新可能。
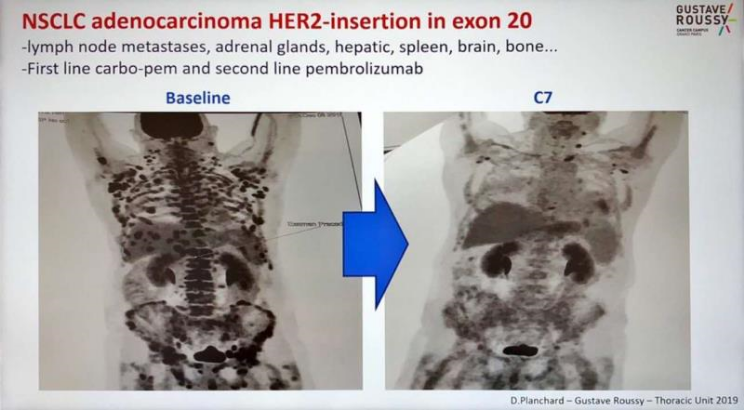
病例来源:https://twitter.com/dplanchard/status/1266701523809165313
三个关键词,快速了解ADC药物
ADC的全称是抗体-药物偶联物(antibody-drug conjugate),是一类由连接子将抗体和细胞毒性药物(有效载荷)组合在一起的靶向生物药剂。ADC的每个组成部分都发挥着不同的功能:1-2
精准靶向:抗体部分是ADC药物的主体框架结构和导航系统,负责将ADC分子选择性地递送至肿瘤细胞表面,同时通过靶点介导的内吞作用进入到细胞内;
安全传递:连接子负责在肿瘤细胞内或者表面高效释放毒素小分子,其化学性质决定了毒素小分子如何及何时释放出来。连接子的稳定性决定了ADC药物中的毒素小分子是传递到肿瘤细胞内部,还是有可能在运输过程中过早释放并跟随血浆传递到其他组织而产生毒性。连接子的稳定性显著影响ADC药物的安全性和有效性。
高效杀伤:细胞毒性药物是 ADC 内化到癌细胞后发挥细胞毒性、摧毁癌细胞的弹头,可实现对癌细胞的高效清除。
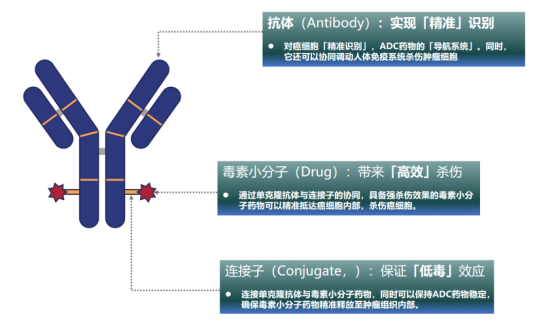
ADC药物结构示意图
精准靶向肺癌,ADC药物的治疗革命
虽然全身化疗、靶向治疗和免疫疗法可以治疗晚期肺癌,但许多患者最终会出现疾病进展。现在,ADC这一新兴的靶向治疗方法,通过将细胞毒性药物直接递送到癌细胞,最大限度地减少脱靶效应,为肺癌提供了一个有希望的新治疗选择(Tawfiq RK 2025)。2
ADC药物的治疗优势主要表现在:3
l ADC药物单靶点特异性结合使脱靶毒性显著降低,治疗窗口大幅拓宽;
l 细胞毒素在肿瘤局部的高浓度释放,既增强了杀伤效力,又避免了全身暴露带来的副作用;
l 当某些ADC药物释放的有效载荷具有渗透性或跨膜性时,还可能诱发旁观者效应,从而增强ADC的疗效。此外,这些药物的旁观者效应也可能改变肿瘤微环境,从而进一步增强ADC的杀伤作用。
*旁观者效应:ADC 的旁观者效应是指某些 ADC药物能够将有效载荷从抗原阳性肿瘤细胞扩散到邻近的抗原阴性肿瘤细胞,从而增强抗肿瘤活性。这种效应使得 ADC 即使在靶抗原表达不均匀的肿瘤中也能发挥作用,因为有效载荷可以从结合了 ADC 的抗原阳性细胞扩散到邻近的抗原阴性细胞,进而杀死它们。4
成功的ADC药物开发依赖于选择正确的抗原靶点和设计精确的抗体,理想的靶点是在癌细胞上高度表达,而在正常细胞中的表达水平较低。目前非小细胞肺癌(NSCLC)的热门靶点主要包括HER2、TROP2、c-MET和EGFR等,HER2的低内化和降解率使其成为非小细胞肺癌的主要ADC靶点(Tawfiq RK 2025)。2
德曲妥珠单抗是全球首个肺癌领域靶向HER2的ADC药物。5该药物采用高活性载药系统与可裂解连接子技术,将人源化 HER2 单克隆抗体与毒素小分子(DXd)结合,具备精准靶向和高效低毒的双重优势。通过采用半胱氨酸偶联,药物抗体比(DAR)达到理论上最高值 8:1。相比早期研发的 ADC,德曲妥珠单抗在血液循环中具有高度稳定性,直到被癌细胞中过表达的肽内化并选择性裂解,从而释放出强效的有效载荷来诱导 DNA 损伤和细胞凋亡,并可对邻近的肿瘤细胞产生“旁观者”杀伤作用。6
除了德曲妥珠单抗外,更多针对肺癌的ADC药物正在迎来突破,或在不久的将来为患者提供更加有效的治疗选择。
挑战犹存,未来可期——ADC药物在肺癌领域的发展方向
ADC药物的未来正沿着一条清晰的发展轨迹演进,但现存的挑战亟待解决。如肿瘤抗原表达异质性,这可能导致不一致的反应和治疗结果。其他的重要挑战还包括不良反应和治疗耐药性等。2因此ADC药物在肺癌领域的发展方向主要集中在以下几个方面:
开发新的靶点:在ADC药物的靶点选择方面,除了肿瘤细胞表面靶点外,肿瘤微环境的靶点是该领域的新热点之一。此类靶点,因其分布在肿瘤组织周围,比肿瘤组织更容易从血液循环接触到ADC分子。除了更强的抗肿瘤效果外,产生耐药性的可能性也可降低。1
从单药突破走向联合增效:为提高疗效并延缓耐药性,可考虑将ADC与其他药物联合使用。
如将ADC与免疫治疗或靶向治疗相结合,则有可能实现协同或附加效应,从而提高治疗效果。例如,ADC诱导的免疫原性细胞死亡可以刺激抗肿瘤免疫反应,免疫检查点抑制剂可能进一步放大这种免疫反应等。2
提升细胞毒性药物技术:ADC的药效与其连接的细胞毒性分子数量密切相关,连接的细胞毒性分子数量越多,疗效可能越好,但也增加了毒性风险;连接的细胞毒性分子数量越少,疗效可能不足。因此,精准选择细胞毒性分子数量是一个技术难点。另外,选择合适的细胞毒性药物也至关重要,既要考虑药物的杀伤能力,又要平衡其毒性和疗效。1
结语
ADC药物作为精准医疗的杰出代表,正在重塑肺癌治疗格局。从"三体"结构的精巧设计,到临床实战的斐然战绩,再到未来趋势的多元探索,ADC药物不仅突破了传统治疗的疗效瓶颈,更开辟了肺癌精准医疗的新纪元。随着技术迭代与策略创新,ADC药物有望从单药走向联合,从后线迈向全程,为肺癌患者带来更长生存、更高生活质量的希望,照亮人类攻克癌症的征途。
参考文献
1、刘文超等.抗体偶联药物的技术现状和展望.生物化学与生物物理进展.2023;50(5):1167-1189.
2、Tawfiq RK et al.Targeting Lung Cancer with Precision: The ADC Therapeutic Revolution.Current Oncology Reports.https://doi.org/10.1007/s11912-025-01655-5
3、Fu ZW et al.Antibody drug conjugate: the “biological missile” for targeted cancer therapy.Signal Transduction and Targeted Therapy 2022; 7:93.
4、Staudacher AH et al.Antibody drug conjugates and bystander killing: is antigen-dependent internalisation required?British Journal of Cancer /2017; 117:1736–1742.
5、Mehta GU et al.FDA approval summary: fam-trastuzumab deruxtecan-nxkifor unresectable or metastatic non-small cell lung cancer with activating HER2 mutations.The Oncologist, 2024, 29, 667–671.
6、Li BT et al. Trastuzumab Deruxtecan in HER2-Mutant Non-Small-Cell Lung Cancer. N Engl J Med. 2022 Jan 20;386(3):241-251.
审批编码:CN-20250606-00008
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)