首页 > 医疗资讯/ 正文
在动脉粥样硬化的晚期,脆弱斑块的破裂和血栓形成成为急性心血管事件和死亡的主要诱因。牙周炎相关牙龈卟啉单胞菌(Pg)等致病性感染已被怀疑会增加动脉粥样硬化性心血管疾病的风险,但其与动脉粥样硬化斑块不稳定的关系仍然难以捉摸。2025 年 5 月 23 日,华中科技大学同济医学院陈莉莉、南方科技大学王松灵、北京大学口腔医院邓旭亮、武汉协和医院董念国共同通讯在Signal Transduction and Targeted Therapy上在线发表题为“Porphyromonas gingivalis aggravates atherosclerotic plaque instability by promoting lipid-laden macrophage necroptosis”的研究论文。在人类临床样本中,Pg阳性簇的水平与动脉粥样硬化斑块坏死核心区与总斑块面积的比值呈正相关,表明斑块不稳定。
在家兔和Apoe- / -小鼠中,Pg通过触发氧化应激导致巨噬细胞程序性坏死,促进斑块坏死,加重斑块不稳定性。这一过程伴随着巨噬细胞中叉头框O3 (FOXO3)蛋白水平的降低。机制分析表明,Pg脂多糖(LPS)通过TLR4信号通路诱发巨噬细胞氧化应激,进而激活MAPK/ ERK介导的FOXO3磷酸化和降解。而牙龈蛋白酶是Pg产生的一类蛋白酶,能有效水解巨噬细胞胞浆中的FOXO3。二者均可降低FOXO3的核内水平,继而从巨噬细胞清除率受体1(Msr1)启动子释放组蛋白去乙酰化酶2 (HDAC2),从而促进Msr1转录。 MSR1介导的脂质摄取增强进一步放大了氧化应激诱导的脂质巨噬细胞程序性坏死。综上所述,Pg可加重巨噬细胞氧化应激依赖性程序性坏死,从而扩大动脉粥样硬化斑块的坏死核心,最终促进斑块不稳定。

动脉粥样硬化性心血管疾病(ASCVD)占全球心血管疾病病例死亡人数的1/3。动脉粥样硬化是一种由脂质代谢功能障碍引发的血管慢性炎症性疾病,最终可发展为临床上明显的ASCVD。在动脉粥样硬化的晚期,动脉斑块逐渐从稳定发展到不稳定,最终导致斑块破裂、脱离、斑块内出血(IPH)和血栓形成。由于血栓形成潜力高,它们可能带来更大的临床风险。据报道,这些不稳定的斑块是导致许多主要不良心血管事件的主要病因。动脉粥样硬化斑块不稳定代表慢性和多因素病理进展。早期斑块由氧化低密度脂蛋白(ox-LDL)的内皮下沉积引发,并在持续的脂质积累、慢性炎症和细胞外基质重塑下进一步扩大,导致动脉壁增厚和随后的临床缺血性心脏病。在持续的病理生理刺激下,晚期斑块发生结构和成分改变。这些现象共同使动脉粥样硬化斑块不稳定。虽然驱动动脉粥样硬化斑块在动脉壁内形成和生长的基本机制已被广泛表征,但从良性稳定病变转变为不稳定、易破裂斑块的病理过程仍然知之甚少。
脂质和炎症被认为是加剧动脉粥样硬化斑块不稳定的典型和主要驱动因素,但重要的促成因素仍在被发现。人们认为慢性传染病(包括牙周病)会促进ASCVD的发展。牙周炎已被证实与冠心病(MI)风险升高显著相关。牙龈卟啉单胞菌(Pg)是导致慢性牙周病病因的主要致病菌,据报道在流行病学和机制上与动脉粥样硬化的发展有关。此外,Pg及其血浆抗体水平与患者腹主动脉瘤直径和血栓体积呈显著相关性。Pg可以在MI小鼠模型中定植缺血心肌组织,促进心脏破裂,从而增加死亡率。这一证据强调了Pg在动脉粥样硬化斑块不稳定中可能起的作用。然而,仍然缺乏关于Pg感染与斑块不稳定之间关联的表型和机制研究。
坏死核心的形成和扩展是斑块脆弱性的核心决定因素。斑块内坏死核心主要由胆固醇晶体、脂质和细胞碎片组成,但缺乏胶原蛋白基质。结构脆弱的位点容易破裂、IPH和血栓形成。研究结果表明,在人动脉粥样硬化晚期,大部分巨噬细胞和血管平滑肌细胞表现出坏死的超微结构特征。经验证,细胞焦亡、铁死亡和坏死性凋亡等常见的调节性坏死方式在动脉粥样硬化进展和斑块不稳定过程中被不同地激活与凋亡不同,坏死细胞释放具有免疫刺激性的细胞内成分,启动无菌性炎症级联反应,从而加剧旁观者细胞死亡。这些发现强调了坏死是导致坏死核心扩张和斑块易损性的主要因素。研究表明,Pg可诱导巨噬细胞凋亡、坏死性凋亡和细胞焦亡以及VSMC凋亡,但其在坏死核心扩大中的作用及其潜在的分子机制尚不清楚。
在本研究发现富含高水平Pg的人动脉粥样硬化斑块更不稳定,结合对兔和小鼠的研究,证明Pg感染通过促进氧化应激介导的脂质巨噬细胞坏死性凋亡,加重了以斑块坏死增加为特征的病变不稳定。这种氧化应激不仅源于Pg的刺激,而且主要是由巨噬细胞清道夫受体1 (MSR1)介导的脂质摄取增强而放大。在机制上,Pg衍生的毒力因子脂多糖(LPS)和牙龈蛋白酶通过破坏叉头框O3 (FOXO3)-组蛋白去乙酰化酶2 (HDAC2)介导的对MSR1的转录抑制,从而上调MSR1的表达,从而促进后续级联反应导致程序性坏死。总之,研究结果表明,牙周致病菌感染与动脉粥样硬化斑块不稳定之间存在因果关系,并可能为ASCVDs的疾病预防和临床管理提供新的治疗策略。
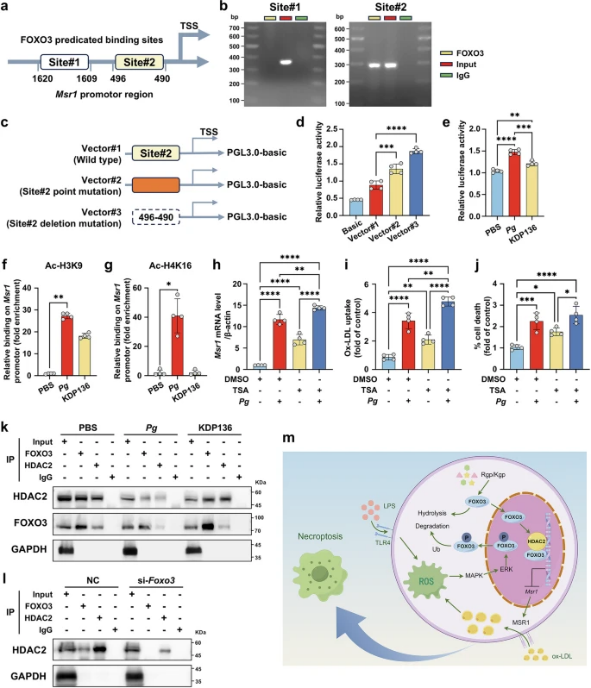
图1 HDAC2被FOXO3募集到启动子中并抑制MSR1转录(摘自Signal Transduction and Targeted Therapy)
参考消息:https://doi.org/10.1038/s41392-025-02251-6
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)