首页 > 医疗资讯/ 正文
阿尔茨海默病 (Alzheimer's Disease,AD) 是最常见的痴呆形式,其病理特征包括细胞外淀粉样蛋白-β (amyloid‐beta,Aβ) 沉积形成斑块和脑实质中的神经原纤维缠结脑血管异常在 AD 进展的早期表现出来,并与加速脑萎缩和认知能力下降有关。值得注意的是,神经影像学研究表明,AD 患者通常表现出各种形式的小血管疾病,例如白质高信号 (white matter hyperintensities ,WMH)、血管周围间隙扩大和微出血。此外,AD 患者的血脑屏障 (blood‐brain barrier,BBB) 的结构和功能受损,表现为血小板衍生生长因子受体β(platelet‐derived growth factor receptor β,PDGFRβ)水平升高或脑脊液 (cerebrospinal fluid,CSF) 白蛋白与血清白蛋白的比率(Qalb)增加。
越来越多的证据表明异常血管生成的发生,其特征是 AD 患者死后脑中血管生成因子(vascular endothelial growth factor ,VEGF)水平升高和小血管密度升高。对 AD 患者尸检大脑的单个核 RNA 测序的分析证实,AD 大脑中的内皮细胞表现出促血管生成表型。成人大脑中异常的血管生成可导致过度无功能的小血管形成和内皮壁完整性、周细胞覆盖和基底膜功能的损害。这种现象被认为是在各种神经系统疾病中观察到的 BBB 功能障碍的一个促成因素。然而,AD 患者异常血管生成和淀粉样蛋白与 tau 病理之间的关系,以及它在脑血管病理中的作用仍不清楚。所以分析血管生成因子与脑血管病变、神经退行性和认知功能之间的关系有重要的意义。
1月8日,中国科学技术大学第一附属医院神经内科申勇团队在Alzheimers Dement(IF=13.1)在线发表了题为“Pathological angiogenesis was associated with cerebrovascular lesion and neurodegeneration in Alzheimer's disease”的研究,结果提示tau 病理学可能在病理性血管生成中起关键作用,导致 AD 的脑血管病变和神经变性。

本研究调查了死后人类 AD 大脑和临床 AD 队列中病理性血管生成与脑血管损伤和神经变性之间的关系。评估了死后人脑的脑血管病变、Aβ和 tau 病变,并检测了中国老龄化和神经退行性疾病倡议 (China Aging and Neurodegenerative Disease Initiative ,CANDI) 队列中的CSF中的 12 种血管生成因子。研究结果如下:
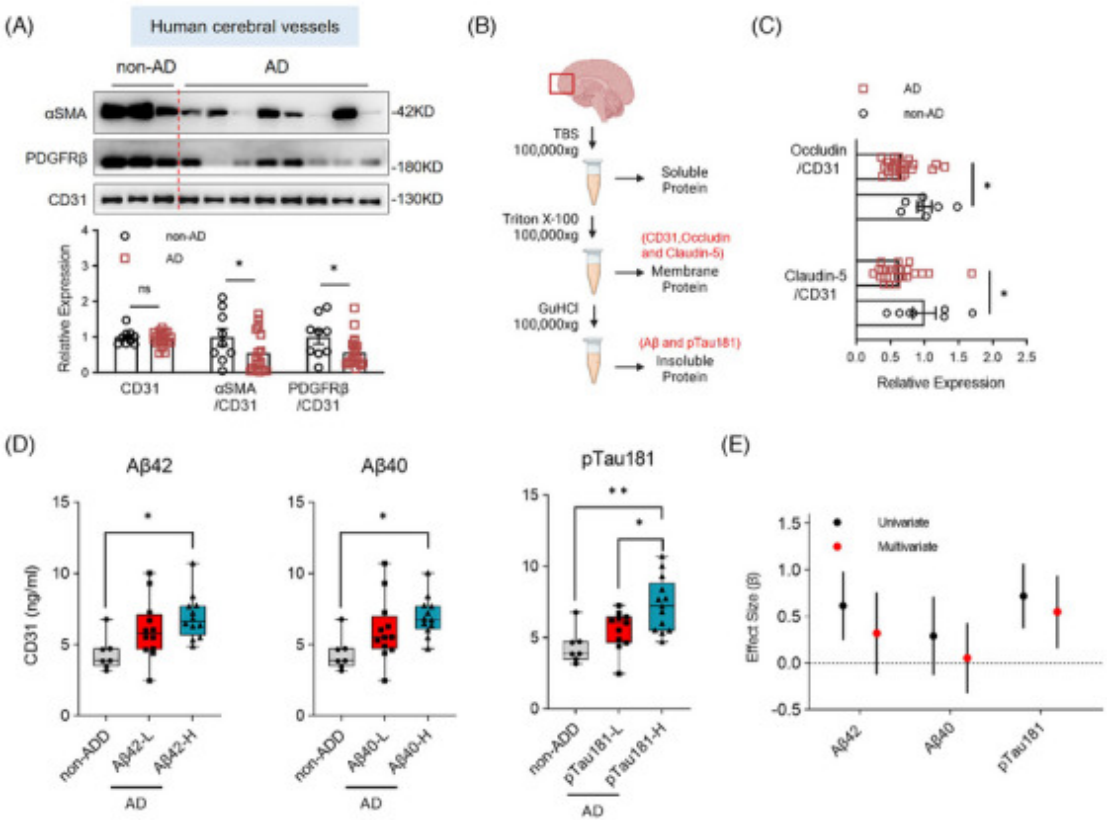
图1.与人类 AD 大脑中的 tau 病理相关的脑血管病变和 CD31 水平升高
升高的血管标志物 CD31 与人脑中的 tau 病理和 BBB 损伤表现出更强的相关性。同时在 CANDI 队列中,较高水平的 CSF 血管生成因子也显示出与 CSF pTau181 的更强相关性。此外,发现异常的血管生成生物标志物与脑萎缩和认知能力下降有关。值得注意的是,只有与 VEGF 通路(CSF sVEGFR1、sVEGFR2、VEGF-C 和 PLGF)和血管生成素-TIE 通路(CSF sTIE2)相关的血管生成因子与 AD 生物标志物(CSF Aβ42/40 或 pTau181)和血管损伤相关,表明它们在 AD 的致病性血管生成中起主要作用。这些结果共同表明,受 tau 病理影响的异常 CSF 血管生成因子在脑血管损伤中起重要作用,并有助于AD的发生。
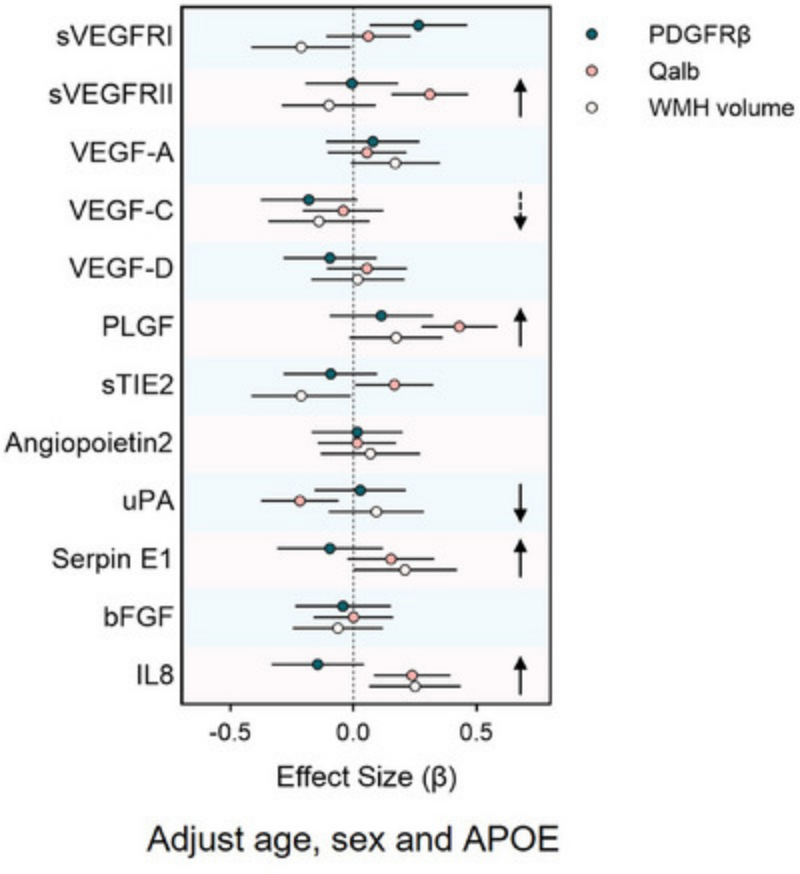
图2.血管生成生物标志物与脑血管损伤生物标志物之间的关联
生理性血管生成通常在在成人大脑中几乎处于静止状态。然而,阿尔茨海默病可以重新激活病理性血管生成,其确切机制尚不清楚。在本研究中,多变量分析表明,不溶性pTau181,而不是Aβ42或Aβ40,在AD脑中与CD31表现出主要关系。此外,来自临床AD队列的数据显示,CSF血管生成生物标志物sVEGFR1、sTIE2、VEGF‐C、VEGF‐D、血管生成素2、bFGF和Serpin E1水平升高与CSF pTau181相关,而只有CSF sVEGFR1、sTIE2和bFGF与CSF Aβ42/40呈正相关。同时,中介分析显示CSF Aβ42/40、CSF sVEGFR1和sTIE2之间的关系主要由CSF pTau181介导。因此,tau病理似乎是脑脊液血管生成因子水平升高的主要原因。然而,作为AD中最早的驱动因子,Aβ31触发下游tau病理,并可能在AD中观察到的异常血管生成中起关键作用。
这项研究的一个有趣发现是较高水平的 sVEGFR1 与较低的 WMH 以及恶化的周细胞损伤(用 CSF PDGFRβ水平测量)之间的关联。一种可能的解释是 sVEGFR1 可以通过捕获VEGF因子来阻碍异常血管生成,从而减轻 WMH 的发生。
病理性血管生成可诱发毛细血管的形态和功能异常,包括螺旋形态、血管直径减小和血流受损。AD大脑中升高的细血管被认为是功能失调的毛细血管。本研究提出 AD大脑中异常的新血管是功能丧失的血管,随着疾病的进展可能会演变成功能失调的细血管。异常血管生成介导的脑血管病变可能进一步促进神经退行性和认知障碍。本研究观察到 sVEGFR1、PLGF 和 IL8 与基线时较低的皮质厚度或较高的血清 NFL 水平相关。较高水平的 sTIE2 和血管生成素 2 也与脑萎缩、MMSE 评分下降或血清 NFL 升高有关,这可能是由于血管生成素 2 升高拮抗作用损害血管生成素 1-TIE2 通路以加剧血管通透性。此外,研究还观察到促血管生成因子 VEGF-A 和 uPA 与皮质厚度呈正相关。因此,这些血管生成因子在脑血管病变和神经退行性变中具有不同的功能。
综上所述,本研究的结果表明tau 病理学而不是 Aβ 病理学在影响血管生成因子的表达方面起着重要作用,从而导致 AD 患者血管生成异常。此外,研究发现异常的 CSF 血管生成因子与脑血管损伤之间存在密切关联,包括周细胞损伤、 BBB 渗漏、 WMH 和神经变性。这些观察结果表明,病理性血管生成可能代表了导致 AD 脑血管损伤和神经退行性变的新机制。这突出了抑制 AD 中血管过度生长或促进未成熟血管成熟的潜在治疗价值。
原始出处:
Pathological angiogenesis was associated with cerebrovascular lesion and neurodegeneration in Alzheimer's disease. Alzheimers Dement. 2025 Feb;21(2):e14521. doi: 10.1002/alz.14521. Epub 2025 Jan 8. PMID: 39777972; PMCID: PMC11848169.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)