首页 > 医疗资讯/ 正文

根据WHO的定义,T淋巴母细胞性淋巴瘤(T-LBL)与急性淋巴细胞白血病(T-ALL)一起被归类为T-LBL/ALL,迄今为止,治疗T-LBL/ALL的唯一治疗方法是异体干细胞移植,自体造血干细胞(auto-HSCT)移植后的清髓调理方案是不能接受同种异体造血干细胞移植(allo-HSCT)的患者的一种选择,全身照射(TBI)是目前广泛应用的清髓调理方法,具有较低的复发率、较好的无进展生存期(PFS)和较低的移植相关死亡率(TRM)的优势。来自郑州大学第一附属医院的研究团队开展了一项回顾性研究,目的是评价不能接受同种异体造血干细胞移植(allo-HSCT)的T-LBL/ALL患者在全身照射加环磷酰胺(TBI/Cy)治疗后自体造血干细胞移植(auto-HSCT)的有效性和安全性。
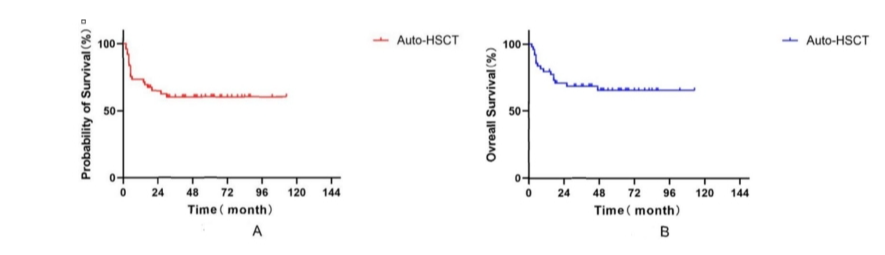
图1:T-LBL/ALL患者PFS(A)和OS(B)(n=50)
2013年至2023年,郑州大学第一附属医院肿瘤科共收治T-LBL/ALL患者50例,其中26例行同种异体 HSCT ,24例行自体 HSCT 后行TBI/Cy,所有患者在 HSCT 后均实现完整的造血重建。两组患者在无进展生存期 (PFS) 和总生存期 (OS) 的差异中无统计学意义 (P=0.791,HR 1.127,95% CI:0.456-2.785;P = 0.456,HR 0.685,95% CI:0.256–1.828)。尽管接受同种异体 HSCT 的患者累积复发率低于自体 HSCT 患者 (P=0.033,HR 3.707,95%CI 1.188–11.570,2 年复发率 11.5% vs. 33.3%),但非复发死亡率 (NRM) 的发生率高于自体 HSCT 组 (P=0.014,HR 0.000,95%CI:-1.000 -1.000,2 年 NRM 23.1% vs. 0%)。
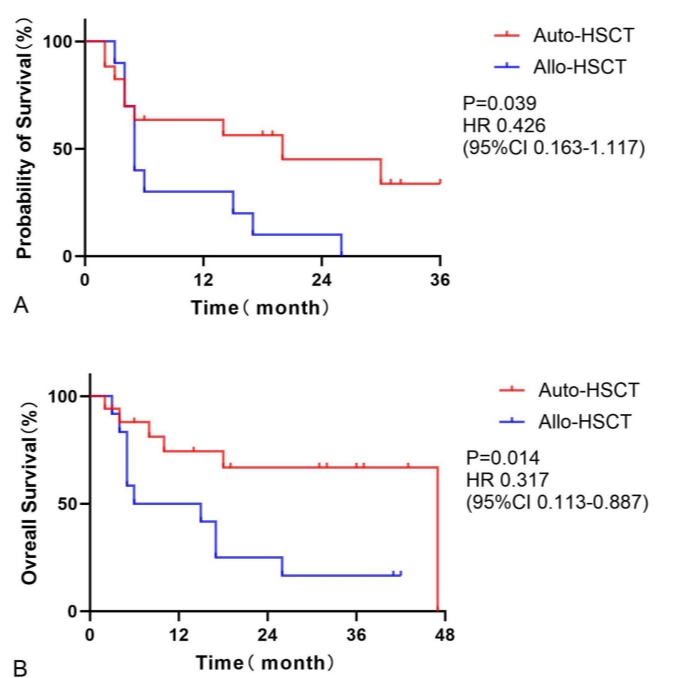
图2:接受auto-HSCT(n=24)和alloc-hsct(n=26)的T-LBL/ALL患者的PFS(A)和OS(B)。
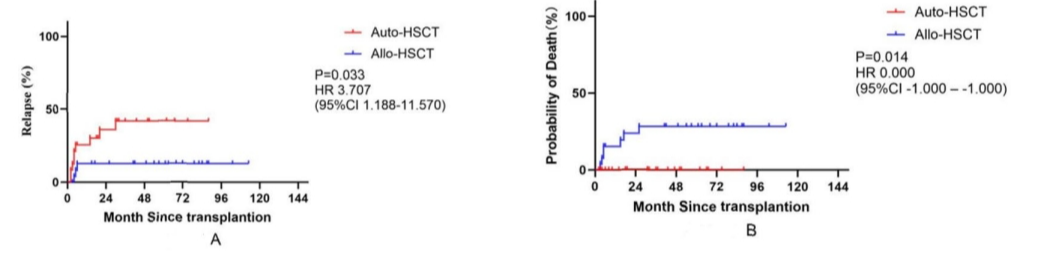
图3:接受auto-HSCT(n=24)和alloc-hsct(n=26)的T-LBL/ALL患者的累计复发发生率(A)和非复发死亡率(B)
通过Landmark分析,两组在 3 年 PFS 和 4 年 OS 曲线上显示统计学显着差异(P = 0.039,HR 0.426,95% CI:0.163-1.117;P=0.014,HR:0.317,95% CI 0.113–0.887)。通过 COX 分析,基线体能状态不良 (ECOG-PS≥2) 和 CNS 受累是 PFS 和 OS 的危险因素。
总之,T-LBL/ALL 是一种罕见的侵袭性疾病,同种异体造血干细胞移植仍然是主要治疗方法,但与治疗相关死亡率的较高发生率相关,在这种情况下,TBI/Cy 后进行自体 HSCT 是一个很好的选择。在缺乏前瞻性随机试验来为该领域的决策提供信息的情况下,该研究的数据可能有助于对个体患者的竞争风险进行仔细分析。
原始出处:
Mao J, Ge J, Ding S, et al. TBI/Cy followed by auto-HSCT is a good choice next to allo-HSCT for patients with T-LBL/ALL. Sci Rep. 2024;14(1):22356. Published 2024 Sep 27. doi:10.1038/s41598-024-72897-9
猜你喜欢
- Eur J Pediatr:“家庭餐处方”结合生活方式治疗,对肥胖儿童体重指数z评分(BMIz)及代谢健康的影响
- 女性更年期的症状有哪些 女人出现8种症状说明更年期到了
- 病例分享:这种混合密度影像像浸润的结节缘何病理仍是原位癌伴微浸润?是否藏着混合磨玻璃结节是原位癌的奥秘!
- 河南新增6例本土无症状转确诊 现有本土确诊病例166例
- 贯彻落实积极应对人口老龄化国家战略让老年人共享改革发展成果安享幸福晚年
- European Radiology:基于深度学习的软组织肿瘤CT和MRI微创交互分割
- 北京首家麦当劳叔叔之家正式启用
- 26种常见的自身免疫性疾病
- 这种水果正大量上市!3周内47名儿童死亡,只因过量食用!
- 急性心梗支架球囊杆离断导丝飞扬,抓捕器主动脉内抓出
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)