首页 > 医疗资讯/ 正文
意外创伤,如车祸、枪击或刺伤,常常造成严重的组织缺损并伴随缺损腔内难以控制的出血。可膨胀海绵已被开发用于软组织(如股动脉、肝脏和皮肤)的压迫止血,实现难以压迫出血的急救。而在真实的创伤场景中,组织损伤情况往往更为复杂(软、硬组织都可能损伤),止血海绵需要适应不同组织的力学特性、缺损形状以及不同的出血行为实现自压迫应急止血。这对海绵材料的力学结构设计提出挑战:海绵需要兼顾高的弹性模量实现压迫止血,同时需要高的变形能力实现不同组织缺损的完全填充。
针对这一问题,浙江大学医学院附属邵逸夫医院赵玥绮副研究员、方向前教授联合浙江大学刘昭明研究员,基于前期研究中所开发的无机离子寡聚体(Nature 2019, 574, 394),发现磷酸钙这类离子化合物的晶体链具有一个临界尺寸,在该尺寸下的离子结构可兼具高弯折强度和高可弯折性。以临界尺寸的磷酸钙晶体链(C-CaP)为无机机械强化单元复合到有机蚕丝(SF)结构中,可使得到的有机-无机杂化海绵(SF-C)兼具高的弹性模量和高的可变形性。因此SF-C海绵具有可靠的组织压迫止血性能、组织形状适配性能,同时表现出良好的促凝能力,在大鼠软、硬组织缺损出血模型中实现了优异的止血效果,止血速度显著快于先前报道的多种组织缺损止血材料。该研究以“Highly Deformable and Robust Ionic Structure for Multi-Tissue Adaptive Hemostatic Sponges”为题发表在《Advanced Functional Materials》期刊上。

【SF-C杂化物的制备及其表征】
研究团队首先通过丝素蛋白(SF)与磷酸钙寡聚体(CPOs)的共组装制备了SF-C杂化物。高分辨透射电镜(HRTEM)的结果表明,SF-C杂化物中的磷酸钙(CaP)在SF中表现为一维的链状结构,其平均长度为35 nm,厚度为1.8 nm。XRD结果显示,SF-C杂化物在(002)的衍射峰强度相对(211)较高,这表明其中的CaP晶体链在c轴上具有更优的取向。此外,SF-C杂化物在(210)和(300)上没有观察到衍射峰,表明CaP晶体沿a轴和b轴生长受限。根据XRD确定的晶向,研究人员模拟了SF-C杂化物中CaP的晶体结构,其表现为沿a轴和b轴只有两个重复晶胞单元的离子晶体结构。
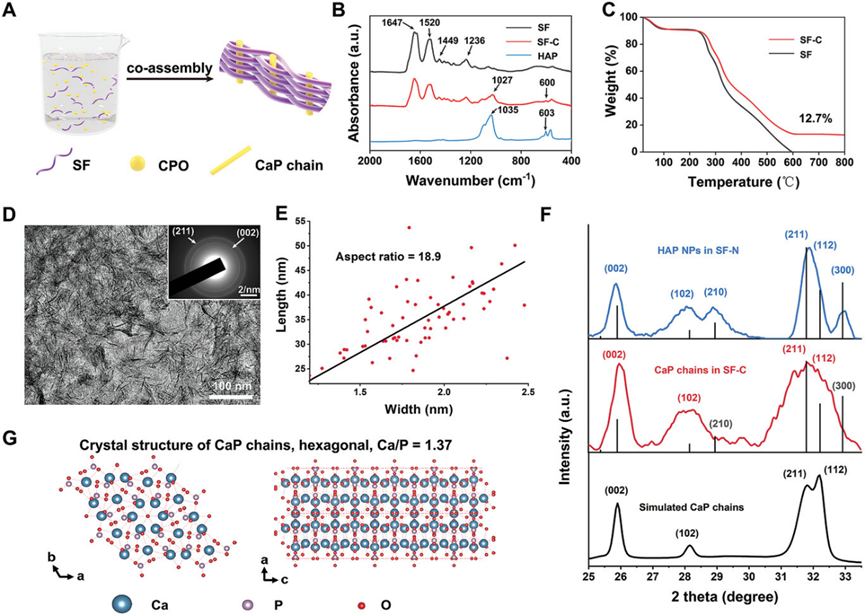
图1 SF-C杂化物的制备及其表征
【高弯折强度且可变形的离子晶体链结构】
值得注意的是,SF-C杂化物中的CaP晶体链具有从0°到73°的弯曲角度,这表明该晶体链具有一定的可变形性。这种高弯曲角度通常发生在聚合物链弯曲的情况下,而在无机晶体中则并不常见。研究团队对其他有机-CaP杂化体系(尺寸≈1 nm或>3 nm)的研究表明,当CaP的尺寸≈1 nm时,无机寡聚体均匀分布在有机基质内。在这些有机-CaP混合体系中,力学性能与无机含量有关,无法平衡韧性与变形性。而尺寸范围在3 - 10 nm的CaP晶体则表现出刚性和直的形态,缺乏变形能力。由此推测,CaP晶体的韧性和变形性可能与尺寸有关。随后,研究人员用简化的晶格模型分析了弯曲角、离子结构厚度与离子结构长度之间的关系,并通过分子动力学模拟的方法对其进行验证。结果表明,CaP离子晶体链的变形能力与其厚度直接相关,较薄的CaP晶体链(0.95 nm)可变性但缺乏一定的弯曲能,较厚的CaP晶体链(6.65 nm)在外力下表现为断裂而非变形,而1.8 nm恰好是其临界尺寸。该临界尺寸的CaP离子晶体链(C-CaP)在具有一定的变形能力的同时拥有较强的弯曲能(655 kBT,显著高于聚合物链的20 ~ 150kBT),实现了韧性和变形性之间的平衡,对提升有机-无机杂化材料的机械强度和可变形性具有重要意义。
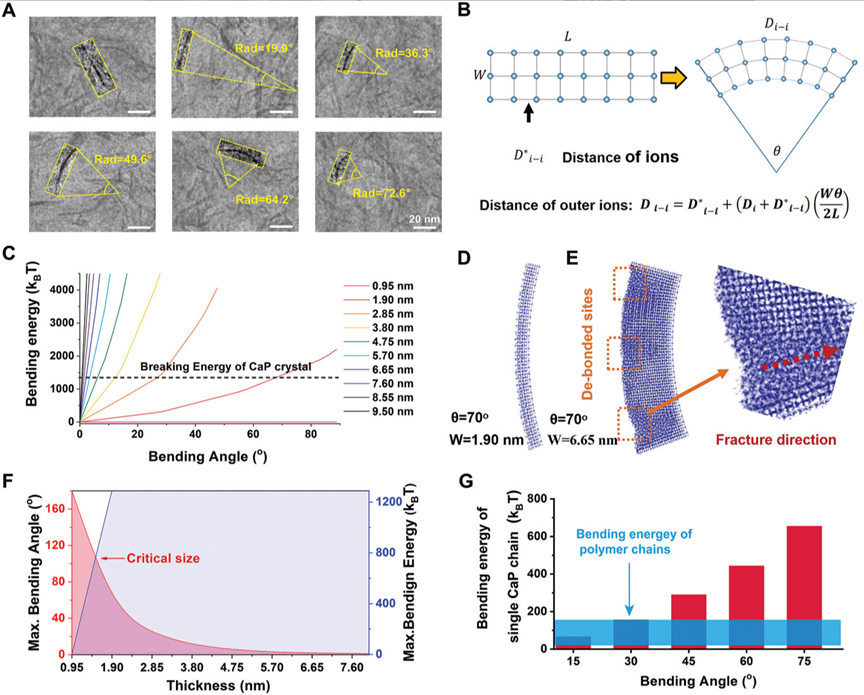
图2 C-CaP的表征及分子动力学模拟
【SF-C杂化海绵的机械性能与形状适配性能】
随后,研究人员通过低温退火将SF-C杂化物制备成SF-C海绵并对其性能进行测试。结果显示,SF-C海绵具有良好的机械性能以及液体吸收性能,这得益于C-CaP对SF的机械强化作用。此外,C-CaP并不会影响海绵的变形能力,SF-C海绵在不同模具中均展现了良好的适配能力,其形状适配分辨率(SAR)达到了10 μm以下,能够良好地匹配毛细血管的尺寸。因此,C-CaP的添加赋予了SF-C海绵良好的机械性能、超快的液体吸收性能和高形状适配性能,极大地提高了其在复杂组织缺损出血治疗中的可靠性。
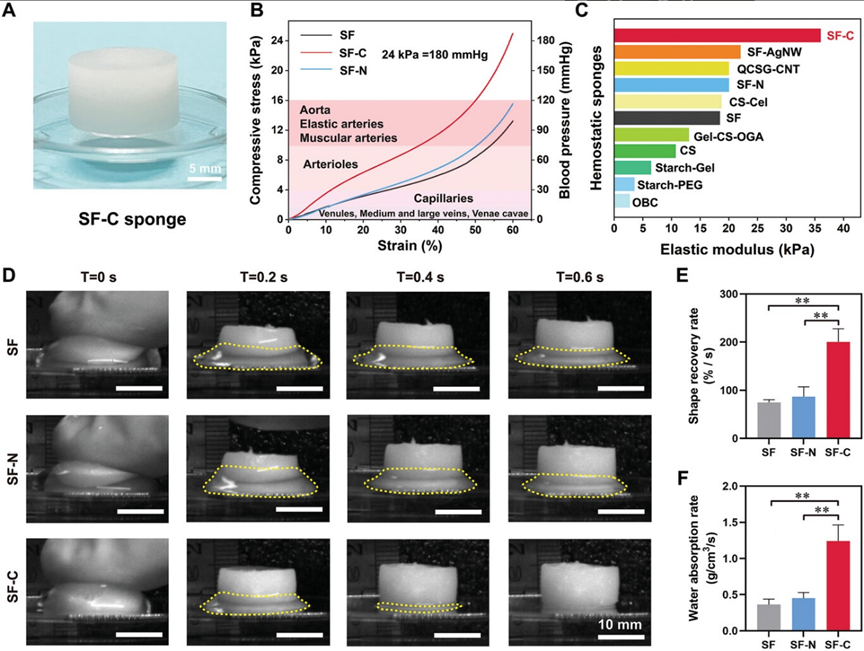
图3 SF-C杂化海绵的机械性能与液体吸收性能
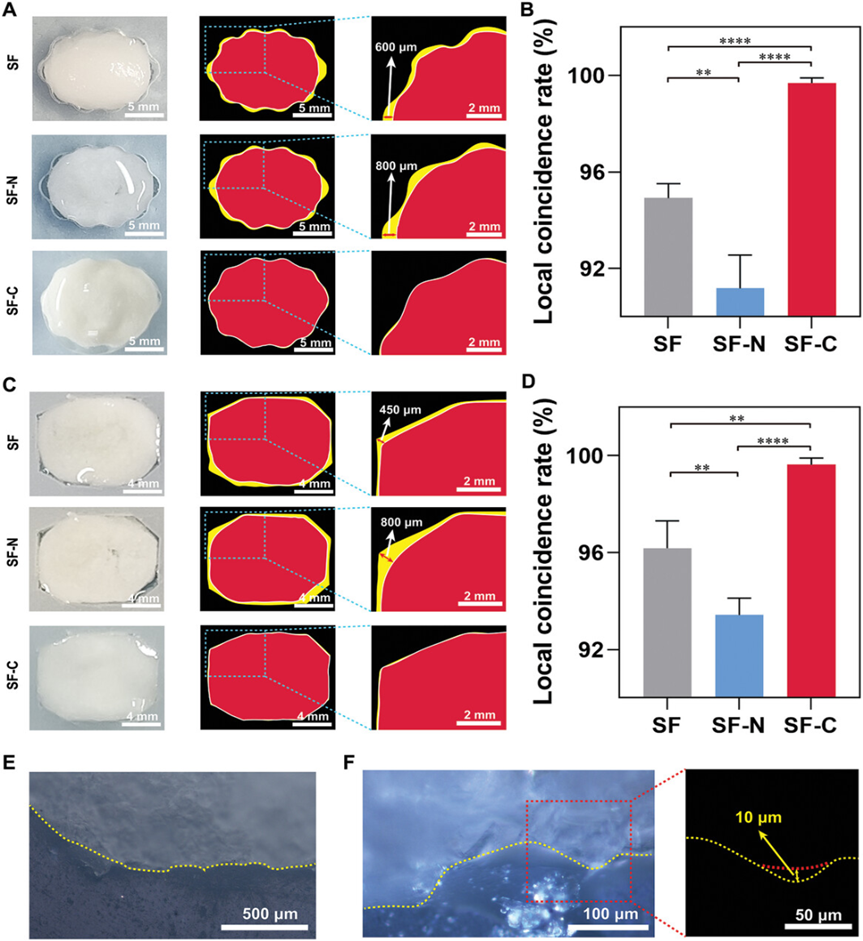
图4 SF-C杂化海绵的形状适配性能
【SF-C海绵的促凝能力】
为了进一步探究SF-C海绵在止血方面的潜力,研究人员对其促凝能力进行了测试。结果显示,SF-C海绵具有良好的促凝能力,这得益于SF的促凝作用以及CaP对于血液成分的影响。SF-C海绵中均匀分布的C-CaP暴露出了丰富的Ca2+位点,其能够通过静电相互作用提高止血海绵对红细胞、血小板的吸附,进而促进血液的凝固。
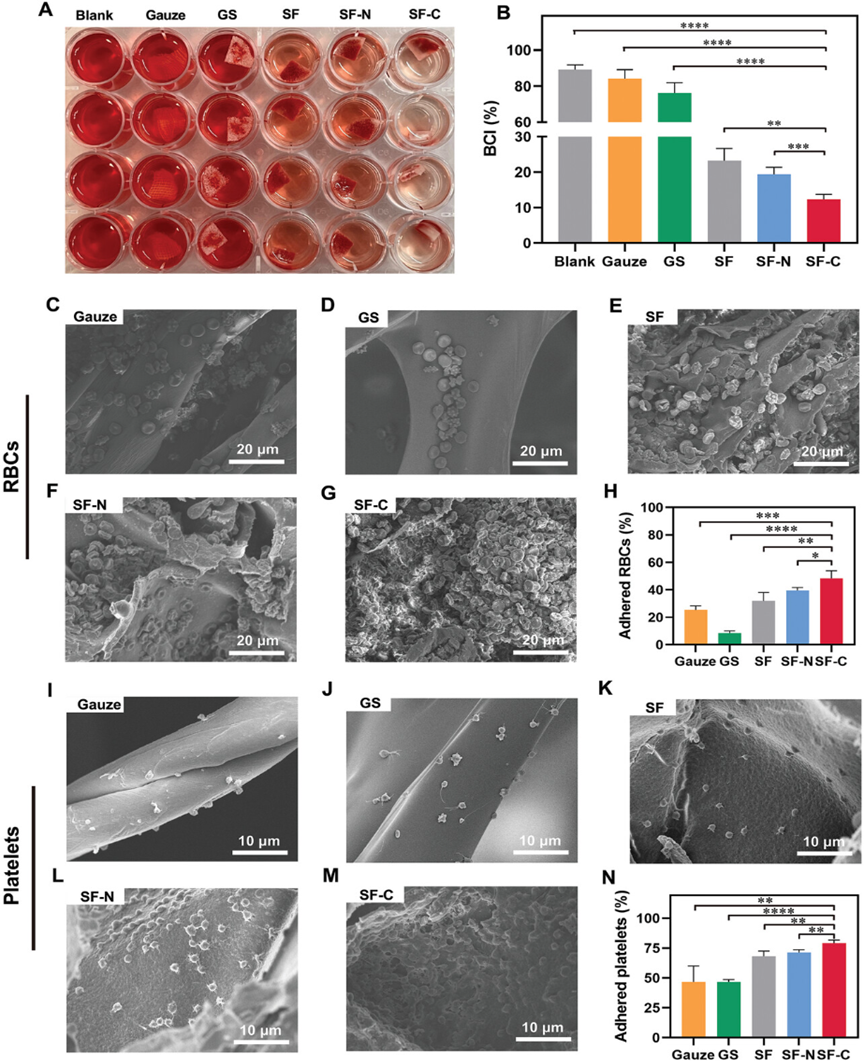
图5 SF-C杂化海绵的促凝能力
【SF-C海绵在软、硬组织中的止血性能】
得益于力学性能以及促凝能力的提升,SF-C海绵在软、硬组织损伤出血模型中均展现出了优异的止血效果。在肝脏穿透性损伤出血模型中,SF-C海绵能够快速吸血并压迫缺损组织中的受损血管进而实现止血的目的,其总失血量仅为医用明胶海绵的1/4左右。在胫骨缺损出血模型中,SF-C海绵能够更好地适配缺损的胫骨,有效地减少了止血海绵与骨组织交界处的渗血,总失血量仅为医用明胶海绵的1/6左右。
研究团队尝试标准化了材料的止血速度(Standardized blood loss ratio, SBLR),通过Standardized blood loss ratio (SBLR) =Wcontrol group / Whaemostatic sponge 进行评价:越高的SBLR数值表明越少的失血(越快的止血)。SF-C海绵在软、硬组织止血速度中均表现出优异的效果,且其多组织缺损的止血能力也具备显著优势。上述实验结果表明,SF-C海绵在治疗复杂组织损伤出血中具有一定的优势和临床应用潜力。
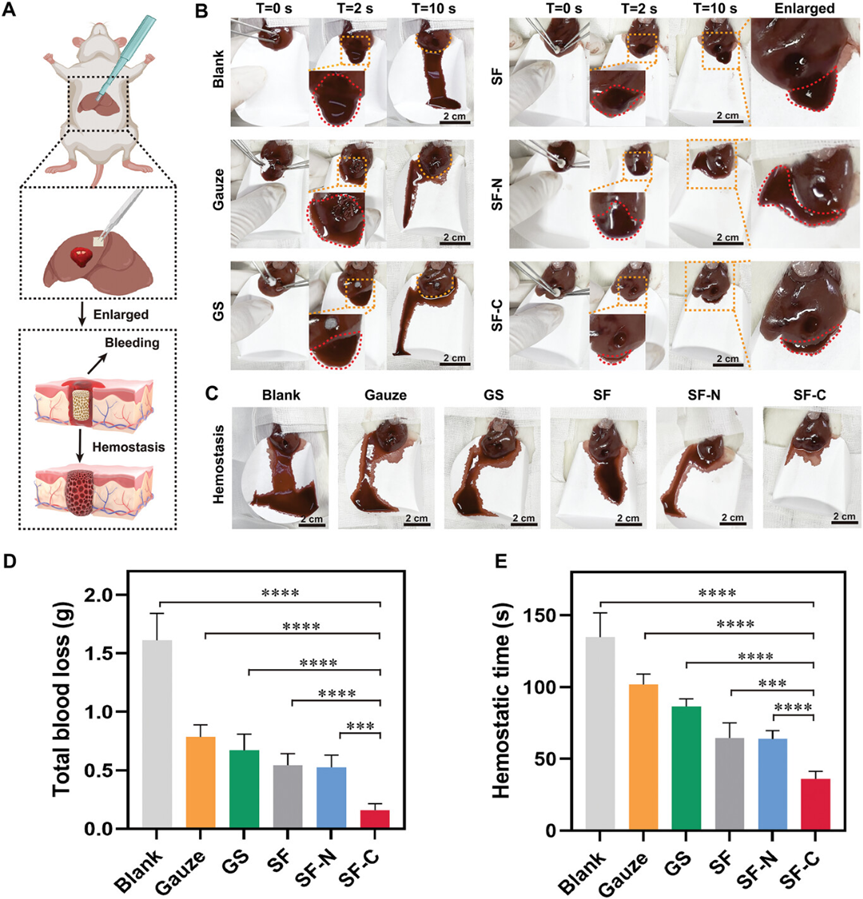
图6 SF-C杂化海绵在大鼠肝脏穿透性损伤出血模型中的止血效果
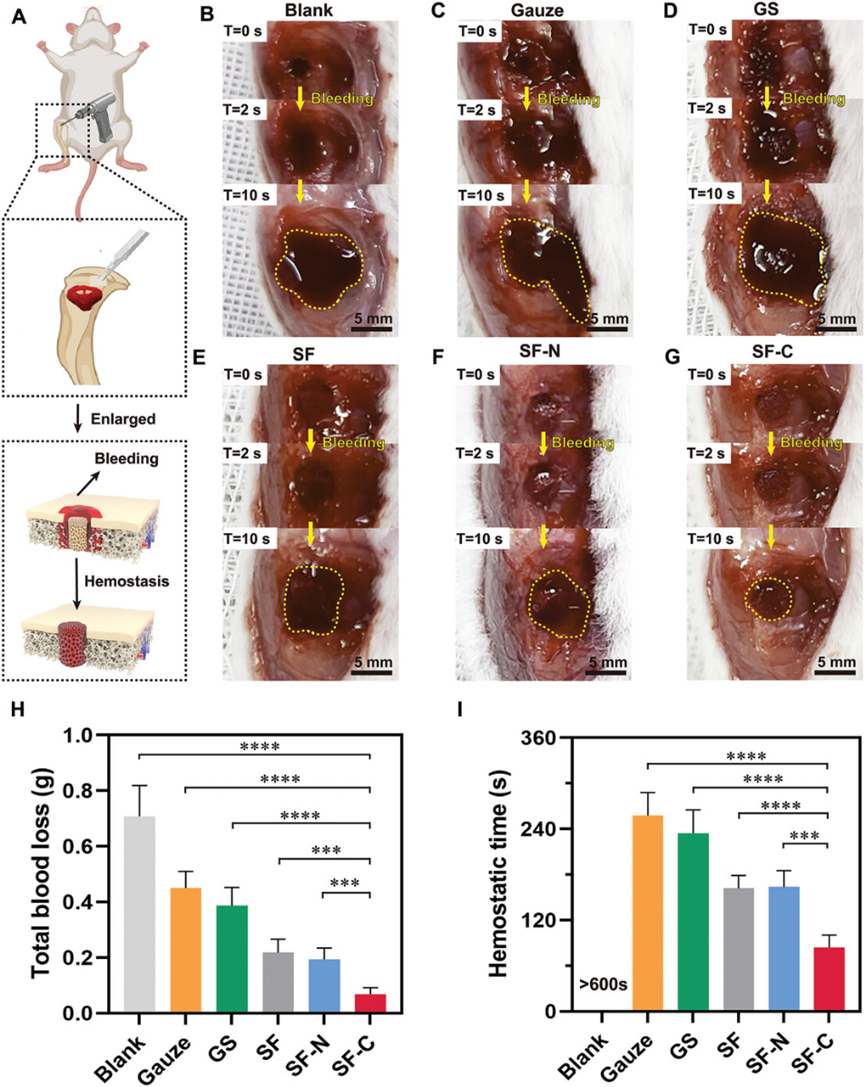
图7 SF-C杂化海绵在大鼠胫骨缺损出血模型中的止血效果
【总结】
该工作发现了临界尺寸下的磷酸钙离子晶体链的力学特性,可具有类似矿物的高弯曲强度和类似聚合物的可变形性。研究人员通过将临界尺寸的CaP晶体链杂化到SF海绵中制备了有机-无机杂化海绵(SF-C),拥有良好的力学强度、形状适配性能以及促凝能力,在大鼠软、硬组织损伤出血模型中均呈现出了优异的止血效果,为治疗复杂组织损伤出血提供了一种非常具有吸引力的止血海绵材料。此外,离子结构中临界尺寸的发现为材料强度与可变形性(这一对矛盾力学)的整合提供新理解,拓宽了人们对于纳米结构材料的设计思路。该项目受到国家自然科学基金(22105168, U22A20282, 22435006, 22275161),浙江省尖兵领雁计划(2024C03080),中央高校基本科研业务费(2022ZJJH02-01, 226-2024-00097)的资助。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)