首页 > 医疗资讯/ 正文
CD19/20双靶点CAR-T
非霍奇金淋巴瘤(NHL)是造血系统常见恶性肿瘤,传统疗法对复发/难治性NHL(R/R NHL)的疗效有限,尤其是对于弥漫性大B细胞淋巴瘤(DLBCL)患者。CAR-T细胞疗法是一种新型高效的免疫疗法,用于治疗R/R造血系统恶性肿瘤,但可能由于体内CAR-T细胞的丢失或抗原的丢失而发生复发,避免CAR-T细胞治疗后抗原丢失的方法之一便是同时靶向另一个抗原。同时靶向CD19和CD22的双靶点CAR-T疗法在R/R B细胞急性淋巴细胞白血病中已经证实疗效和安全性。
深圳大学总医院于力教授团队协同深圳豪石生物开展一项I/II期研究,旨在探索双靶点CD19/20 CAR-T治疗R/R B-NHL的潜力。结果近日发表于《Blood Cancer Journal》。

研究结果
该研究为开放标签、单臂I/II期,纳入11例接受自体CD19/20 CAR-T细胞输注的R/R B-NHL成年患者进行分析(共13 例进行单采),所有患者在CAR-T细胞输注前均接受氟达拉滨联合环磷酰胺的预处理化疗。输注细胞的剂量范围为0.31×106到2.62×106个CAR-T细胞/公斤,中位1.05×106个CAR-T细胞/公斤。
11例患者年龄中位数为59岁,9例为GCB或non-GCB DLBCL。所有患者(100%)均为CAR初治和III期或IV期。4例为双表达(表达c-MYC和BCL2) DLBCL。半数患者活检显示Ki67阳性率超过70%。3例为难治性疾病,其余8例NHL患者经抗肿瘤治疗后复发。
随访12.63个月,大多数患者达到完全缓解(70%),总缓解率为90%,缓解持续时间为11.83个月,中位无进展生存期和总生存期均未达到,3个月和12个月生存率分别为90.91%和81.82%,无进展生存率分别为90%和60%。
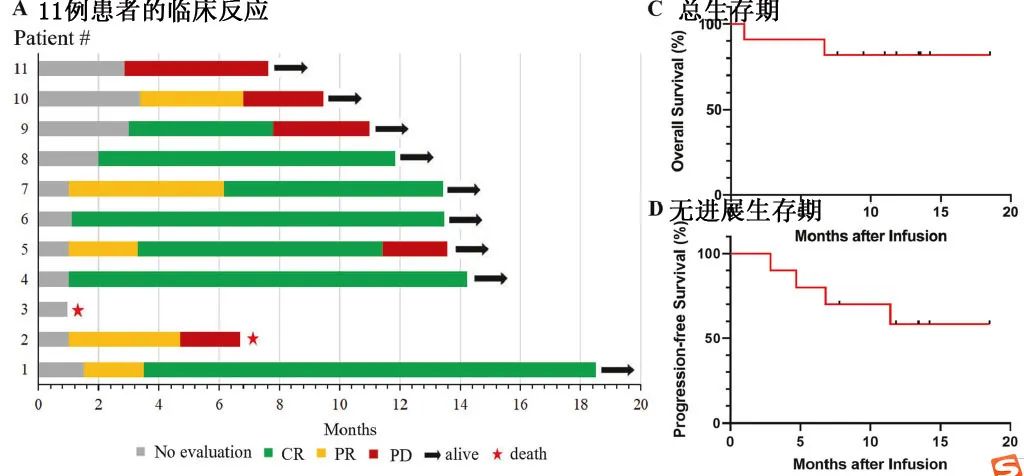
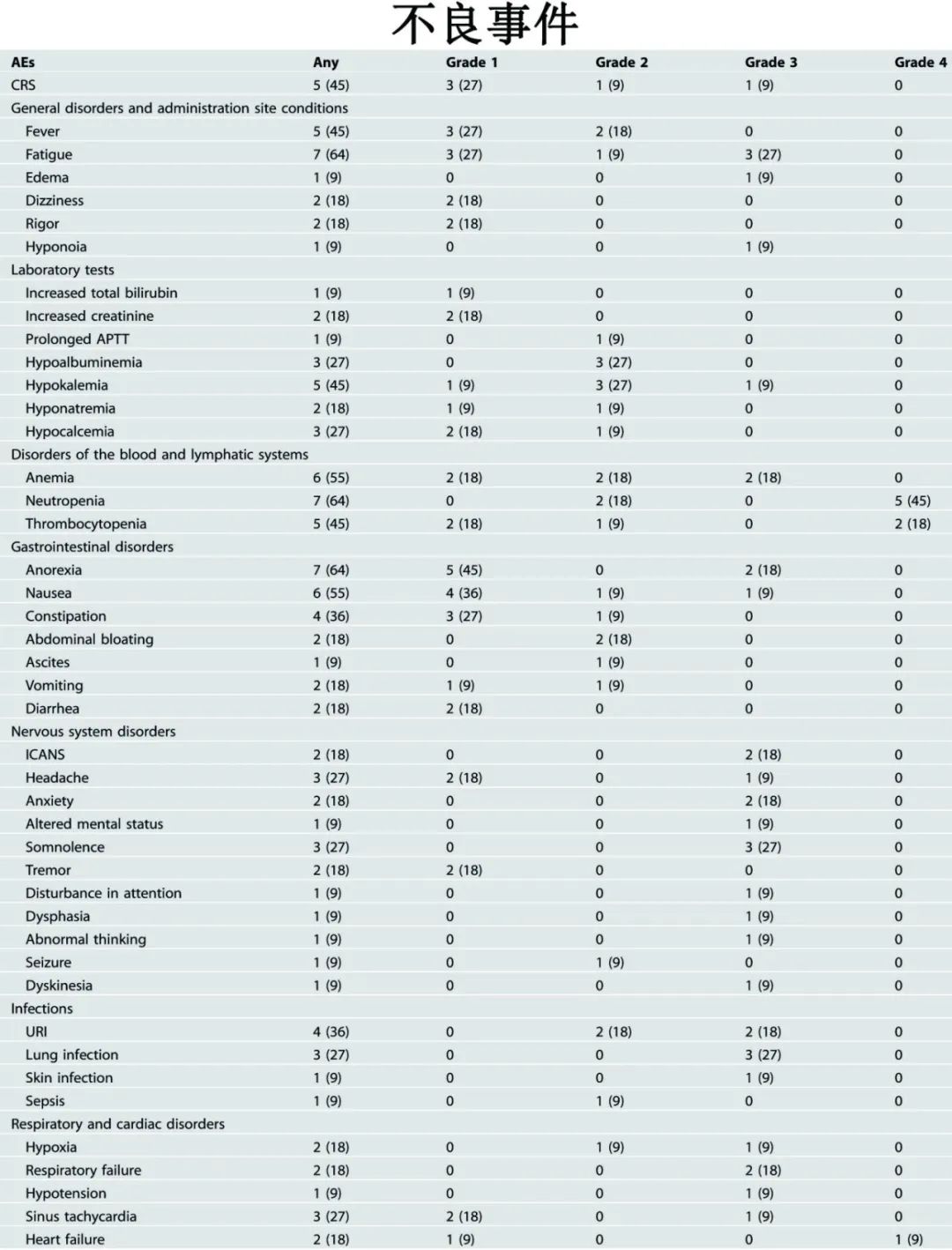
5例(45%)患者发生CRS,中位至发作时间为输注后4天,中位持续时间为2天;4例为1或2,1例为3级,症状为发热、低血压和严重低氧血症;由于复发和肺部感染,一例患者在161天后发生迟发性CRS(3级)。2例患者(18%)发生ICANS,为3级,输注后至ICANS发作的中位时间为11天,中位持续时间为1天。未观察到明显的残余神经损伤。≥3级不良事件包括水肿(n=1,9%)、精神迟钝(9%)、厌食症(n=2、18%)、恶心(9%)、上呼吸道感染 (18%)、肺部感染(n=3,27%)、皮肤感染(9%)、窦性心动过速(9%)、心力衰竭(9%)、贫血(18%)、低钾血(9%)、中性粒细胞减少(n=5,45%)、血小板减少(18%)和肌肉骨骼障碍(18%)。
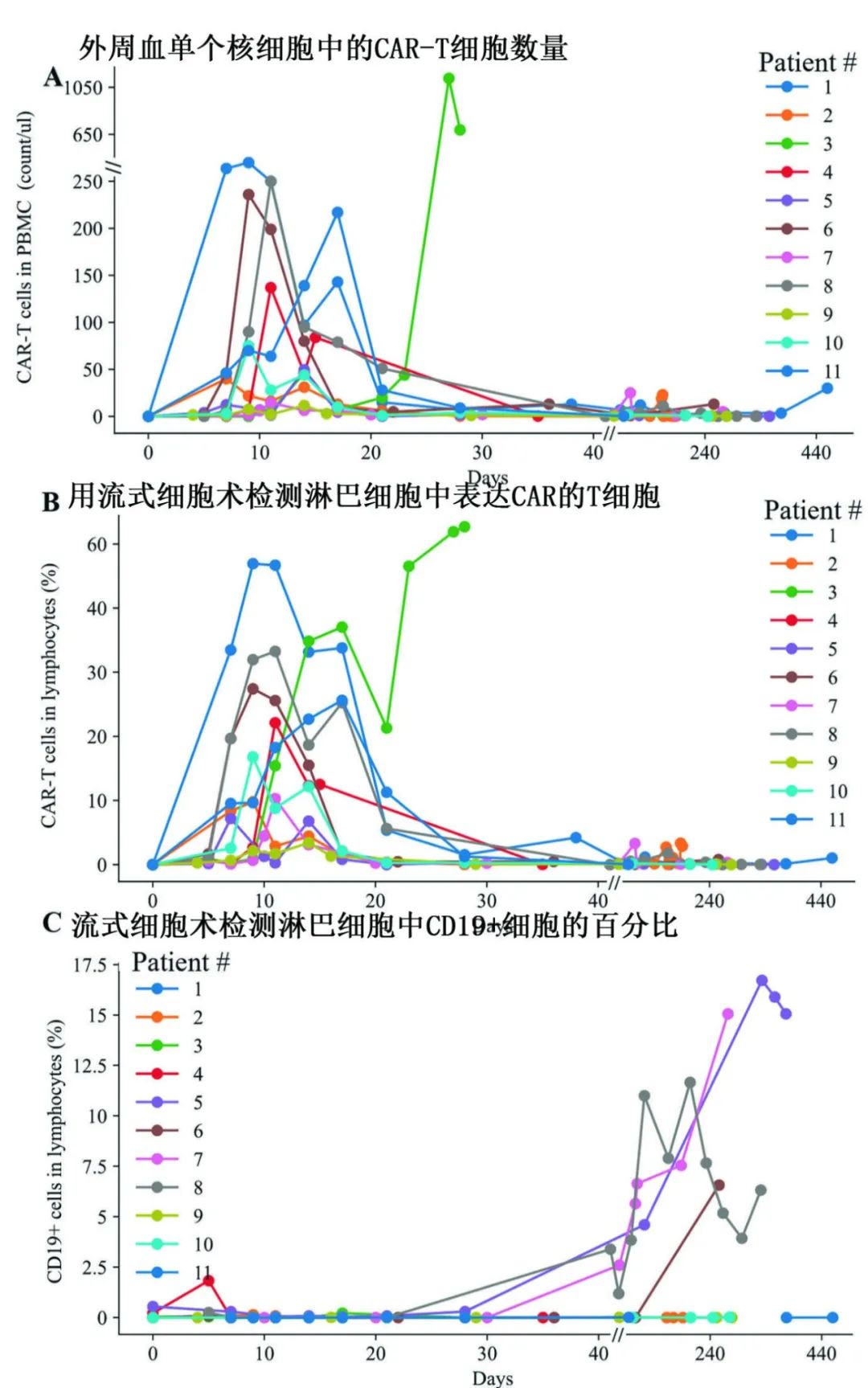
利用流式细胞术监测CAR-T细胞输注后不同时间点外周血中CAR-T细胞,对所有患者的CAR-T细胞扩增数据进行分类并绘制为动态曲线,该曲线在不同患者之间存在差异。CAR-T细胞在输注后第2周(第7天至第14天)出现第一次高增殖。在扩增高峰时,外周血单个核细胞(PBMC)中检测到高达65.41%的CAR-T细胞(中位数22.12%)。9例应答患者者中有5例持续可检测到CAR-T细胞,所有5例患者都保持持续CR,证实双靶点CAR-T细胞的体内扩增和持久性。CAR-T细胞输注后,所有患者外周血B细胞均降至检测以下,4例患者(36.4%)在CAR-T细胞输注后100天CD19+ B细胞恢复正常。
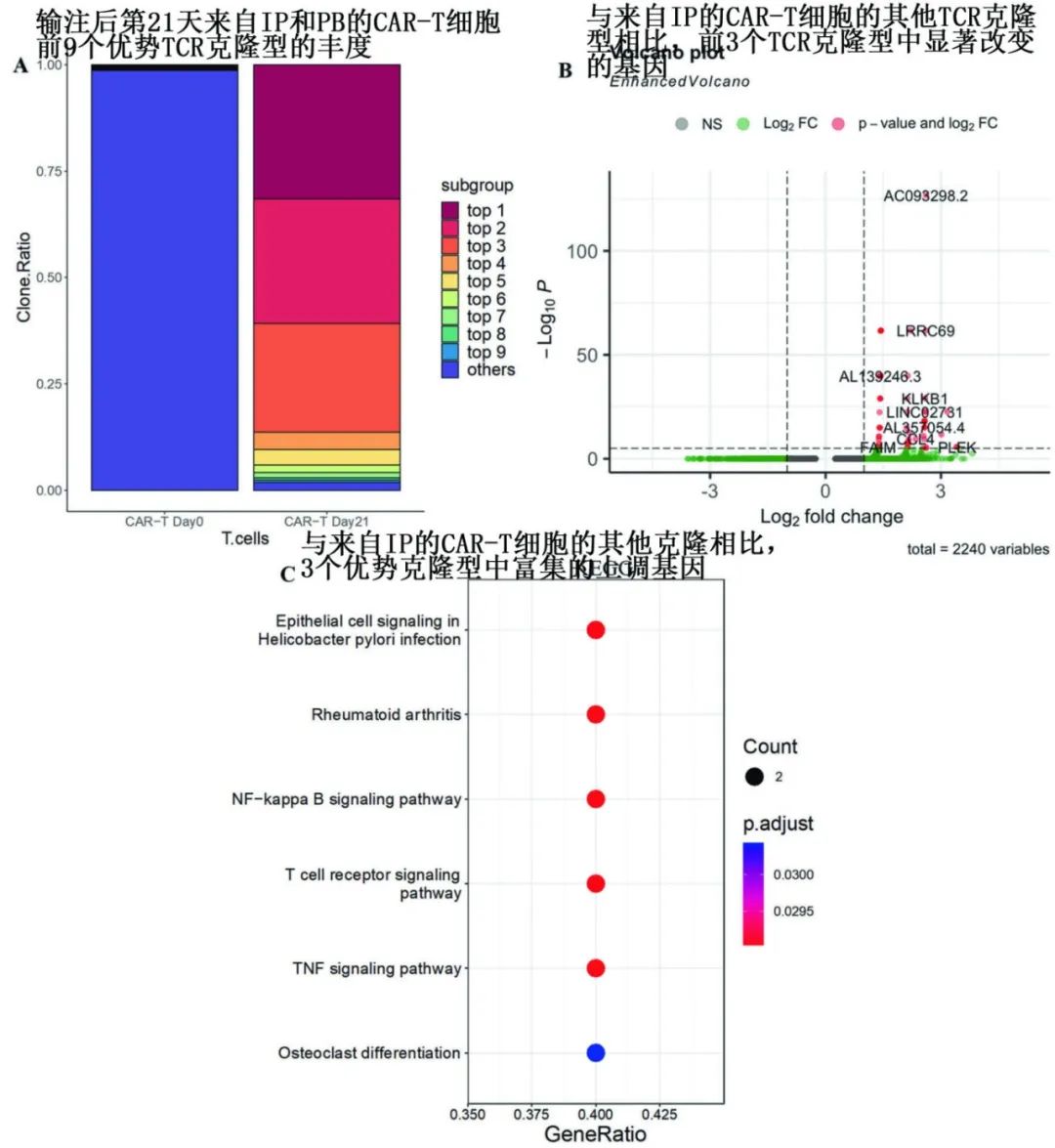
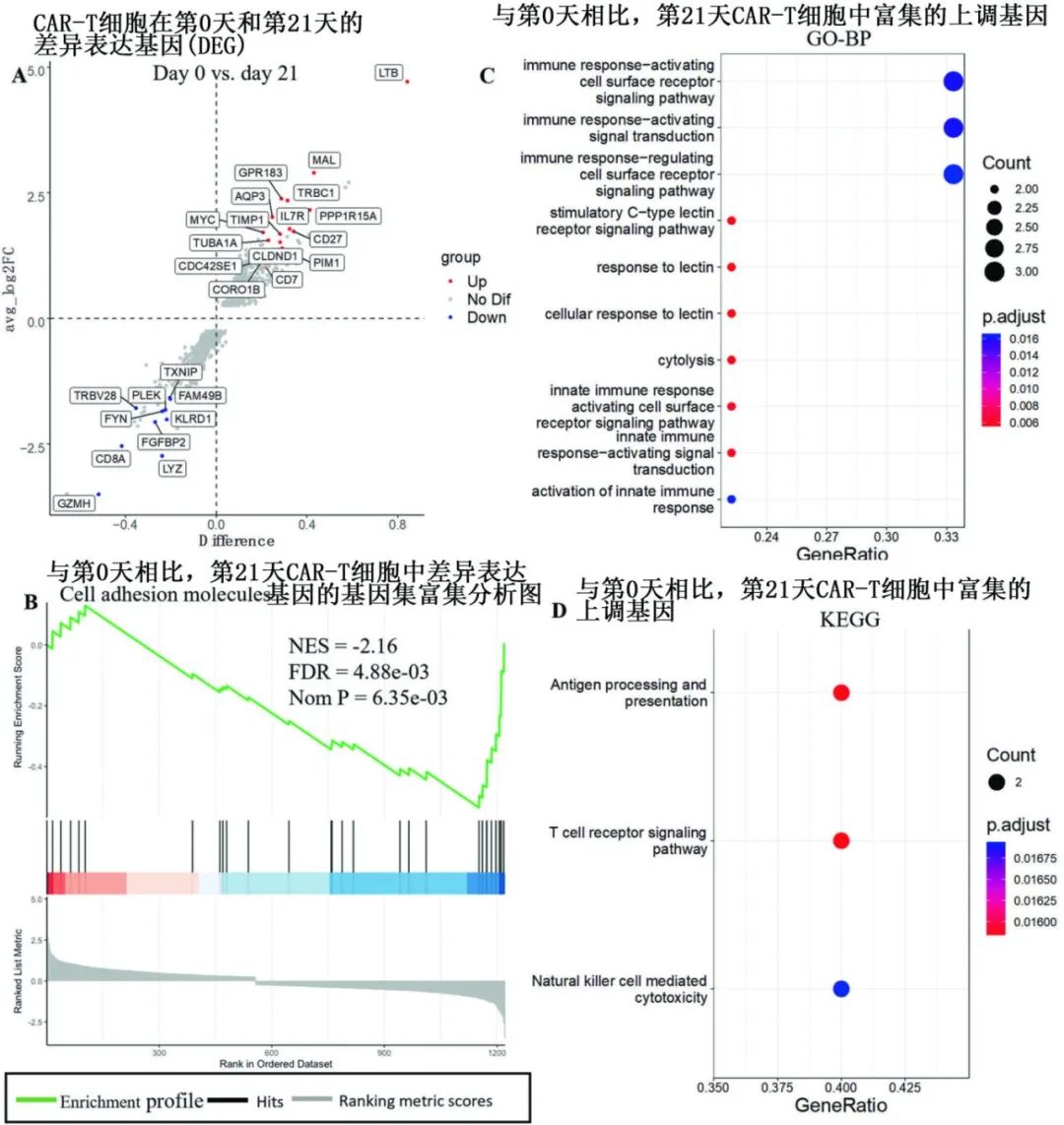
CAR-T细胞输注后CAR-T细胞库的动力学方面,在CAR-T输注产品中共鉴定出1796个克隆,输注后其中仅保留168个克隆,其中部分克隆在输注21天后的外周血样本中扩增。与0天时几乎100%相比,第21天时IP中前9种CAR-T细胞克隆型的比例较低。这些数据表明,输注后CAR-T细胞在血液中表现出较低的多样性和较高水平的克隆扩增。前3个TCR克隆占总CAR-T细胞的80%以上。然后在第21天聚焦从IP和PB样品中获得的CAR-T细胞的前3个TCR克隆型。比较的CAR-T细胞的前3个TCR克隆与来自IP的其他克隆的差异表达基因后发现,前3个TCR克隆的免疫相关信号通路相关基因的倍数变化更高,但在第21天时,两种类型的CAR-T细胞之间的基因表达没有差异。体内扩增的TCR克隆主要来源于输注产物(IP)中免疫相关信号通路相关基因表达增加的TCR克隆。
重点分析了第21天IP和PB中CAR-T细胞的差异表达基因。与来自IP的CAR-T细胞相比,第21天CAR-T细胞中16个基因的表达增加,且第21天的CAR-T细胞显示出与细胞粘附分子相关的特征。与来自IP的CAR-T细胞相比,第21天的CAR-T细胞表现出免疫应答和细胞溶解/细胞毒性,证实体内CAR-T细胞的动力学与免疫应答和细胞溶解/细胞毒性相关基因表达的增加相关。
总结
该I/II期研究证明靶向CD19和CD20的自体CAR-T治疗R/R NHL的安全性和有效性,突出了双靶点CAR-T在细胞免疫治疗中的价值。但该研究的样本量较小,需要更大的患者队列来进一步验证该方法的长期有效性和安全性。体内TCR克隆的增殖主要来源于输注产物中与免疫相关信号通路相关的基因表达升高的克隆,而体内CAR-T细胞的动力学与免疫反应和细胞溶解/细胞毒性相关基因的表达增加相关。
参考文献
Wang, L., Fang, C., Kang, Q. et al. Bispecific CAR-T cells targeting CD19/20 in patients with relapsed or refractory B cell non-Hodgkin lymphoma: a phase I/II trial. Blood Cancer J. 14, 130 (2024). https://doi.org/10.1038/s41408-024-01105-8
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)