首页 > 医疗资讯/ 正文
一、活检标本
1、大体检查
Ⅰ级推荐:记录组织大小与数目
2、光镜下检查
Ⅰ级推荐:明确病变性质和组织学类型;肿瘤/非肿瘤;良性/恶性;组织学类型;浸润层次(如果有)。
Ⅱ级推荐:用于诊断的免疫组化标志物检测
-
病理诊断困难时,可根据胃肿瘤的诊断与鉴别诊断、预后评估及治疗等需要选择胃癌诊断相关标记物检测。
Ⅲ级推荐:评估是否幽门螺旋杆菌(Hp)感染(ⅠB类)
-
胃幽门螺杆菌(Hp)感染状态是第8版胃癌分期要求登记的项目之一。具备条件的医疗单位应对胃癌患者的Hp状态进行评估并登记。
与NCCN指南比较
NCCN指南指出病理报告中应包括:
-
浸润(若存在)
-
组织学类型(胃腺癌的亚型分类(区分肠型或弥漫型)可能对治疗具有⼀定指导意义,因为肠型腺癌HER2过表达可能性更大。)
-
分级
-
推荐对所有新诊断的患者通过PCR/NGS进行MSI或通过IHC行MMR通用检测
二、内镜下切除标本(EMR/ESD)
内镜切除(EMR/ESD)已成为早期胃癌有效的治疗策略。EMR/ESD标本应由内镜或手术医师充分展开、固定于木板或泡沫板上进行钉板固定。按2~3mm间隔并垂直于黏膜面进行全部取材、制片观察。
1、大体检查
Ⅰ级推荐:肿瘤部位;肿瘤大小(cm3)
-
第8版AJCC/UICC分期系统对胃癌和食管癌/食管胃交界部(GEJ)癌的分期标准做出了明确的定义:对于GEJ癌,若肿瘤侵及EJ线且肿瘤中心位于EJ线以下<2cm(Siewert分型为I型和Ⅱ型),采用食管癌分期标准;若累及EJ线但其中心位于EJ以下≥2cm或未累及EJ线的肿瘤(Siewert分型为Ⅲ型),则采用胃癌分期标准。因此,准确判断胃食管交界线的位置及其是否受到肿瘤侵犯对于评估这一区域肿瘤至关重要。
胃肿瘤的解剖部位编码:
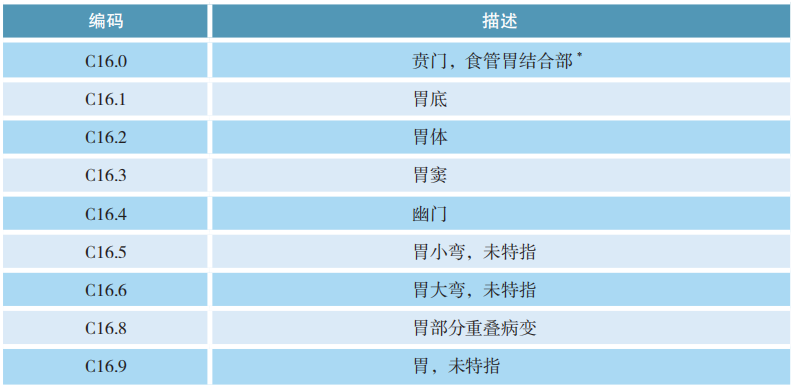
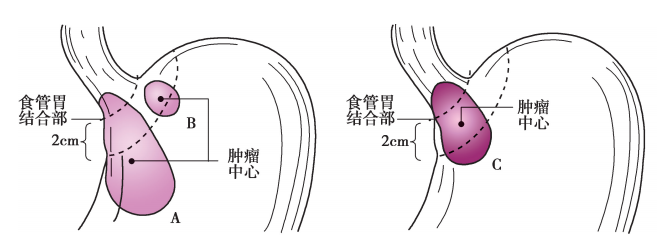
食管胃结合部肿瘤分期示意
(1)肿瘤中心距EGJ>2cm进入近端胃,应按胃癌进行TNM分期。
(2)不累及EGJ的贲门癌(肿瘤中心距EGJ<2cm)按胃癌进行TNM分期。
(3)累及EGJ且肿瘤中心位于距EGJ<2cm的胃近端,按食管癌进行TNM分期。
2、光镜下检查
Ⅰ级推荐:上皮内瘤变/腺瘤级别(低级别/高级别);浸润性癌:组织学类型/Lauren分型、组织学分级、浸润深度(pT分期)、水平切缘和基底切缘、血管淋巴管侵犯
-
胃癌组织病理学分类参照2019年版的《WHO消化系统肿瘤学分类》。病理诊断分型有困难建议提交上级医院会诊。
胃肿瘤组织学分类(WHO消化系统肿瘤学分类,2019版)
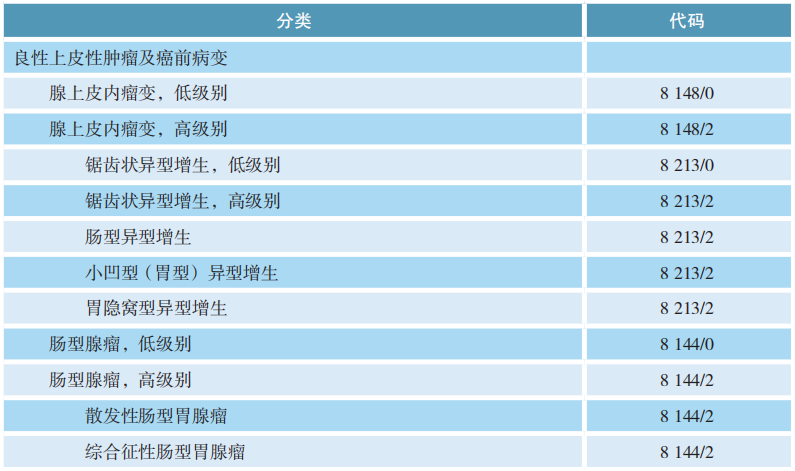
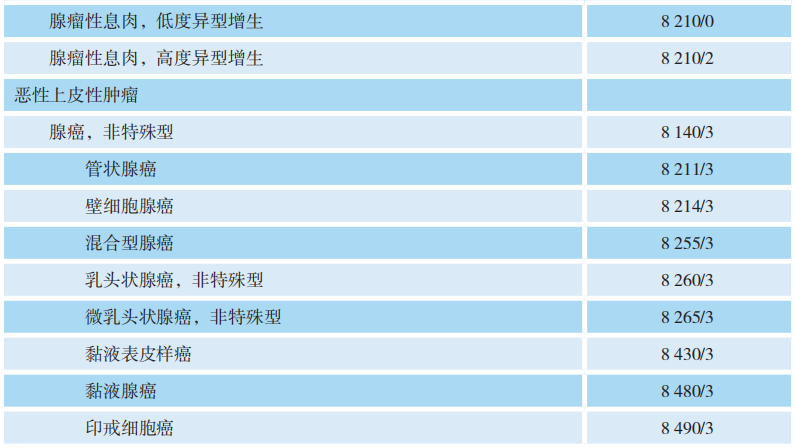
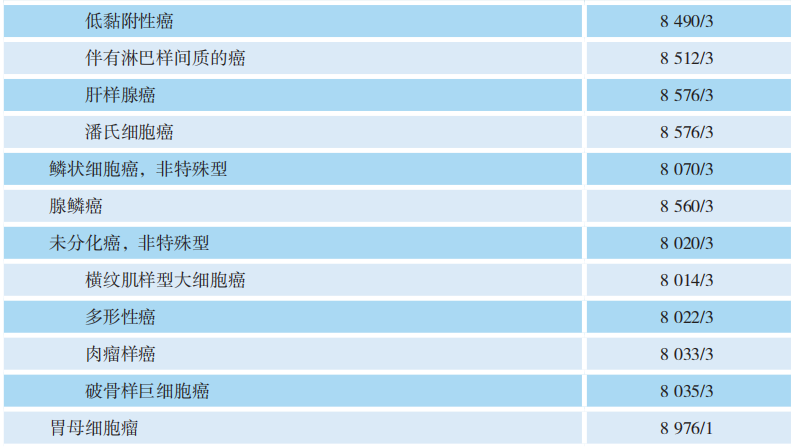
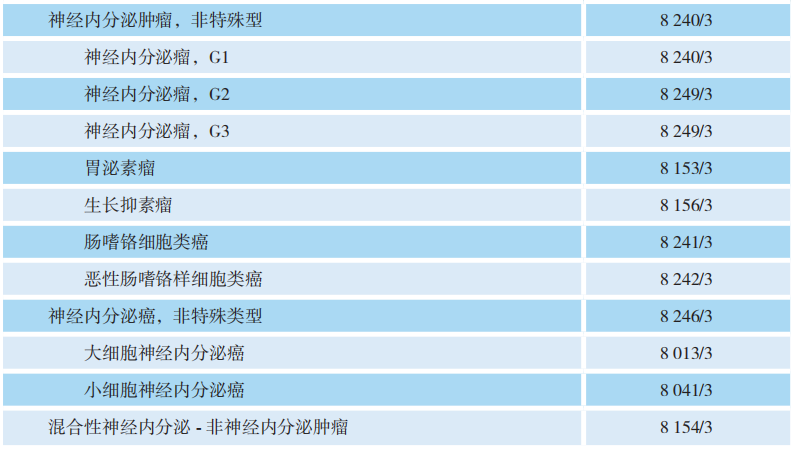
-
Lauren分型根据胃癌组织学生长方式将胃腺癌分为肠型、弥漫型、混合型。肠型:肿瘤主要由高至中分化的异型腺体组成,有时在肿瘤浸润前缘可呈现低分化。弥漫型:肿瘤由黏附性差的细胞组成,广泛浸润胃壁,很少或没有腺体形成。混合型:含有大致相同数量的肠型与弥漫型的胃癌。
Ⅱ级推荐:用于诊断的免疫组化标志物检测;早期胃癌大体类型
-
早期胃癌:癌组织局限于黏膜内及黏膜下层,不论是否伴有区域淋巴结转移。
Ⅲ级推荐:评估是否幽门螺旋杆菌(Hp)感染(ⅠB类)
与NCCN指南比较
NCCN指南指出病理报告中应包括:
-
浸润(若存在)
-
组织学类型
-
分级
-
肿瘤浸润深度
-
⾎管/淋巴管浸润
-
黏膜及深切缘状态
-
推荐对所有新诊断的患者通过PCR/NGS进行MSI或通过IHC行MMR通用检测
三、无术前辅助治疗的手术切除标本
1、大体检查
Ⅰ级推荐:手术标本类型;肿瘤部位;肿瘤大小(cm3);肿瘤距近/远侧切缘距离;淋巴结检出数目和分组(至少检获16枚、最好检获>30枚淋巴结)。
-
送检的分组淋巴结均应取材包埋,未经新辅助治疗的根治术标本应检出不少于16枚淋巴结,若为获得更准确的分期,获检淋巴结数量最好>30枚。为了准确判断淋巴结转移范围,推荐外科医师及病理医师按照胃区域淋巴结分组进行取材和分组报告。
胃区域与远处淋巴结分组标准:
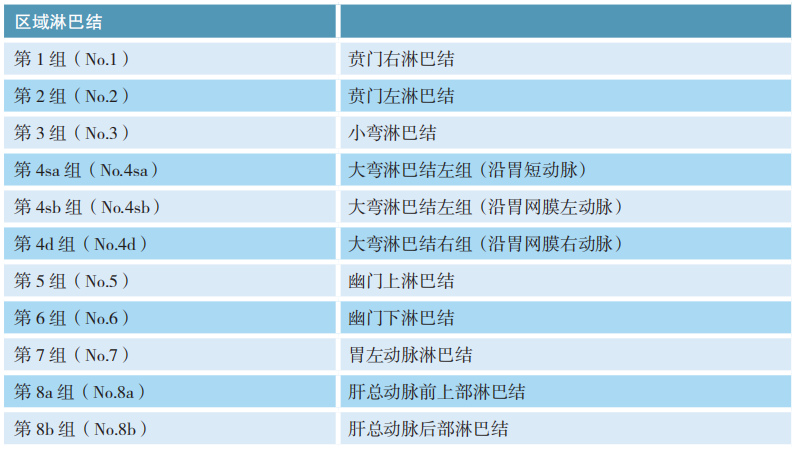

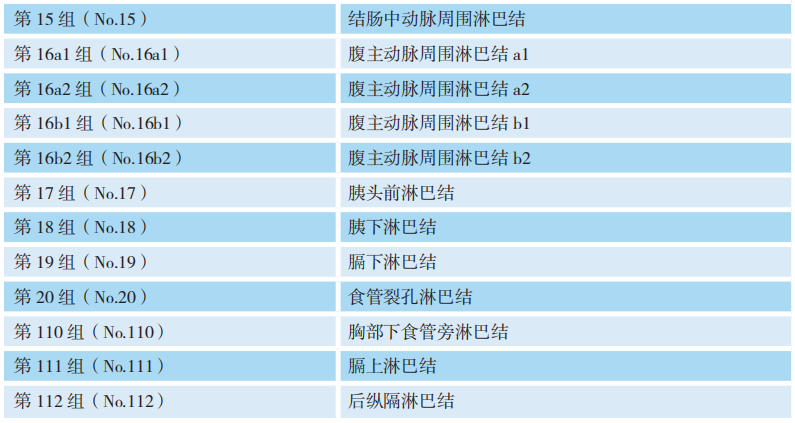
注:*远处(非区域)淋巴结转移视为转移性疾病(M1)。
2、光镜下检查
Ⅰ级推荐:组织学类型/Lauren分型/组织学分级(G1、G2、G3)/浸润深度(pT分期);血管、淋巴管、神经侵犯近/远侧切缘;食管/十二指肠侵犯情况(如切取);淋巴结转移数/受检淋巴结数(pN分期);癌结节数目;远处转移(pM分期);pTNM分期(第8版)
-
本指南推荐采用距切缘1mm内见癌细胞定义为切缘阳性。
-
原发灶相邻的浆膜下癌结节,虽然无残留淋巴结组织结构,仍被认为是区域淋巴结转移。推荐对区域转移性淋巴结和癌结节进行分别记录。
-
胃癌局部或区域之外的部位获取、经病理证实的转移性病灶被视为远处转移(pM1):包括手术切除的远处站点淋巴结以及其他器官组织中见癌细胞累及(如腹腔灌洗液或腹膜种植结节)。
Ⅱ级推荐:用于诊断的免疫组化标志物检测;进展期胃癌大体类型
-
进展期胃癌指癌组织侵犯胃壁固有肌层或穿透肌层达浆膜层者。进展期胃癌可根据Borrmann分型将大体形态分为4种类型。BorrmannI型:结节隆起型;Ⅱ型:局限溃疡型;Ⅲ型:浸润溃疡型;IV型:弥漫浸润性(局部Bor.IV,皮革样胃)。
胃癌大体分型:
(1)普通型早期胃癌(EGC)大体分型
Ⅰ型:隆起型(肿瘤凸起于黏膜表面≥0.5cm)
Ⅱ型:浅表型
Ⅱa:浅表隆起型(肿瘤凸起于黏膜表面<0.5cm)
Ⅱb:浅表平坦型
Ⅱc:浅表凹陷型(肿瘤凹陷于黏膜表面<0.5cm)
Ⅲ型:凹陷型(肿瘤凹陷于黏膜表面≥0.5cm)
混合型:如Ⅱa+Ⅱc;Ⅱc+Ⅲ等
(2)特殊类型早期胃癌大体分型
浅表扩散型(肿瘤最大径≥4cm)
微小癌(肿瘤最大径<0.5cm)
小胃癌(0.5cm<肿瘤最大径<1.0cm)
多发性早期胃癌(≥2个独立EGC病灶)
残胃早期癌
(3)进展期胃癌(AGC)大体分型(Borrmann分型)
Ⅰ型:结节隆起型
Ⅱ型:局限溃疡型
Ⅲ型:浸润溃疡型
Ⅳ型:弥漫浸润性(局部Bor.Ⅳ,皮革样胃)
Ⅲ级推荐:
评估是否幽门螺旋杆菌(Hp)感染(ⅠB类)
与NCCN指南比较
NCCN指南指出病理报告中应包括所有内镜黏膜切除术要素及:
-
肿瘤中心位置与EGJ的关系(肿瘤中心点位于胃近端2cm以内并跨越EGJ,按食管癌的分期进行分类;⽽肿瘤中⼼距离近端胃大于2cm的肿瘤,按胃癌分期进行分类。)
-
肿瘤与EGJ是否存在交叉
-
淋巴结状态和已恢复的淋巴结数
-
推荐对所有新诊断的患者通过PCR/NGS进行MSI或通过IHC行MMR通用检测(若之前未行)
四、术前新辅助治疗的手术切除标本
1、大体检查
Ⅰ级推荐:手术标本类型;肿瘤部位;肿瘤大小(cm3);肿瘤距近/远侧切缘距离;淋巴结检出数目和分组(至少检获16枚、最好检获>30枚淋巴结)(对于无明显肿物的标本应仔细检查并多点取材,以免误判肿瘤治疗反应与临床分期)
2、光镜下检查
Ⅰ级推荐:组织学类型/Lauren分型/组织学分级(G1、G2、G3)/浸润深度(pT分期);血管、淋巴管、神经侵犯近/远侧切缘;食管/十二指肠侵犯情况(如切取);淋巴结转移数/受检淋巴结数(pN分期);癌结节数目;远处转移(pM分期);pTNM分期(第8版);肿瘤退缩分级(TRG);ypTNM分期(第8版)
-
肿瘤退缩分级(TRG)的病理学评估根据肿瘤细胞残留及纤维化程度进行分级,推荐使用AJCC第八版/NCCN指南的分级系统。第8版胃癌分期提出了采用ypTNM表示新辅助治疗后手术病理分期。
肿瘤术前辅助治疗效果评估(肿瘤退缩分级,tumor regression grade,TRG):

注:1)肿瘤细胞是指存活的瘤细胞,不包括退变、坏死细胞。
2)放/化疗后可能出现大的无细胞黏液湖,不能将其认为肿瘤残余。
Ⅱ级推荐:用于诊断的免疫组化标志物检测;进展期胃癌大体类型
Ⅲ级推荐:评估是否幽门螺旋杆菌(Hp)感染(ⅠB类)
与NCCN指南比较
NCCN指南强调:
-
对于新辅助治疗后⾁眼所见⽆明显肿瘤残留的s/p标本,应在肿瘤部位⼴泛取样
-
病理学报告应包括⽆术前放化疗胃切除加治疗效果评估在内的所有要素
注:当活检无法取得确诊时,刷片或灌洗液细胞学检测可用于确认是否存在肿瘤;不能手术的晚期胃癌的腹水或胸腔积液脱落细胞学检查、远处转移病灶活检等应按照相应临床病理常规进行处理与诊断。
五、分子诊断
分子分型:经组织病理学确诊后,需进行相关分子检测,根据分子分型指导治疗
-
对于标准治疗失败的晚期胃癌患者可以进行二代测序(NGS)检测寻找潜在的治疗靶点。强调使用获得认证的平台和产品,采取严格的质量控制和规范的操作流程,确保结果的可靠性。
Ⅰ级推荐:
1、所有经病理诊断证实为胃腺癌的病例均有必要进行HER2检测(1A类)
-
HER2阳性晚期胃癌患者可从抗HER2治疗中获益,HER2状态可预测晚期胃癌患者对曲妥珠单抗治疗的反应和生存获益,应当对所有胃癌进行HER2状态检测。
-
据文献报道,基于血液中ctDNA靶向测序的HER2基因体细胞拷贝数结果与荧光原位杂交数据高度一致,对于无法取得活检组织的患者,液体活检HER2扩增情况是一种可能的有效补充手段。基于ctDNA的HER2扩增情况还可用于胃癌患者曲妥珠单抗治疗反应的监测。
-
HER2的免疫组化(IHC)和原位杂交(insituhybridzation,ISH)检测全程应严格按照胃癌HER2检测指南(2016版)建议的操作规范执行,相关检测(IHC、FISH/DSISH)应选用中国国家药品监督管理局批准的试剂盒。
胃癌组织的HER2检测流程:
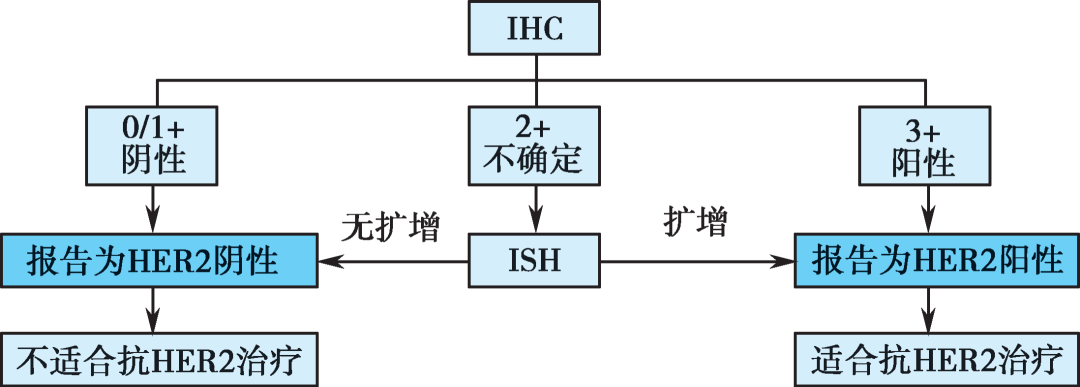
HER2.人表皮生长因子受体2;IHC.免疫组织化学;ISH.原位杂交
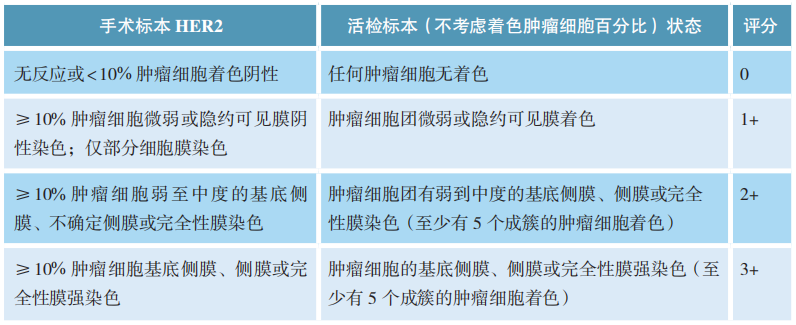
胃癌标本HER2免疫组化检测结果判读和评分标准:
胃癌标本HER2原位杂交检测结果判读:

注:FISH使用×100物镜观察;DSISH使用×(40~60)物镜观察。选择扩增程度最高区域,观察并计数至少20个连续肿瘤细胞核。
2、所有新诊断胃癌都推荐评估MSI/MMR状态(1B类)
-
针对程序性死亡受体-1(PD-1)及其配体-1(,PD-L1)的免疫检查点抑制剂疗法是近年肿瘤免疫治疗的研发热点。对临床上拟采用PD-1/PD-L1抑制剂治疗的胃癌患者,推荐评估微卫星不稳定(MSI)/错配修复缺陷(MMR)状态、PDL1表达与肿瘤TMB,EBV对于免疫治疗的疗效预测价值仍有争议。
-
错配修复(MMR)蛋白检测:免疫组化方法检测MLH1、PMS2、MSH2、MSH6等4个蛋白表达,阳性定位于细胞核,任何一个蛋白表达缺失评价为dMMR(错配修复功能缺陷),所有4个蛋白表达均阳性为pMMR(错配修复功能完整)。
-
微卫星不稳定(MSI):建议采用美国国家癌症研究院(NCI)推荐的5个微卫星检测位点(BAT25、BAT26、D5S346、D2S123、D17S250)。结果分为三级:所有5个位点均稳定为微卫星稳定(MSS),1个位点不稳定为微卫星低度不稳定(MSI-L),2个及2个以上位点不稳定为微卫星高度不稳定(MSI-H)。MSI多由MMR基因突变及功能缺陷导致,也可以通过检测MMR蛋白缺失来反映MSI状态。一般而言,dMMR相当于MSI-H,pMMR相当于MSI-L或MSS。
Ⅱ级推荐:
1、对拟采用PD-1/PD-L1抑制剂治疗的胃癌患者,推荐胃癌组织中评估PD-L1表达状态(2A类)
-
PD-L1检测推荐选用获得认证的抗体与平台,确保检测结果的可靠性。适合进行PD-L1检测标本中的肿瘤细胞必须至少100个。检测报告推荐使用联合阳性分数(CPS)或者肿瘤区域阳性(TAP)评分,CPS=PD-L1染色细胞(包括肿瘤细胞、巨噬细胞与淋巴细胞)的总数/镜下肿瘤细胞总数(×100);TAP=PD-L1阳性的肿瘤细胞与肿瘤相关免疫细胞(包括巨噬细胞与淋巴细胞)/肿瘤总面积×100%。
新增:
2、拟针对Claudin 18.2靶点治疗建议进行Claudin 18.2表达检测(2A类)
-
Claudin 18.2通过免疫组化方法进行检测,目前阳性判读标准仅来自临床试验,Claudin 18.2阳性由肿瘤细胞完整、基底外侧或外侧膜染色的强度,以及肿瘤细胞膜着色所占百分比两个方面决定。但不同的临床研究采用不同的判读标准:MONO研究阳性入组标准为≥50%肿瘤细胞中等或强表达者;FAST研究阳性定义为≥40%的肿瘤细胞中,染色强度为2+或3+的肿瘤;而SPOTLIGHT、GLOW研究使用自动化平台进行检测,人组标准为≥75%肿瘤细胞呈现中到强的膜染色。
Ⅲ级推荐:
NTRK融合基因检测、FGFR2、c-MET检测(2B类)
-
FDA批准了针对NTRK基因融合阳性的实体瘤患者使用TRK抑制剂靶向治疗(如larotrectinib或entrectinib)。对于标准治疗失败的胃癌患者可以进行NTRK基因融合检测,NTRK基因融合可以使用多种方法进行检测,免疫组化方法是一种快速、方便的初筛手段,但仍需要应用FISH或NGS进行验证。
-
对于标准治疗失败的晚期或复发胃癌患者,为了寻找潜在的治疗靶点,可进行FGFR2、c-MET等标志物检测。
与NCCN指南比较
-
NCCN指南专家组推荐首选应用IHC检测HER2,对于IHC检测结果(疑似)为2+的病例推荐随后采用ISH⽅法检测。HER2 IHC检测结果阳性(3+)或阴性(0或1+)的患者无需再行进⼀步ISH检测。HER2:CEP17比值≥2或平均HER2拷贝数≥6.0信号因子/细胞的病例被视为ISH/FISH检测结果阳性。
-
所有新确诊的胃癌患者都应通过聚合酶链反应(PCR)、NGS检测MSI或通过IHC对MMR进行通用检测。
-
对于适合接受PD-1抑制剂治疗的局部晚期、复发或存在转移的胃癌患者,可考虑进行PD-L1检测。
-
靶向⽣物标志物:
HER2过表达/扩增
PD-L1免疫组化表达
微卫星不稳定
肿瘤突变负荷
NTRK基因融合
RET基因融合
BRAF V600E突变
-
对于可能⽆法进行传统活检或疾病进展监测的转移性或晚期胃癌患者,可以考虑液体活检。
六、胃癌报告参考模板
有条件的单位推荐使用标准化的病理报告模板,有助于诊断规范化与后续临床分析,报告模板供参考使用。
胃癌报告参考模板
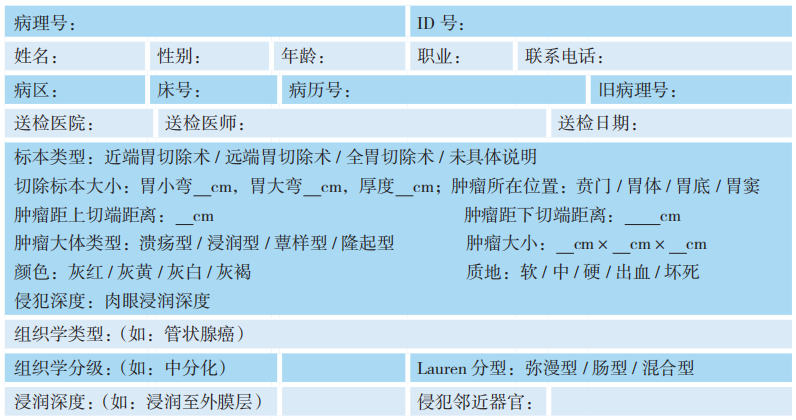
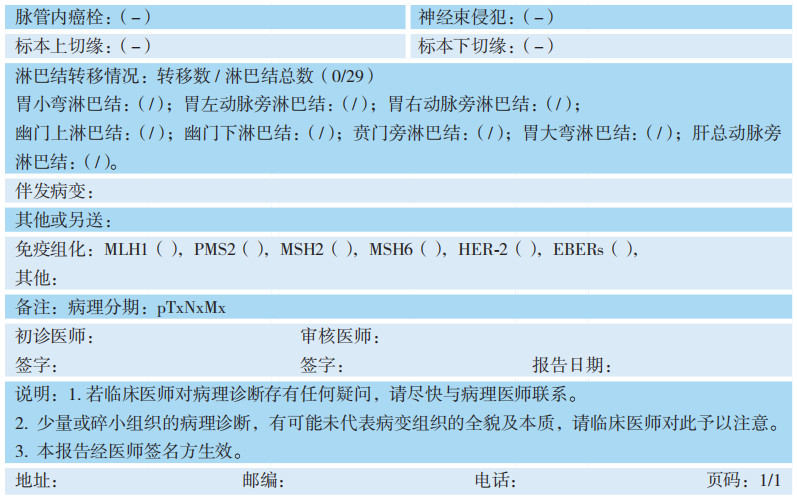
参考文献及书籍:
1.中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)胃癌诊疗指南 2024[M]. 北京 :人民卫生出版社, 2024.
2.NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Gastric Cancer. Version 1.2024
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)